브로민화물
"오늘의AI위키"의 AI를 통해 더욱 풍부하고 폭넓은 지식 경험을 누리세요.
1. 개요
브로민화물은 브로민 음이온(Br-)을 포함하는 화합물을 통칭한다. 자연적으로 해수, 특정 광물 및 해산물에 존재하며, 질산이나 질산은을 이용하여 검출할 수 있다. 브로민화물 염은 물에 용해되어 브로민화물 이온을 생성하며, 브로민은 가수분해 및 산화 반응을 겪는다. 과거에는 진정제 및 조울증 치료에 사용되었으나, 부작용과 안전성 문제로 인해 사용이 감소했다. 생물학적으로는 일부 효소의 보조 인자로 작용하며, 호산구는 항기생충성 브로민화 화합물을 생성하는 데 브로민화물을 사용한다. 유기브로민 화합물 생산 및 사진 젤라틴 실버 공정에도 활용된다.
더 읽어볼만한 페이지
- 이탈기 - 염화 이온
염화 이온은 염소 원자가 전자를 얻어 음전하를 띤 음이온으로, 생물학적 역할, 삼투압 조절, 수생 생태계 및 금속 부식에 영향을 미치며 염화이온 측정기로 농도 측정이 가능하다. - 이탈기 - 아자이드
아자이드는 1890년 쿠르티우스가 발견한 질소 원자를 포함하는 작용기(-N3)를 갖는 화합물의 총칭으로, 에어백 추진제, 고분자 화학, 의약 화학 등 다양한 분야에 응용되지만 폭발성과 독성에 주의해야 한다. - 브로민화물 - 브로민화 에티듐
브로민화 에티듐은 핵산 검출에 사용되는 형광 화합물로, DNA 및 RNA 검출에 활용되며 아가로스 겔 전기영동 시 DNA 밴드를 확인하는 데 사용되지만, 변이원성이 강해 취급에 주의해야 한다. - 브로민화물 - 브로민화 칼륨
브로민화 칼륨은 칼륨과 브로민의 이온 화합물로, 사진 현상액 억제제, 적외선 분광법 윈도우, 수의학에서의 개 간질 치료제 등으로 사용되지만, 과거 인간 간질 치료제로 사용된 이력은 부작용 문제로 현재는 제한적이다. - 음이온 - 황화물
황화물은 황이 다른 원소와 결합한 화합물로, 금속 황화물, 황화광물, 유기 황화물 등 다양한 형태로 존재하며 반도체 특성, 안료, 촉매 등으로 활용되지만 부식성과 유해성을 지니기도 한다. - 음이온 - 산화물
산화물은 산소와 다른 원소의 화합물로, 다양한 화학량론적 조성을 가지며, 여러 분야에 응용되고, 화학 조성이 같더라도 결정 구조가 다른 다형성을 띠기도 하는 비화학량론적 화합물이다.
| 브로민화물 - [화학 물질]에 관한 문서 | |
|---|---|
| 일반 정보 | |
| 화학식 | Br− |
| 몰 질량 | 79.904 g·mol−1 |
| 짝산 | 브롬화 수소 |
 | |
 | |
| 약리학 | |
| ATC 코드 | N05CM11 |
| 반감기 | 12일 |
| 열화학 | |
| 표준 생성 엔탈피 | -121 kJ·mol−1 |
| 엔트로피 | 82 J·mol−1·K−1 |
| 관련 이온 | |
| 기타 음이온 | 플루오린화물 염화물 아이오딘화물 |
| 식별 정보 | |
| CAS 등록번호 | 24959-67-9 |
| UNII | 952902IX06 |
| 펍켐 CID | 259 |
| 켐스파이더 ID | 254 |
| KEGG | C01324 |
| ChEBI | 15858 |
| ChEMBL | 11685 |
| 바일슈타인 등록번호 | 3587179 |
| 겔린 등록번호 | 14908 |
| SMILES | [Br-] |
| 표준 InChI | 1S/BrH/h1H/p-1 |
| 표준 InChIKey | CPELXLSAUQHCOX-UHFFFAOYSA-M |
2. 자연 발생
브로민화물은 일반적인 해수(35 PSU)에 약 65mg/L의 농도로 존재하며, 이는 해수에 녹아있는 염 전체의 약 0.2%를 차지한다. 해산물과 심해 식물은 육지에서 얻은 식품보다 일반적으로 높은 수준의 브로민화물을 함유하고 있다. 자연 발생, 결정질 브롬화은인 브롬은광은 가장 흔한 브로민화물 광물로 알려져 있지만 매우 희귀하다. 은 외에도 브로민은 수은 및 구리와 결합된 광물에도 존재한다.[5]
브로민화물은 일반적인 해수(35 PSU)에 약 65mg/L의 농도로 존재하며, 이는 용존 염 전체의 약 0.2%를 차지한다. 해산물과 심해 식물은 일반적으로 육지에서 얻은 식품보다 높은 수준의 브로민화물을 함유하고 있다. 천연 결정성 브롬은광은 자연 발생, 결정질 브로민화물 광물로 알려져 있지만 매우 희귀하다. 은 외에도 브로민은 수은 및 구리와 결합된 광물에도 존재한다.[5]
3. 화학적 특성
질산 또는 질산은을 사용하여 브로민화물 이온을 검출할 수 있으며, 암모니아수를 통해 크림색 침전이 사라지는 것을 확인할 수 있다.
3. 1. 브로민화물 염의 해리
알칼리 금속, 알칼리 토금속 및 기타 여러 금속의 브로민화물 염은 물(및 일부 알코올 및 소수의 에테르)에 용해되어 브로민화물 이온을 생성한다. 전형적인 예는 물에 완전히 해리되는 브롬화나트륨이다.[1]
:NaBr → Na+ + Br−[1]
3. 2. 브로민의 가수분해
브로민은 물과 쉽게 반응하여 가수분해를 겪는다.[6]
:Br2 + H2O → HOBr + HBr
이는 차아브로민산(HOBr)과 브로민화 수소산(수용액 상태의 HBr)을 생성한다. 이 용액을 "브로민수"라고 부른다.[6] 브로민의 가수분해는 수산화 나트륨과 같은 염기가 존재할 때 더 유리하게 진행된다.[6]
:Br2 + NaOH → NaOBr + NaBr
이 반응은 염소를 수산화 나트륨 존재 하에 용해시켜 표백제를 생산하는 것과 유사하다.[6]
3. 3. 브로민화물의 산화
브로민 이온 검출은 산화제(예: 묽은 HNO3)를 첨가하여 수행할 수 있다.[7] 발라드와 뢰비히의 방법은 해수와 특정 염수에서 브롬을 추출하는 데 사용될 수 있다. 브로민 농도가 충분한지 검사하는 시료에 염소를 첨가하면 브롬(Br2)이 생성된다.[7]
:Cl2 + 2 Br− → 2 Cl− + Br2
4. 의학적 이용
브로민 화합물, 특히 브로민화 칼륨은 19세기와 20세기 초에 진정제로 자주 사용되었다. 미국에서는 만성 독성 때문에 1975년까지 일반 의약품 진정제 및 두통 치료제(예: 브로모-셀처)에 사용되었다.[28] 이러한 사용으로 인해 "브롬화물"이라는 단어는 위안을 주는 상투적인 표현이라는 의미를 갖게 되었다.[15] 제1차 세계 대전 동안 영국 군인들은 성적 충동을 억제하기 위해 브롬화물을 복용했다고 한다.[16]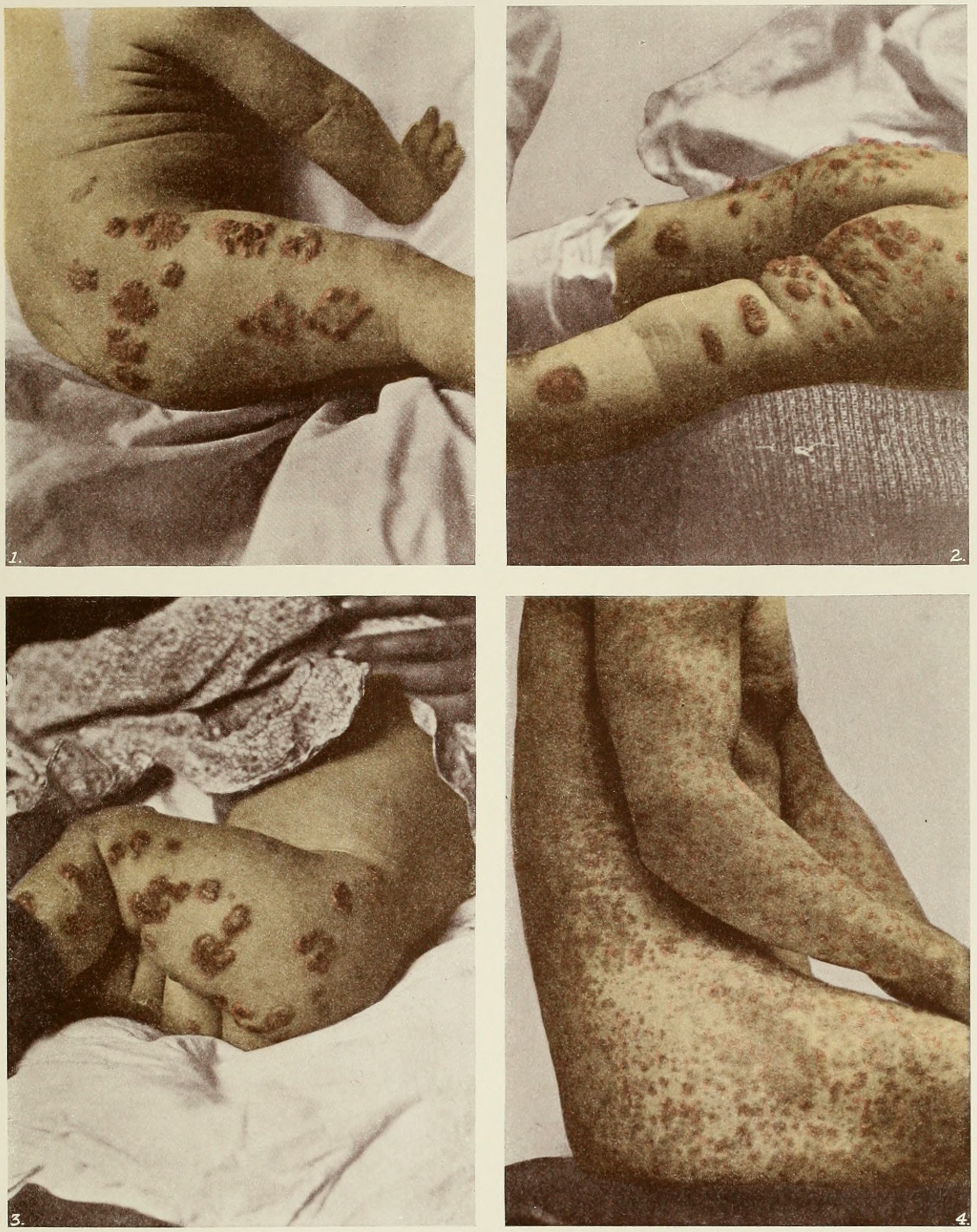
브로민화 리튬은 1900년대 초부터 진정제로 사용되었으나, 1940년대에 더 안전하고 효과적인 진정제(바르비투르산염)가 등장하면서 사용이 줄어들었다.[12] 탄산 리튬, 염화 리튬과 마찬가지로 양극성 장애 치료제로 사용되었다.
1954년부터 1977년까지 오스트레일리아 생화학자 셜리 앤드류스는 빅토리아의 로열 파크 정신 병원에서 리튬을 조울증 치료에 안전하게 사용하는 방법을 연구했다. 앤드류스는 이 연구를 수행하는 동안 브롬이 정신 질환 증상을 유발한다는 것을 발견하여 브롬 사용이 크게 감소했다.[13]
브롬 염은 온수 욕조에서 약한 살균제로 사용되어 ''현장''에서 차아브롬산염을 생성한다.
브롬 이온은 항간질 작용이 있으며, 미국에서는 브롬 염 형태로 수의학에 사용된다.
4. 1. 부작용
브로민화물에 의한 부작용으로는 브롬 중독이 있으며, 이는 다양한 신경 증상을 일으킬 수 있다.[28] 또한, 피부 질환을 유발할 수도 있다. 자세한 내용은 브로민화 칼륨 문서를 참조.5. 생물학적 역할
브로민화물은 생화학에서 자주 언급되지는 않지만, 일부 효소는 브로민화물을 기질 또는 보조 인자로 사용한다. 한 보고서에 따르면 브로민화물은 콜라겐 IV의 설폰이민 가교의 과산화 촉매 작용에 필수적인 보조 인자이다. 이 번역 후 변형은 모든 동물에서 발생하며, 브로민은 인간에게 필수적인 미량 원소이다.[19]
호산구는 다세포 기생충과 싸우기 위해 브로민화물이 필요하다. 차아브로민산염은 호산구 과산화효소를 통해 생성되는데, 이 효소는 염화물을 사용할 수도 있지만 브로민화물을 선호한다.[20] [25]
호주 퀸즐랜드에서 인간 혈액 내 브로민화물의 평균 농도는 5.3±1.4mg/L이며, 나이와 성별에 따라 다르다.[21] 이보다 훨씬 높은 수치는 브롬화 화학 물질에 노출되었음을 나타낼 수 있다. 브로민화물은 해산물에도 존재한다.
브로민화물은 표준적인 해수에 약 65mg/L의 농도로 녹아 있으며, 이는 해수 중 모든 염류의 0.2%에 해당한다. 해산물에는 일반적으로 높은 수준의 브로민화물이 포함되어 있다. 육상에서 얻는 음식의 브로민화물량은 다양하다.
신체에서 브로민화물을 사용하지만, 브로민화물이 생명에 필수적인지는 아직 밝혀지지 않았으며, 일반적으로 그 기능은 염화물에 의해 대체될 수 있다.
6. 기타 응용
브로민화물은 유기브로민 화합물 생산에 사용되며, 유기브로민 화합물은 주로 브롬화 난연제로 사용된다.[8] 일부 브롬화 난연제는 인간과 환경에 잔류성, 생물 축적성 및 독성을 나타내며, 신경 행동 장애와 내분비 교란을 유발하는 것으로 의심된다.[9][10]
AgBr은 사진 젤라틴 실버 공정에 사용되지만, 현재는 대부분 사용되지 않는다.[11]
참조
[1]
웹사이트
Bromide – PubChem Public Chemical Database
https://pubchem.ncbi[...]
National Center for Biotechnology Information
[2]
서적
Chemical Principles
Houghton Mifflin
[3]
논문
Ambiguous bromine
[4]
논문
Revised effective ionic radii and systematic studies of interatomic distances in halides and chalcogenides
1976
[5]
웹사이트
Mindat.org - Mines, Minerals and More
https://www.mindat.o[...]
2018-04-29
[6]
서적
Chemistry of the Elements
Elsevier
[7]
논문
Bromide levels in natural waters: its relationship to levels of both chloride and total dissolved solids and the implications for water treatment
https://linkinghub.e[...]
2021-03-07
[8]
간행물
Bromine Compounds
Wiley-VCH, Weinheim
[9]
웹사이트
Polybrominated Diphenyl Ethers (PBDEs) Action Plan Summary | Existing Chemicals | OPPT | US EPA
http://www.epa.gov/o[...]
2012-12-03
[10]
웹사이트
Brominated Flame Retardants in the Environment
http://www.cerc.usgs[...]
Columbia Environmental Research Center
2012-12-03
[11]
웹사이트
A Guide to Fiber-Base Gelatin Silver Print Condition and Deterioration
http://gawainweaver.[...]
George Eastman House, International Museum of Photography and Film
2009-10-30
[12]
Webarchive
Bipolar disorder
https://www.webmd.co[...]
2022-02-24
[13]
웹사이트
Papers of Shirley Andrews
https://nla.gov.au/n[...]
2022-10-26
[14]
서적
The Great American fraud
https://archive.org/[...]
Press of the American Medical Association
[15]
웹사이트
the definition of bromide
https://www.dictiona[...]
2016-12-21
[16]
서적
Japan's Comfort Women: Sexual slavery and prostitution during World War II and the US Occupation
Routledge
[17]
서적
The Biological Basis of Therapeutics
Macmillan
1970
[18]
논문
The diversity of naturally occurring organobromine compounds
1999
[19]
논문
Bromine Is an Essential Trace Element for Assembly of Collagen IV Scaffolds in Tissue Development and Architecture
[20]
논문
Eosinophils Preferentially Use Bromide to Generate Halogenating Agents
1989-04-05
[21]
논문
Background levels of bromide in human blood
[22]
웹사이트
Bromide – PubChem Public Chemical Database
https://pubchem.ncbi[...]
National Center for Biotechnology Information
2015-12-20
[23]
서적
Chemical Principles 6th Ed.
Houghton Mifflin Company
[24]
문서
Bipolar disorder
http://www.webmd.com[...]
[25]
문서
Eosinophils preferentially use bromide to generate halogenating agents - Mayeno et al. 264 (10): 5660 - Journal of Biological Chemistry
http://www.jbc.org/c[...]
[26]
웹인용
Bromide – PubChem Public Chemical Database
https://pubchem.ncbi[...]
National Center for Biotechnology Information
[27]
서적
Chemical Principles 6th Ed.
https://archive.org/[...]
Houghton Mifflin Company
[28]
서적
The Great American fraud
https://books.google[...]
본 사이트는 AI가 위키백과와 뉴스 기사,정부 간행물,학술 논문등을 바탕으로 정보를 가공하여 제공하는 백과사전형 서비스입니다.
모든 문서는 AI에 의해 자동 생성되며, CC BY-SA 4.0 라이선스에 따라 이용할 수 있습니다.
하지만, 위키백과나 뉴스 기사 자체에 오류, 부정확한 정보, 또는 가짜 뉴스가 포함될 수 있으며, AI는 이러한 내용을 완벽하게 걸러내지 못할 수 있습니다.
따라서 제공되는 정보에 일부 오류나 편향이 있을 수 있으므로, 중요한 정보는 반드시 다른 출처를 통해 교차 검증하시기 바랍니다.
문의하기 : help@durumis.com