오나셈노진아베파르보벡
"오늘의AI위키"의 AI를 통해 더욱 풍부하고 폭넓은 지식 경험을 누리세요.
1. 개요
오나셈노진 아베파르보벡은 5q 염색체의 SMN1 유전자 돌연변이와 관련된 척수성 근위축증 치료를 위해 개발된 생물의약품이다. 정맥 주사로 투여되며, 미국에서는 2세 미만 척수성 근위축증 환자를 대상으로, 유럽 연합과 캐나다에서는 임상 진단을 받았거나 SMN2 유전자를 최대 3개 복사본 가진 환자를 치료하는 데 사용된다. 부작용으로는 구토, 간 효소 증가, 간 문제, 혈소판 감소증 등이 있으며, 개발은 아베시스가 진행하고 노바티스가 인수했다. 2019년 미국 FDA 승인 이후, 여러 국가에서 승인되었지만, 승인 지역별로 적용 범위는 다르다. 치료 비용이 매우 높고, 데이터 조작 논란, 기증 계획에 대한 윤리적 비판 등 사회적, 경제적 논란이 있다.
더 읽어볼만한 페이지
| 오나셈노진아베파르보벡 - [화학 물질]에 관한 문서 | |
|---|---|
| 약물 정보 | |
| 상품명 | 졸겐스마 |
| Drugs.com | Onasemnogene abeparvovec Drugs.com |
| 캐나다 허가 | Rx-only / Schedule D |
| 유럽 연합 허가 | Rx-only |
| DailyMedID | Onasemnogene abeparvovec |
| 미국 허가 | Rx-only |
| 호주 임신 등급 | B2 |
| 투여 경로 | 혈관 내 |
| ATC 코드 | M09AX09 |
| 호주 법적 지위 | S4 |
| 캐나다 법적 지위 | Rx-only / Schedule D |
| 영국 법적 지위 | POM |
| 미국 법적 지위 | Rx-only |
| 유럽 연합 법적 지위 | Rx-only |
| CAS 등록번호 | 1922968-73-7 |
| PubChem | 384585535 |
| DrugBank | DB15528 |
| UNII | MLU3LU3EVV |
| KEGG | D11559 |
| 동의어 | AVXS-101, onasemnogene abeparvovec-xioi |
| GT 대상 유전자 | SMN1 |
| GT 벡터 | 아데노-관련 바이러스 혈청형 9 |
| 추가 정보 | |
| 지속 효과 | 평생 (?) |
2. 적응증 및 사용
오나셈노진 아베파르보벡은 5q 염색체의 ''SMN1'' 유전자 돌연변이와 관련된 질병인 척수성 근위축증 치료를 위해 개발되었으며, 주로 어린 아이들에게 진단되어 근육 기능의 점진적인 상실과 빈번한 사망을 유발한다. 이 약물은 정맥 주입으로 투여된다.[9]
일반적인 부작용으로는 구토와 간 효소 증가가 있다.[63][66] 메스꺼움이 나타날 수 있다.[7] 심각한 부작용으로는 간 문제와 혈소판 감소증이 나타날 수 있다.[7] 임상 시험에서 일시적으로 트로포닌-I 수치가 증가되는 것이 관찰되었으며, 이러한 소견의 임상적 중요성은 알려지지 않았다.[7] 그러나 다른 동물 연구에서는 심장 독성이 관찰되었다.[7] 간부전으로 인한 사망 2명이 보고되었다.[67]
오나셈노진아베파르보벡은 프랑스 근육학 연구소의 연구를 바탕으로, 2018년 노바티스에 인수된 미국의 생명 공학 스타트업 아베시스가 개발하였다.[12][13]
오나셈노진아베파르보벡은 2019년 기준으로 치료당 2125000USD로 세계에서 가장 비싼 약물이었다.[29] 첫 분기 판매액은 1.6억달러였다.[30]
미국에서 오나셈노진 아베파르보벡은 SMN1 유전자의 이중 대립 유전자 돌연변이가 있는 2세 미만의 척수성 근위축증 환자를 치료하는 데 적응증으로 사용된다.[7] 이 치료법은 미국 및 기타 특정 국가에서 2세 미만의 척수성 근위축증 어린이, 질병의 증상 발현 전 단계의 어린이에게도 사용하도록 승인되었다.[25] 유럽 연합과 캐나다에서는 척수성 근위축증 임상 진단을 받았거나, ''SMN2'' 유전자를 최대 3개 복사본 가진 척수성 근위축증 환자를 치료하는 데 사용된다.[5][10][11] 2019년 미국에서 2세 미만 어린이를 대상으로 처음 승인된 이후,[25][7] 오나셈노진아베파르보벡의 승인은 지역별로 다르게 적용된다.[26][27][28]
3. 작용 기전
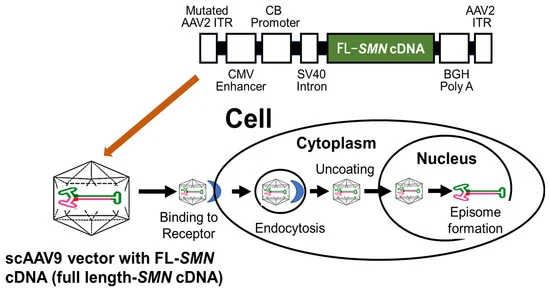
오나셈노진 아베파르보벡은 척수성 근위축증(SMA)의 근본 원인인 ''SMN1'' 유전자 돌연변이를 해결하기 위해 개발된 생물의약품이다. 이 약물은 AAV9 바이러스 캡시드를 운반체로 사용하여, 합성 프로모터와 함께 정상적인 ''SMN1'' 전이 유전자를 포함하고 있다.[4]
오나셈노진 아베파르보벡은 정맥 주사 또는 척수 내 투여를 통해 투여되며, AAV9 바이러스 벡터는 ''SMN1'' 전이 유전자를 손상된 운동 뉴런의 세포 핵으로 운반한다.[51] 전달된 ''SMN1'' 유전자는 SMN 단백질의 생성을 증가시켜 척수성 근위축증의 증상을 완화하고 생명 예후와 운동 기능을 개선한다.[47][51]
운동 뉴런은 세포 분열을 하지 않기 때문에, 오나셈노진 아베파르보벡으로 도입된 ''SMN1'' 유전자는 장기간 안정적으로 유지될 수 있다. 따라서 1회 투여만으로도 평생 효과가 지속될 수 있을 것으로 기대된다.[51][52]
4. 부작용
5. 개발 역사
미국 식품의약국(FDA)은 오나셈노진아베파르보벡에 패스트 트랙, 획기적 치료제, 우선 심사, 희귀 의약품 지정을 부여했다.[25]
6. 사회와 문화
일본에서는 2020년 5월 20일부터 공공 의료 시스템을 통해 이 약물을 사용할 수 있게 되었으며, 일본 공공 의료 시스템에서 보장하는 가장 비싼 약물이 되었다.[31] 중앙사회보험의료협의회는 가격을 환자당 1540000USD (167077222엔)으로 협상했다.[32][33]
내부 고발자는 노바티스가 이 약물에 대한 특정 연구에서 데이터 조작을 했다고 알렸다.[34] 노바티스는 2019년 10월, 실험 동물에서 관찰된 독성 효과를 7개월 동안 미국 식품의약국(FDA)와 유럽 의약품청(EMA)에 알리지 않았음을 인정했다.[37] EMA는 데이터 조작 문제로 인해 이 약물에 대한 신속 평가 허용 결정을 철회했다.[38]
2019년 12월, 노바티스는 연간 100회 투여분의 오나셈노진 아베파르보벡을 미국 외 지역 어린이들에게 추첨을 통해 기증하겠다고 발표했다. 노바티스는 생명 윤리 전문가들의 권고에 따른 것이라고 주장했지만,[39] 유럽 위원회,[40] 일부 유럽 의료 규제 기관[41] 및 환자 단체는 이 결정이 정서적으로 부담스럽고, 최적이 아니며, 윤리적으로 의심스럽다고 비판했다.[42]
6. 1. 법적 지위
2019년 미국에서 2세 미만 어린이를 대상으로 처음 승인된 이후,[25][7] 오나셈노진 아베파르보벡의 승인은 지역별로 다르게 적용된다.[26][27][28]
6. 2. 경제성
Onasemnogene abeparvovec영어의 치료당 가격은 2125000USD로, 2019년 기준으로 세계에서 가장 비싼 약물이다.[29] 첫 번째 분기 판매에서 1.6억달러 상당의 약물이 판매되었다.[30]
일본에서는 2020년 5월 20일부터 공공 의료 시스템을 통해 이 약물을 사용할 수 있게 되었으며, 일본 공공 의료 시스템에서 보장하는 가장 비싼 약물이 되었다.[31] 중앙사회보험의료협의회는 환자당 167077222JPY (약 1540000USD)로 가격을 협상했다.[32][33]
6. 3. 논란
내부 고발자는 노바티스가 이 약물에 대한 특정 연구에서 데이터 조작을 했다고 알렸다.[34] FDA에 제출한 서류에서 노바티스는 브라이언과 앨런 캐스퍼 형제라는 두 명의 임원이 데이터를 조작하고, 다른 사람들에게 데이터 조작을 강요했으며, 이를 은폐하려 했다고 밝혔다.[35][34] 노바티스는 데이터 조작에 책임이 있는 임원들을 해고했지만, 2019년 6월, 약물 승인 한 달 뒤에야 미국 식품의약국(FDA)에 데이터 무결성 문제를 알렸다.[34] FDA는 이러한 지연에 대해 강력하게 비난했다.[36] 2019년 10월, 노바티스는 실험 동물에서 관찰된 정맥 주사 제형의 독성 효과에 대해 7개월 동안 FDA와 유럽 의약품청(EMA)에 알리지 않았음을 인정했다.[37] EMA는 데이터 조작 문제로 인해 이 약물에 대한 신속한 평가를 허용하려던 결정을 철회했다.[38]
2019년 12월, 노바티스는 연간 100회 투여분의 오나셈노진 아베파르보벡을 글로벌 추첨을 통해 미국 외 지역의 어린이들에게 기증할 것이라고 발표했다. 노바티스는 익명의 생명 윤리 전문가들의 권고에 따른 것이라고 주장했지만,[39] 유럽 위원회,[40] 일부 유럽 의료 규제 기관[41] 및 환자 단체는 이 결정이 정서적으로 부담스럽고, 최적이 아니며, 윤리적으로 의심스럽다고 비판했다.[42] 노바티스는 이 계획을 발표하기 전에 가족이나 의사와 상의하지 않았다.[43][44]
노바티스는 추첨 시스템을 통해 오나셈노진 아베파르보벡 투여량을 기증한 것에 대해 비판을 받았다.[40][41][42]
참조
[1]
웹사이트
Zolgensma
https://www.tga.gov.[...]
2021-03-10
[2]
웹사이트
AusPAR: Onasemnogene abeparvovec
https://www.tga.gov.[...]
2021-04-22
[3]
웹사이트
Summary Basis of Decision (SBD) for Zolgensma
https://hpr-rps.hres[...]
2014-10-23
[4]
웹사이트
Zolgensma 2 x 1013 vector genomes/mL solution for infusion - Summary of Product Characteristics (SmPC)
https://www.medicine[...]
2020-06-30
[5]
웹사이트
Zolgensma EPAR
https://www.ema.euro[...]
2020-03-24
[6]
웹사이트
Zolgensma Product information
https://ec.europa.eu[...]
null
[7]
웹사이트
Zolgensma- onasemnogene abeparvovec-xioi kit full prescribing information
https://dailymed.nlm[...]
2019-05-24
[8]
웹사이트
Zolgensma
https://www.fda.gov/[...]
2019-08-06
[9]
서적
LiverTox: Clinical and Research Information on Drug-Induced Liver Injury
NCBI Bookshelf
2020-08-20
[10]
간행물
Health Canada approves Zolgensma, the one-time gene therapy for pediatric patients with spinal muscular atrophy (SMA)
https://www.newswire[...]
Novartis
2020-12-16
[11]
웹사이트
onasemnogene abeparvovec
https://cadth.ca/ona[...]
2020-05-26
[12]
간행물
Novartis successfully completes acquisition of AveXis, Inc.
https://www.novartis[...]
Novartis
null
[13]
간행물
AveXis receives FDA approval for Zolgensma, the first and only gene therapy for pediatric patients with spinal muscular atrophy (SMA)
https://www.novartis[...]
2019-05-24
[14]
웹사이트
EU/3/15/1509
https://www.ema.euro[...]
2018-09-17
[15]
웹사이트
Novartis' Zolgensma Joins Growing List of Medicines to Lose Accelerated Assessment Status in EU
https://www.raps.org[...]
[16]
웹사이트
HMC implements innovative gene therapy to treat congenital spinal muscular atrophy
https://thepeninsula[...]
2019-11-20
[17]
웹사이트
In First, World's Most Expensive Medicine Used to Treat Israeli Toddler
https://www.jewishpr[...]
2019-11-21
[18]
간행물
Global Novartis News Archive
https://www.novartis[...]
null
[19]
웹사이트
Medicamento conhecido como mais caro do mundo recebe registro da Anvisa
https://g1.globo.com[...]
2020-08-17
[20]
간행물
Health Canada approves Zolgensma, the one-time gene therapy for pediatric patients with spinal muscular atrophy (SMA)
https://www.newswire[...]
Novartis Pharmaceuticals Canada
2020-12-16
[21]
웹사이트
PRODUCT MONOGRAPH INCLUDING PATIENT MEDICATION INFORMATION : ZOLGENSMA
https://pdf.hres.ca/[...]
null
[22]
웹사이트
TGA eBS - Product and Consumer Medicine Information Licence
https://www.ebs.tga.[...]
null
[23]
뉴스
Минздрав зарегистрировал препарат для лечения СМА «Золгенсма»
https://www.vedomost[...]
2021-12-09
[24]
뉴스
Toddler with rare genetic condition can be treated after $2m raised, drug registered
https://www.straitst[...]
2023-05-19
[25]
웹사이트
FDA approves innovative gene therapy to treat pediatric patients with spinal muscular atrophy, a rare disease and leading genetic cause of infant mortality
https://www.fda.gov/[...]
2019-05-24
[26]
간행물
Novartis receives approval from Japanese Ministry of Health, Labour and Welfare for Zolgensma the only gene therapy for patients with spinal muscular atrophy (SMA)
https://www.novartis[...]
null
[27]
웹사이트
First Gene Therapy Products Approved in Brazil
https://www.lexology[...]
2020-09-01
[28]
웹사이트
New Zolgensma data demonstrate age-appropriate development when used early, real-world benefit in older children and durability 5+ years post-treatment
https://www.novartis[...]
null
[29]
뉴스
$2.1m Novartis gene therapy to become world's most expensive drug
https://www.theguard[...]
2019-05-25
[30]
뉴스
Novartis' Zolgensma study halted by FDA amid safety questions
https://www.reuters.[...]
2019-10-30
[31]
웹사이트
初の「億超え新薬」ゾルゲンスマの薬価はどう決まったか
https://answers.ten-[...]
AnswersNews
[32]
웹사이트
厚生労働省告示第二百十四号
https://www.mhlw.go.[...]
Ministry of Health, Labour and Welfare, Japan
[33]
웹사이트
脊髄性筋萎縮症に対する遺伝子治療用製品「ゾルゲンスマ®点滴静注」薬価基準収載のお知らせ
https://www.novartis[...]
Novartis Pharma
[34]
뉴스
Novartis blames former AveXis executives for Zolgensma data manipulation
https://news.yahoo.c[...]
2019-09-24
[35]
뉴스
Novartis to put AveXis into protective custody after data manipulation scandal
https://www.fierceph[...]
2019-09-24
[36]
간행물
Statement on data accuracy issues with recently approved gene therapy
https://www.fda.gov/[...]
2019-12-01
[37]
뉴스
Novartis says delayed telling FDA of Zolgensma concern due to 'mistake'
https://www.reuters.[...]
2019-11-11
[38]
웹사이트
Zolgensma°: the drug of extremes
https://english.pres[...]
2020-04-01
[39]
뉴스
Novartis in talks with patients upset about lottery-like gene therapy giveaway
https://www.reuters.[...]
Reuters
2021-05-29
[40]
웹사이트
Answer given by Ms Kyriakides on behalf of the European Commission
https://www.europarl[...]
2020-04-21
[41]
웹사이트
No "lottery for life" - Statement by Beneluxa Health Ministers addressing the global managed access program designed by Novartis and Avexis
https://beneluxa.org[...]
2020-04-21
[42]
웹사이트
AVXS-101 (Zolgensma) to be made available globally through a controversial programme
https://www.sma-euro[...]
2020-04-21
[43]
뉴스
Dismay at lottery for $2.1m drug to treat children with muscle-wasting disease
https://www.theguard[...]
2019-12-21
[44]
뉴스
Novartis to Offer World's Most Expensive Drug for Free Via Lottery
https://www.wsj.com/[...]
2019-12-21
[45]
논문
International nonproprietary names for pharmaceutical substances (INN): recommended INN: list 79
[46]
웹사이트
Onasemnogene abeparvovec (USAN/INN)
https://pubchem.ncbi[...]
2021-09-09
[47]
웹사이트
1人あたり約1億7000万円!…驚愕の高額新薬「ゾルゲンスマ」は財政を破壊するのか
https://weekly-econo[...]
エコノミストOnline
2022-01-08
[48]
웹사이트
Onasemnogene abeparvovec - AveXis - AdisInsight
https://adisinsight.[...]
2018-10-06
[49]
웹사이트
KEGG DRUG: オナセムノゲンアベパルボベック
https://www.kegg.jp/[...]
2020-02-27
[50]
웹사이트
ゾルゲンスマ 添付文書
https://www.data-ind[...]
2024-09-06
[51]
웹사이트
初の「億超え新薬」ゾルゲンスマの薬価はどう決まったか
https://answers.ten-[...]
Answers News
2022-01-08
[52]
웹사이트
Novartis announces FDA filing acceptance and Priority Review of AVXS-101, a one-time treatment designed to address the genetic root cause of SMA Type 1
https://www.novartis[...]
Novartis
2018-12-04
[53]
웹사이트
AveXis receives FDA approval for ZolgensmaR, the first gene therapy for paediatric patients with SMA
https://www.sma-euro[...]
2019-05-25
[54]
웹사이트
Novartis successfully completes acquisition of AveXis, Inc.
https://www.novartis[...]
Novartis
2018-10-06
[55]
뉴스
Slovenian Firm Involved in First Gene Therapy for Spinal Muscular Atrophy
https://www.total-sl[...]
Total Slovenia News
2019-06-03
[56]
웹사이트
FDA approves innovative gene therapy to treat pediatric patients with spinal muscular atrophy, a rare disease and leading genetic cause of infant mortality
http://www.fda.gov/n[...]
미국 식품의약품국
2019-05-24
[57]
뉴스
$2.1m Novartis gene therapy to become world's most expensive drug
https://www.theguard[...]
2019-05-25
[58]
뉴스
2億円、「世界一高い薬」承認へ 脊髄性筋萎縮症の治療薬
https://www.47news.j[...]
2020-02-27
[59]
웹인용
Zolgensma
https://www.tga.gov.[...]
2021-09-08
[60]
웹인용
AusPAR: Onasemnogene abeparvovec
https://www.tga.gov.[...]
2021-09-08
[61]
웹인용
Summary Basis of Decision (SBD) for Zolgensma
https://hpr-rps.hres[...]
2022-05-29
[62]
웹인용
Zolgensma 2 x 1013 vector genomes/mL solution for infusion - Summary of Product Characteristics (SmPC)
https://www.medicine[...]
2020-07-30
[63]
웹인용
Zolgensma- onasemnogene abeparvovec-xioi kit full prescribing information
https://dailymed.nlm[...]
2019-11-18
[64]
웹인용
Zolgensma
https://www.fda.gov/[...]
2019-11-01
[65]
웹인용
FDA approves innovative gene therapy to treat pediatric patients with spinal muscular atrophy, a rare disease and leading genetic cause of infant mortality
https://www.fda.gov/[...]
2019-11-18
[66]
웹인용
Zolgensma EPAR
https://www.ema.euro[...]
2020-07-30
[67]
뉴스
졸겐스마 환자 2명 간부전 사망 첫 보고
http://www.bosa.co.k[...]
2022-08-23
본 사이트는 AI가 위키백과와 뉴스 기사,정부 간행물,학술 논문등을 바탕으로 정보를 가공하여 제공하는 백과사전형 서비스입니다.
모든 문서는 AI에 의해 자동 생성되며, CC BY-SA 4.0 라이선스에 따라 이용할 수 있습니다.
하지만, 위키백과나 뉴스 기사 자체에 오류, 부정확한 정보, 또는 가짜 뉴스가 포함될 수 있으며, AI는 이러한 내용을 완벽하게 걸러내지 못할 수 있습니다.
따라서 제공되는 정보에 일부 오류나 편향이 있을 수 있으므로, 중요한 정보는 반드시 다른 출처를 통해 교차 검증하시기 바랍니다.
문의하기 : help@durumis.com