면역 형광법
"오늘의AI위키"의 AI를 통해 더욱 풍부하고 폭넓은 지식 경험을 누리세요.
1. 개요
면역 형광법은 항체에 형광 물질을 결합하여 항원-항체 반응을 시각화하는 기술로, 앨버트 쿤스 등에 의해 1950년대에 개발되었다. 이 기술은 면역학, 세포생물학, 병리학 등 다양한 분야에서 항원의 존재를 확인하고 분포를 파악하는 데 사용된다. 면역 형광법은 직접법과 간접법으로 나뉘며, 형광체의 종류와 형광 현미경 기술의 발전을 통해 지속적으로 개선되고 있다. 하지만 세포의 투과성 문제, 광퇴색, 자가 형광, 스펙트럼 중첩 등의 한계점도 존재한다.
더 읽어볼만한 페이지
- 면역 검사 - C-반응성 단백질
C-반응성 단백질(CRP)은 간에서 생성되는 단백질로, 염증 반응의 지표로 사용되며, 세균 감염, 조직 손상, 자가면역 질환 등에서 혈중 농도가 증가하여 면역 반응에 기여한다. - 면역 검사 - 헤마글루티닌
헤마글루티닌은 바이러스 표면에 존재하는 당단백질로, 숙주 세포의 시알산에 결합하여 세포 침투를 돕고 유전 물질을 전달하며, 혈청학적 분석 및 질병 진단에 활용된다. - 해부병리학 - 위축
위축은 정상적인 발달이나 질병으로 인해 신체 조직이나 기관의 크기가 감소하는 현상을 의미하며, 정상적인 발달, 노화, 질병, 약물 사용 등 다양한 원인에 의해 발생한다. - 해부병리학 - 육종 (종양)
육종은 골육종과 연조직 육종으로 분류되며, 뼈와 연부조직에서 발생하는 악성 종양으로, 방사선 노출, 유전적 요인 등이 위험 요인으로 작용하며, 영상 검사, 생검을 통해 진단하고 수술, 화학요법, 방사선 치료 등을 시행한다.
| 면역 형광법 |
|---|
2. 역사
앨버트 쿤스(Albert Coons) 등에 의해 1950년대에 발표되었다.[25][26][27][24]
면역형광법은 형광 염료로 표지된 항체를 사용하여 항원-항체 반응을 통해 항원을 검출하고 시각화하는 방법이다. 특이적인 면역 반응을 사용하므로 특이성이 우수하다. 항체가 항원에서 인식하는 특정 영역을 에피토프라고 한다. 형광 염료는 촉매하는 화학 반응에 의해 소모되지 않고, 분해능과 신호 대 잡음비가 우수하며, 다중 염색을 한 경우에도 식별성이 뛰어나다. 형광 현미경이나 공초점 레이저 현미경을 사용하면 기존의 광학 현미경의 검출 한계 이하의 해상도에 도달할 수 있다고 여겨진다. 효소 항체법과 비교했을 때, 형광 항체법은 효소처럼 온도나 pH 등의 조건에 따라 반응 생성물의 양이 증감하는 일이 없으므로, 항원의 양과 형광량의 상관 관계는 비교적 좋다고 생각된다[23].
3. 원리
단순한 항원의 소재 분포를 가시화하는 목적뿐만 아니라, DNA 메틸화의 진행 정도와 소재의 분포 상황에 대한 지견을 얻기 위한 반정량적인 방법으로도 사용 가능하다. 현미경의 한계 성능까지 사용하는 경우도 많으며, 렌즈는 유침의 높은 개구수 (NA)의 것을 사용한다[23]. 특정 항원에 대응하는 항체에 형광 색소를 표지하여 항원-항체 반응에 의해 항원의 존재를 검출하고, 분포 상황을 시각화한다.[24]
3. 1. 형광 색소
면역형광법에 사용되는 대표적인 형광 색소는 다음과 같다.
이 외에도 다양한 형광 색소가 개발되어 사용되고 있다.
4. 종류
면역형광법은 크게 직접법과 간접법으로 나뉜다. 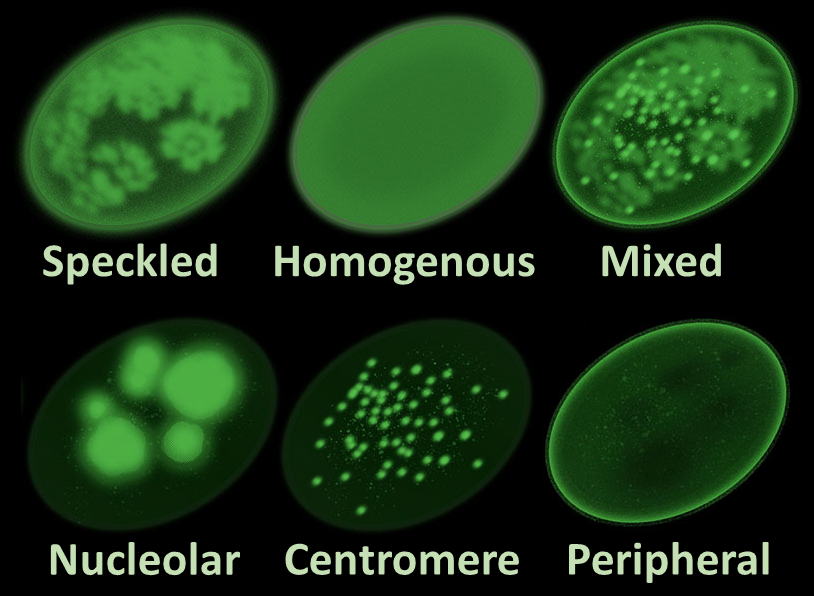
직접법은 형광 물질이 결합된 일차 항체를 이용하고, 간접법은 표지되지 않은 일차 항체와 형광 표지된 이차 항체를 이용한다. 직접법은 간편하지만 민감도가 낮고, 간접법은 복잡하지만 다양한 이차 항체를 이용할 수 있어 유연성이 높고 신호 증폭이 가능하다.[23]
4. 1. 직접법 (Primary Immunofluorescence)
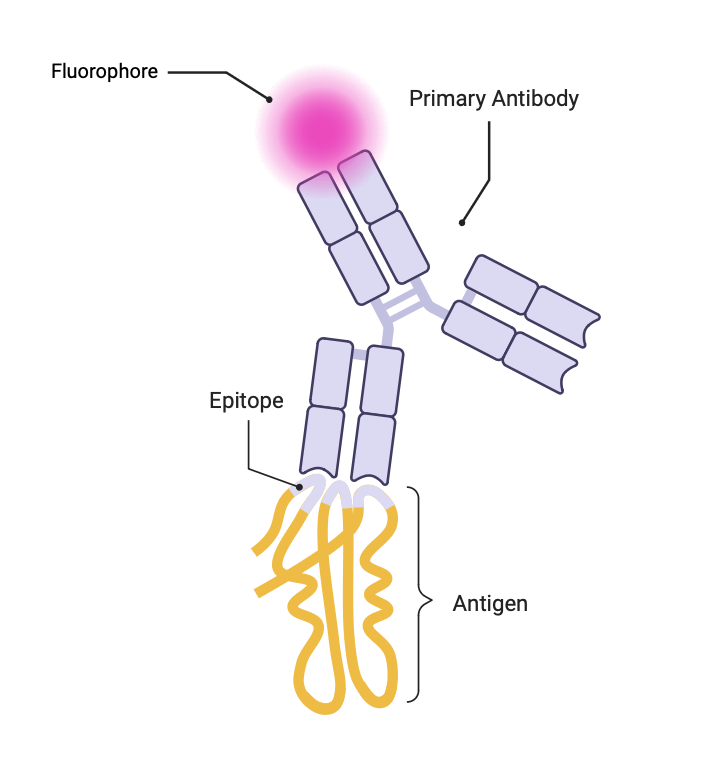
일차(직접) 면역 형광법(DIF)은 형광체와 접합된 단일 항체를 사용한다. 항체는 표적 분자(항원)를 인식하여 에피토프라고 불리는 특정 부위에 결합한다. 부착된 형광체는 형광 현미경을 통해 감지할 수 있으며, 형광체의 종류에 따라 여기된 후 특정 파장의 빛을 방출한다.[1][14]
형광체를 항체에 직접 부착하면 시료 준비 절차의 단계가 줄어들어 시간과 분석 중 비특이적 배경 신호를 줄일 수 있다.[12] 또한 항체 교차 반응의 가능성과 전체 과정에서의 실수를 제한한다. DIF의 한 가지 단점은 항원에 결합할 수 있는 항체의 수가 제한된다는 것이다. 이러한 제한으로 인해 기술에 대한 민감도가 감소할 수 있다. 표적 단백질이 소량만 존재하는 경우, 이차 면역 형광법이 더 나은 접근 방식이며, 이차(간접) 면역 형광법과 비교할 때 DIF보다 더 민감한 것으로 간주된다.[2][12][1]
'''직접법'''은 형광 물질을 화학적으로 결합한 단일 일차 항체를 이용한다. 일차 항체는 표적 분자(항원)를 인식하는 특정 부위인 에피토프에 결합한다. 이는 적응 면역을 가진 생물의 면역 반응을 조작하는 과정을 통해 달성된다. 표지된 형광 색소는 형광 현미경으로 검출 가능하며 단파장의 빛에 의해 여기되면 각 형광 색소에 고유한 파장의 빛을 방출한다.[23]
4. 2. 간접법 (Secondary Immunofluorescence)
형광단이 항체에 접합("태그")되는 면역 형광 염색 절차는 유지된 세포 내 발현 항체와 살아있는 세포의 세포 표면 항원에 모두 적용할 수 있다. 면역 형광 기술에는 1차(직접) 및 2차(간접)의 두 가지 일반적인 종류가 있다.[1][2]간접법(Secondary Immunofluorescence, SIF)은 형광 물질이 접합되지 않은 1차 항체를 사용하고, 형광 물질이 결합된 2차 항체를 사용하여 1차 항체를 검출한다. 2차 항체는 1차 항체에 특이적으로 결합한다.[1]
이 기법은 직접법보다 복잡하고 시간이 걸리지만, 다양한 2차 항체 및 검출 방법을 특정 1차 항체에 사용할 수 있으므로 유연성이 높아진다.[23]
4. 2. 1. 신호 증폭 기법
2차(간접) 면역 형광법은 여러 개의 2차 항체가 동일한 1차 항체에 결합할 수 있기 때문에 1차 면역 형광법보다 더 민감하게 여겨진다. 항원당 형광 물질 분자 수가 증가하면 방출되는 빛의 양이 증가하여 신호가 증폭된다.[1] 간접법의 민감도를 더욱 높이기 위해 아비딘-비오틴 복합체(ABC 방법)[15], 표지된 스트렙타비딘-비오틴(LSAB 방법)[16]과 같은 신호 증폭 기법들이 사용된다.5. 한계
면역형광법은 몇 가지 한계점을 가지고 있다. 우선 항체가 큰 단백질이기 때문에 일반적으로 살아있는 세포의 온전한 세포막이나 세포 내 막을 통과하지 못하며, 이로 인해 세포 내 구조를 연구할 때 고정된 세포에만 제한된다. 또한, 형광 물질은 빛에 노출되면 점차 형광을 잃는 광퇴색 현상이 발생한다. 이외에도 자가 형광, 스펙트럼 중첩, 비특이적 염색과 같은 문제들이 발생할 수 있다.[1][2]
5. 1. 세포 투과성 문제
항체는 큰 단백질이기 때문에 일반적으로 살아있는 세포의 온전한 세포막이나 세포 내 막을 통과하지 못한다.[17] 따라서 면역 형광법은 세포 내 구조를 연구할 때 고정된(죽은) 세포에만 제한된다. 항원 물질은 세포 내부의 자연적인 위치에 단단히 고정되어야 이러한 구조를 시각화할 수 있다.[17] 살아있는 세포 내 구조를 형광으로 연구하기 위해 녹색 형광 단백질(GFP)과 같은 형광 단백질 도메인을 포함하는 재조합 단백질을 사용할 수 있다. GFP 기술은 세포의 유전 정보를 변경하는 것을 포함한다.[18][19]5. 2. 광퇴색 (Photobleaching)
형광 물질은 빛에 노출되면 점차 형광을 잃는 광퇴색 현상이 발생한다.[12] 이는 형광체의 영구적인 빛 방출 능력 손실을 의미한다.[1] 광퇴색을 줄이기 위해 다양한 전략을 사용할 수 있다. 빛 노출 강도나 시간을 줄이면 형광 빛의 흡수-방출 주기가 감소하여 형광체의 기능을 보존할 수 있다. 또한 형광체의 농도를 높이거나, Alexa Fluors, Seta Fluors 또는 DyLight Fluors와 같이 광퇴색에 대한 내성이 있는 보다 강력한 형광체를 선택할 수도 있다.[2]5. 3. 기타 문제점
면역 형광법을 사용할 때 발생할 수 있는 주요 문제점으로는 광퇴색, 자가 형광, 스펙트럼 중첩, 비특이적 염색 등이 있다.[1][2]- 광퇴색(Photobleaching): 형광체가 빛에 노출되어 영구적으로 빛 방출 능력을 잃는 현상이다.[12][1] 빛 노출 강도나 시간을 줄이거나, 형광체 농도를 높이거나, Alexa Fluors, Seta Fluors, DyLight Fluors와 같이 광퇴색에 강한 형광체를 사용하여 광퇴색 위험을 줄일 수 있다.[2]
- 자가 형광(Autofluorescence): 샘플 조직이나 세포 자체가 자연적으로 형광을 방출하는 현상이다.[1][2]
- 스펙트럼 중첩(Spectral overlap): 여러 형광 물질을 동시에 사용할 때, 각 형광 물질의 방출 스펙트럼이 겹쳐서 잘못된 신호를 발생시키는 현상이다.[1][2]
- 비특이적 염색(Nonspecific staining): 항체가 의도하지 않은 단백질에 결합하여 위양성 결과를 초래하는 현상이다.[2][4][1]
6. 발전
면역 형광법은 형광체와 형광 현미경 기술의 발전에 힘입어 지속적으로 발전하고 있다. 형광체는 더 밝고 광안정성이 뛰어나면서도, 세포 투과성과 스펙트럼 특성을 유지하도록 개선되고 있다.[20] 또한, 초고해상도 현미경의 개발로 회절 한계 이상의 해상도를 가진 이미지를 얻을 수 있게 되어, 세포 내 구조를 더 자세히 관찰할 수 있게 되었다.[21]
6. 1. 형광체 개발
형광체는 밝기와 광안정성을 향상시키면서 스펙트럼 특성과 세포 투과성을 유지하도록 구조적으로 수정될 수 있다.[20]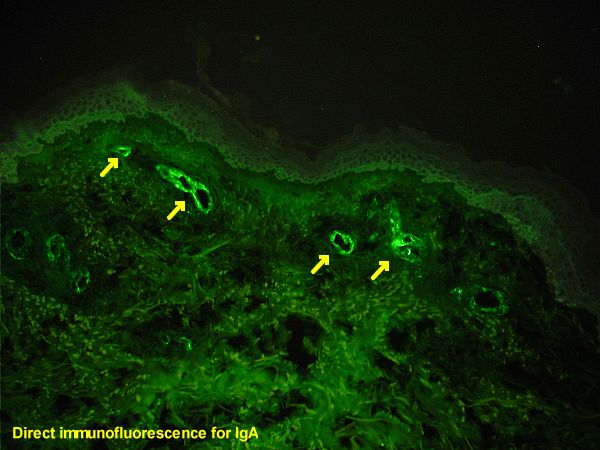
6. 2. 초고해상도 현미경 (Super-resolution microscopy)
초고해상도 형광 현미경 방법은 회절 한계에 의해 부과된 현미경보다 더 높은 해상도의 이미지를 생성할 수 있다. 이를 통해 세포 내의 구조적 세부 사항을 파악할 수 있다.[21] 더 구체적으로는 형광에서의 초고해상도는 인접한 스펙트럼상 동일한 형광체(스펙트럼 중첩)의 동시 형광을 방지하는 현미경의 능력을 의미한다. 최근 개발된 초고해상도 형광 현미경 방법에는 자극 방출 소멸(STED) 현미경, 포화 구조화 조명 현미경(SSIM), 형광 광활성화 국소화 현미경(FPALM), 확률적 광학 재구성 현미경(STORM) 등이 있다.[22]7. 관련 인물
- 앨버트 쿤스(1912-1978): 의사, 병리학자, 면역학자이다.
- 코넬리아 미첼 다운스(1892–1987): 미생물학자, 저널리스트이다.
참조
[1]
논문
Immunofluorescence Techniques
2013-01-01
[2]
서적
Immunofluorescence
https://linkinghub.e[...]
Elsevier
2024-02-14
[3]
논문
Mapping the epitopes of antibodies
2007-01-01
[4]
논문
Chemical labeling strategies for cell biology
https://www.nature.c[...]
2006-08
[5]
논문
Properties of Spin and Fluorescent Labels at a Receptor-Ligand Interface
1999-10
[6]
논문
Neurobiology thanks to microbiology: The legacy of Albert H. Coons (1912–1978)
https://linkinghub.e[...]
1999-11
[7]
논문
Multiplex Immunofluorescence: A Powerful Tool in Cancer Immunotherapy
2023-02-04
[8]
논문
Different intermediate-sized filaments distinguished by immunofluorescence microscopy
1978-10
[9]
논문
Membrane topology of the human breast cancer resistance protein (BCRP/ABCG2) determined by epitope insertion and immunofluorescence
2008-12
[10]
논문
Understanding the complexity of antigen retrieval of DNA methylation for immunofluorescence-based measurement and an approach to challenge
https://linkinghub.e[...]
2015-01
[11]
논문
Application of DAPI and immunofluorescence for enhanced identification of Cryptosporidium spp oocysts in water samples
https://linkinghub.e[...]
1994-03
[12]
논문
Ten Approaches That Improve Immunostaining: A Review of the Latest Advances for the Optimization of Immunofluorescence
2022-01-26
[13]
논문
Anti-Nuclear Antibodies Patterns in Patients With Systemic Lupus Erythematosus and Their Correlation With Other Diagnostic Immunological Parameters.
[14]
서적
IHC Guidebook
Dako Denmark A/S, An Agilent Technologies Company
2014-05-14
[15]
서적
An Introduction to Performing Immunofluorescence Staining
Springer New York
2019
[16]
논문
Machine-based method for multiplex in situ molecular characterization of tissues by immunofluorescence detection
2015-03-31
[17]
웹사이트
Fixation and Permeabilization in in[sic] Immunocytochemistry/Immunofluorescence (ICC/IF)
https://www.novusbio[...]
2024-02-14
[18]
논문
GFP technology for live cell imaging
https://linkinghub.e[...]
2003-12
[19]
논문
Green fluorescent protein
1995-10
[20]
논문
A general method to improve fluorophores for live-cell and single-molecule microscopy
2015-03
[21]
논문
Super-resolution fluorescence microscopy
2009-06-02
[22]
논문
Review of Super-Resolution Fluorescence Microscopy for Biology
http://journals.sage[...]
2011-09-01
[23]
웹사이트
蛍光抗体法とは
http://www2.clst.rik[...]
理化学研究所 生命機能科学研究センター 超微形態研究チーム
2020-09-28
[24]
웹사이트
蛍光抗体法と酵素抗体法の比較
https://www.nichirei[...]
2020-09-28
[25]
논문
"Immunological properties of an antibody containing a fluorescent group."
1941
[26]
논문
"Localization of antigen in tissue cells: II. Improvements in a method for the detection of antigen by means of fluorescent antibody."
1950
[27]
논문
"Studies on antibody production: II. The primary and secondary responses in the popliteal lymph node of the rabbit."
1955
본 사이트는 AI가 위키백과와 뉴스 기사,정부 간행물,학술 논문등을 바탕으로 정보를 가공하여 제공하는 백과사전형 서비스입니다.
모든 문서는 AI에 의해 자동 생성되며, CC BY-SA 4.0 라이선스에 따라 이용할 수 있습니다.
하지만, 위키백과나 뉴스 기사 자체에 오류, 부정확한 정보, 또는 가짜 뉴스가 포함될 수 있으며, AI는 이러한 내용을 완벽하게 걸러내지 못할 수 있습니다.
따라서 제공되는 정보에 일부 오류나 편향이 있을 수 있으므로, 중요한 정보는 반드시 다른 출처를 통해 교차 검증하시기 바랍니다.
문의하기 : help@durumis.com