핵의학
"오늘의AI위키"의 AI를 통해 더욱 풍부하고 폭넓은 지식 경험을 누리세요.
1. 개요
핵의학은 방사성 물질을 사용하여 질병을 진단하고 치료하는 의학 분야이다. 주로 인체 내부의 생리적 기능을 영상화하는 데 초점을 맞추며, 신티그래피, SPECT, PET 등의 기술을 활용한다. 진단 핵의학에서는 방사성 추적자를 사용하여 2차원 또는 3차원 영상을 얻어 질병의 징후를 파악하며, 암, 심장 질환, 신경계 질환 등의 진단에 활용된다. 중재적 핵의학에서는 방사성 물질을 직접 체내에 투여하여 갑상선 기능 항진증, 림프종, 골통 등을 치료한다. 핵의학은 원자로 또는 사이클로트론에서 생산된 방사성 동위원소를 사용하며, 방사선량 관리 및 안전 규정을 준수하여 시행된다.
더 읽어볼만한 페이지
| 핵의학 | |
|---|---|
| 기본 정보 | |
 | |
| 분류 | |
| ICD-10-PCS | CC |
| ICD-9 | 92 |
| MeSH ID | D009683 |
| OPS-301 | 3-70 3-72 8-53 |
| 기타 코드 | 핵의학 |
2. 진단 핵의학 영상
2. 1. 진단
신티그래피(''신트'')는 내부 방사성핵종을 사용하여 2차원 영상을 만드는 것이다.[4]''SPECT''는 여러 투영의 감마 카메라 데이터를 사용하는 3D 단층 촬영 기법으로, 다른 평면에서 재구성할 수 있다. ''양전자 방출 단층 촬영''(PET)은 일치 검출을 사용하여 기능적 과정을 영상화한다.
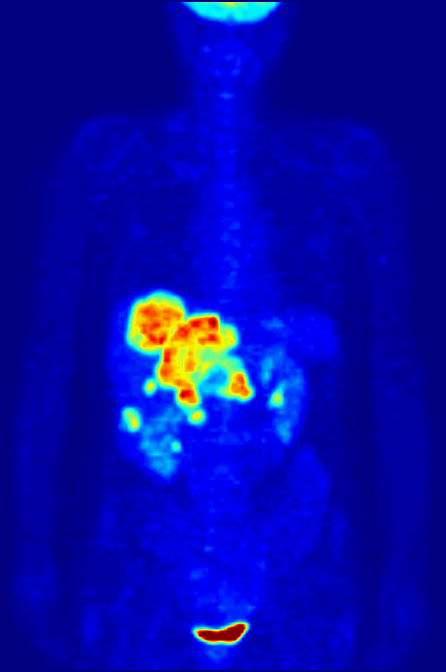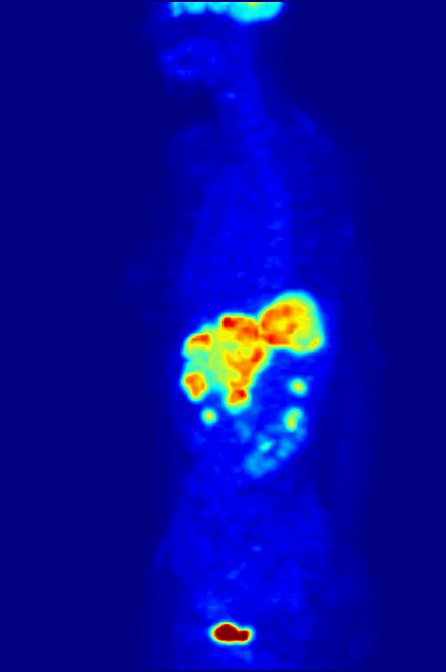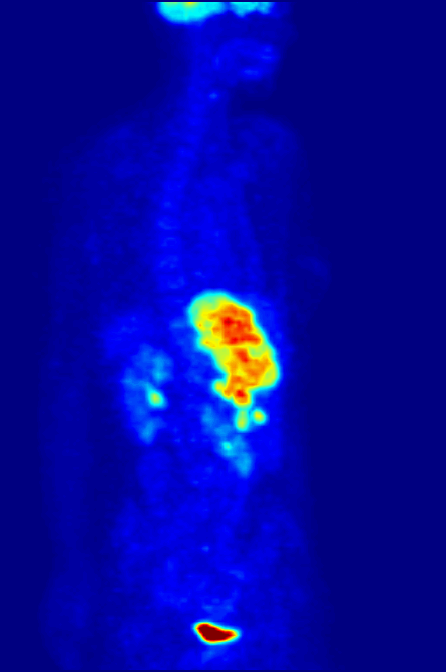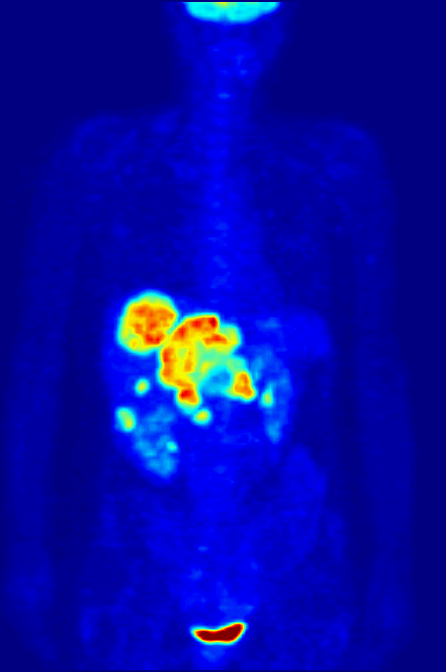
핵의학 검사는 대부분의 다른 영상 기법과 달리, CT나 MRI와 같은 기존의 해부학적 영상과는 달리 조사 중인 시스템의 생리적 기능을 주로 보여준다. 핵의학 영상 연구는 일반적으로 특정 신체 부위(예: 흉부 X선, 복부/골반 CT 스캔, 두부 CT 스캔 등)에 초점을 맞춘 기존 방사선 영상보다 장기, 조직 또는 질병 특이적(예: 폐 스캔, 심장 스캔, 골 스캔, 뇌 스캔, 종양, 감염, 파킨슨병 등)이다. 또한 특정 세포 수용체나 기능을 기반으로 전신 영상을 얻을 수 있는 핵의학 연구가 있다. 예를 들어 전신 PET 스캔 또는 PET/CT 스캔, 갈륨 스캔, 인듐 백혈구 스캔, MIBG 및 옥트레오티드 스캔이 있다.
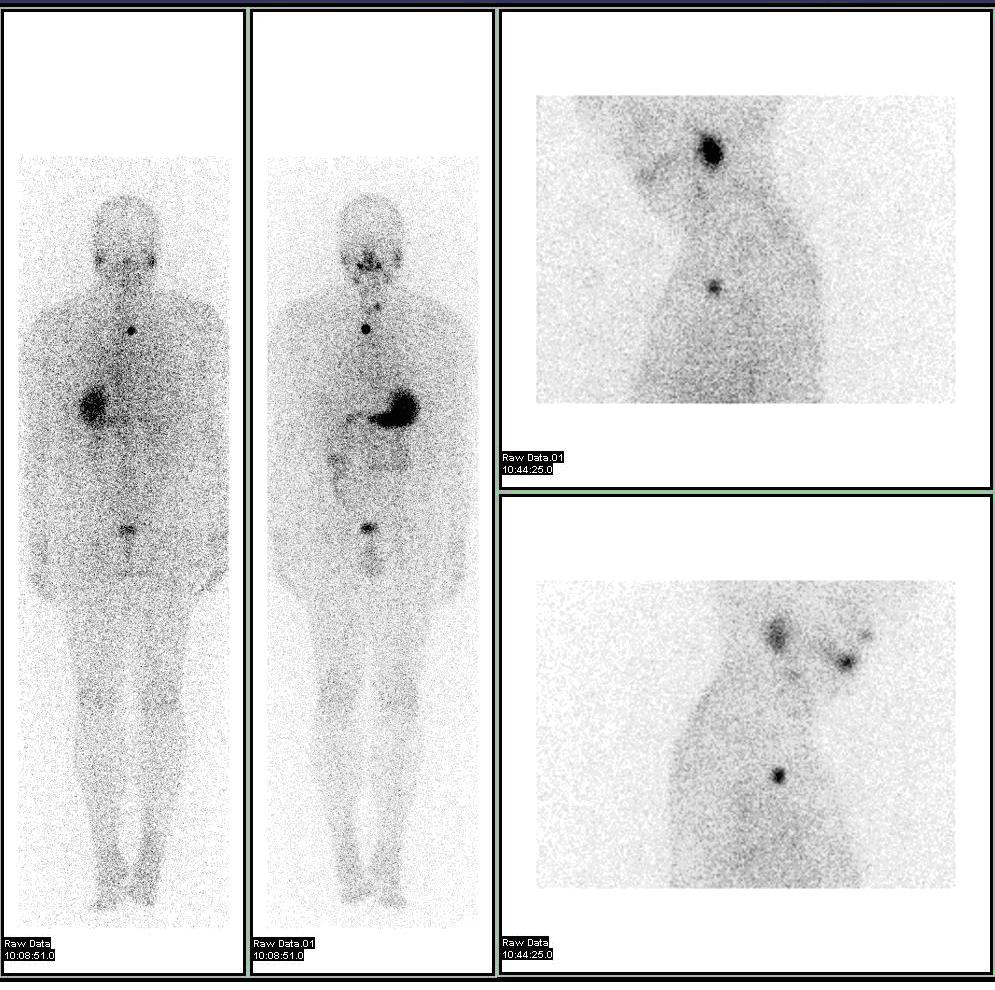
신체의 대사가 질병 과정을 영상화하는 능력은 탁월하지만 독특한 것은 아니다. fMRI와 같은 특정 기술은 혈류를 통해 조직(특히 뇌 조직)의 영상을 생성하여 대사를 보여준다. 또한 CT와 MRI 모두에서 조영 증강 기술은 염증 과정으로 인해 약물을 다르게 처리하는 조직 영역을 보여준다.
핵의학의 진단 검사는 질병이나 병리가 존재할 때 신체가 물질을 다르게 처리하는 방식을 이용한다. 신체에 도입된 방사성핵종은 종종 신체 내에서 특징적으로 작용하는 복합체에 화학적으로 결합되어 있으며, 이는 일반적으로 추적자로 알려져 있다. 질병이 있을 경우 추적자는 신체 주변에 분포되거나 다르게 처리되는 경우가 많다. 예를 들어, 리간드 메틸렌-디포스포네이트(MDP)는 골에 의해 우선적으로 흡수될 수 있다. 테크네튬-99m을 MDP에 화학적으로 부착함으로써 방사능을 수송하고 수산화인회석을 통해 골에 부착하여 영상화할 수 있다. 골절과 같이 생리적 기능이 증가하면 추적자의 농도가 증가하는 경우가 많다. 이는 종종 방사능 축적의 국소적 증가 또는 생리적 시스템 전체의 방사능 축적의 전반적인 증가인 "핫 스폿"의 출현으로 이어집니다. 일부 질병 과정은 추적자의 배제를 초래하여 "콜드 스폿"의 출현으로 이어집니다. 많은 추적자 복합체가 많은 다른 장기, 샘 및 생리적 과정을 영상화하거나 치료하기 위해 개발되었다.
2. 1. 1. 2차원 영상: 신티그래피
신티그래피는 체내에 투여된 방사성 핵종을 이용하여 2차원 영상을 생성하는 핵의학 검사 방법이다. 전신 골 스캔, 심근 관류 스캔, 부갑상선 스캔, 간담 스캔, 폐 환기 및 관류 스캔, 갑상선 스캔 등 다양한 종류의 검사에 활용된다.2. 1. 2. 3차원 영상: SPECT, PET
SPECT(단일 광자 방출 컴퓨터 단층 촬영)는 감마 카메라의 데이터를 사용하여 CT와 유사한 3차원 단층 영상을 생성한다. 감마 카메라는 여러 각도에서 촬영한 다수의 2차원 영상을 통해 3차원 영상을 재구성한다.PET(양전자 방출 단층 촬영)는 양전자를 방출하는 방사성 핵종을 이용하여 생체 내에서 일어나는 기능적 과정을 영상화한다. PET는 포도당 대사, 혈류, 산소 소비와 같은 생리적 활동을 측정하는 데 사용될 수 있다.
2. 2. 하이브리드 스캔 기술
일부 의료기관에서는 핵의학 스캔 영상을 CT 또는 MRI과 같은 다른 영상기법의 영상과 합쳐 방사성 의약품이 집중된 신체 부위를 강조할 수 있도록 소프트웨어나 하이브리드 카메라를 사용한다. 이러한 방법은 종종 영상 융합 또는 공등록(co-registration)이라고 하며, SPECT/CT 및 PET/CT가 그 예시이다. 핵의학에서의 융합 영상 기법은 해부학적 구조와 기능에 대한 정보를 제공하며, 이는 그렇지 않으면 얻을 수 없거나 더 침습적인 절차나 수술이 필요할 수 있다.2. 3. 핵의학 영상의 실제적 고려사항
저선량 방사선 노출의 위험은 아직 잘 알려져 있지 않지만, 모든 인체 방사선 노출은 합리적으로 달성 가능한 최저 수준(ALARP)으로 유지되어야 한다는 신중한 접근 방식이 보편적으로 채택되었다. (원래는 "합리적으로 달성 가능한 최저 수준(ALARA)"으로 알려졌지만, 입법의 최신 초안에서는 "달성 가능한"보다 "합리적인" 부분에 더 중점을 두기 위해 변경되었다.)ALARP 원칙에 따라 핵의학 검사를 위해 환자에게 방사선을 조사하기 전에 검사의 이점을 확인해야 한다. 필요에 따라 해당 환자의 특정 상황을 고려해야 한다. 예를 들어, 환자가 진단을 얻기에 충분한 절차를 견딜 수 없을 가능성이 있다면, 방사성 추적자를 환자에게 주입하는 것은 부적절하다.
절차가 이점을 정당화하는 경우, 방사선 노출(환자에게 주어지는 방사선량)도 "ALARP"로 유지해야 한다. 즉, 핵의학에서 생성된 영상은 확신을 가지고 진단하는 데 필요한 것보다 더 좋아서는 안 된다. 더 많은 방사선을 조사하면 영상의 노이즈를 줄이고 사진적으로 더 매력적으로 만들 수 있지만, 이러한 수준의 세부 정보 없이도 임상적 질문에 답할 수 있다면 부적절하다.
결과적으로, 핵의학 영상의 방사선량은 연구 유형에 따라 크게 달라진다. 유효 방사선량은 일상적인 환경 연간 배경 방사선량보다 낮거나 비슷하거나 훨씬 초과할 수 있다. 마찬가지로, 복부/골반 CT 스캔의 방사선량보다 적거나, 비슷하거나, 더 높을 수도 있다.
일부 핵의학 절차는 가장 정확한 결과를 얻기 위해 연구 전에 특별한 환자 준비가 필요하다. 영상 촬영 전 준비에는 식이 요법 준비 또는 특정 약물의 금지가 포함될 수 있다. 환자는 스캔 전에 핵의학과에 문의하는 것이 좋다.
2. 4. 분석
핵의학 영상화 과정의 결과는 하나 이상의 영상으로 구성된 데이터 집합이다. 다중 영상 데이터 집합에서 영상 배열은 시간 순서(즉, 시네마 또는 동영상), 심장 게이트 시간 순서, 또는 감마 카메라가 환자에 대해 이동하는 공간 순서를 나타낼 수 있다. 단일광자방출컴퓨터단층촬영(SPECT)는 회전하는 감마 카메라에서 획득한 영상을 재구성하여 특정 위치에서 환자를 통과하는 "절편"의 영상을 생성하는 과정이다. 평행한 여러 절편의 집합은 환자 내 방사성핵종 분포의 3차원 표현인 절편 스택을 형성한다.핵의학 컴퓨터는 핵의학에서 사용 가능한 각 특정 영상 기술에 대한 정량적 분석 패키지를 제공한다. 시간 순서열은 동역학 모델(예: 다중 구획 모델 또는 Patlak plot)을 사용하여 추가적인 분석을 할 수 있다.
3. 중재적 핵의학
방사성핵종 치료는 갑상선 기능 항진증, 갑상선암, 피부암 및 혈액 질환 등을 치료하는 데 사용된다. 핵의학 치료에서는 방사선 치료량이 내부(예: 정맥 또는 경구 투여) 또는 치료할 부위 위에 직접 외부에서 화합물 형태로(예: 피부암의 경우) 투여된다.
핵의학 치료에 사용되는 방사성의약품은 단거리만 이동하는 이온화 방사선을 방출하여 원치 않는 부작용과 관련 없는 장기 또는 인접 구조물에 대한 손상을 최소화한다. 대부분의 핵의학 치료는 부작용이 거의 없고 일반 대중에 대한 방사선 노출을 안전한 수준으로 유지할 수 있기 때문에 외래 환자 절차로 수행될 수 있다.
| 물질 | 질환 |
|---|---|
| 아이오딘-131-요오드화나트륨 | 갑상선 기능 항진증 및 갑상선암 |
| 이트륨-90-이브리투모맙 티욱세탄 (제발린) 및 아이오딘-131-토시투모맙 (벡사르) | 불응성 림프종 |
| 131I-MIBG (메타아이오도벤질구아니딘) | 신경내분비종양 |
| 사마륨-153 또는 스트론튬-89 | 진통 골통 치료 |
| 레늄-188 | 피부의 편평세포암종 또는 기저세포암종 |
일부 센터에서는 핵의학과에서 종양 치료를 위해 이소토프의 이식 캡슐(근접치료)을 사용할 수도 있다.[5]
3. 1. 밀봉되지 않은 방사선원 치료
3. 2. 근접치료
4. 핵의학의 역사
핵의학의 역사는 물리학, 화학, 공학, 의학 등 다양한 분야의 과학자들의 기여로 이루어져 있다.[6] 의학사학자들은 핵의학의 다학문적인 성격 때문에 그 탄생 시기를 정확하게 특정하기 어렵다고 말한다. 하지만, 1934년 인공 방사능의 발견과 1946년 오크리지 국립 연구소의 의학적 용도를 위한 방사성핵종 생산 사이를 핵의학의 탄생 시기로 추정하고 있다.[6]
핵의학의 개념적인 기원은 1920년대 중반 독일 프라이부르크에서 조르주 드 외베시가 쥐에게 방사성핵종을 투여하여 대사 경로를 추적하고 추적자 원리를 확립한 실험으로 거슬러 올라간다.[7][8] 1936년, "핵의학의 아버지"로 불리는 존 H. 로렌스는 백혈병 치료에 인-32를 사용하여 인공 방사성핵종을 환자에게 처음으로 적용했다.[7][8]
많은 역사가들은 1934년 프레데리크 졸리오-퀴리와 이렌 졸리오-퀴리 부부가 인공적으로 생산된 방사성핵종을 발견한 것을 핵의학에서 가장 중요한 이정표로 간주한다.[6] 이들의 연구는 빌헬름 뢴트겐의 X선 발견, 앙리 베크렐의 방사성 우라늄 염 발견, 마리 퀴리의 방사성 토륨 및 폴로늄 발견과 "방사능" 용어 정립 등 초기 발견들을 기반으로 이루어졌다. 타케미 다로 또한 1930년대에 의학에 대한 핵물리학의 적용을 연구했다.
1946년 5월 11일, 솔 허츠 박사와 아서 로버츠 박사가 방사성 요오드를 이용한 그레이브스병 치료의 성공적인 사례를 발표하면서 핵의학은 전문 분야로서 대중의 인정을 받게 되었다.[9] 또한, 샘 세이드린[10]은 I-131을 사용하여 갑상선암 전이 환자를 성공적으로 치료하여 핵의학 발전에 기여했다.[11] I-131은 초기에는 갑상선암 치료에 사용되었지만, 이후 갑상선 기능 영상화, 정량화 및 갑상선 기능 항진증 치료로 그 사용 범위가 확대되었다. 테크네튬-99m은 1937년 C. 페리에와 E. 세그레에 의해 처음 발견되었으며, 1960년대에 발생기 시스템 개발을 통해 의학적 사용이 용이해졌다. 오늘날 테크네튬-99m은 핵의학에서 가장 많이 사용되는 원소이다.
1950년대 초, 방사성핵종, 방사능 탐지, 그리고 생화학적 과정을 추적하는 기술에 대한 지식이 확장되면서 핵의학의 광범위한 임상적 사용이 시작되었다. 베네딕트 캐슨의 직선 스캐너 개발과 할 오 앵거의 신틸레이션 카메라(앵거 카메라)에 대한 연구는 핵의학을 의학 영상 전문 분야로 확장시켰다.
1960년대 초, 스칸디나비아 남부에서는 닐스 A. 라센, 다비드 H. 잉그바르, 에릭 스킨호이가 크세논-133 흡입을 통해 뇌의 혈류 지도를 제공하는 기술을 개발했다.[12] 이후 동맥 내 주입 방식이 개발되어 신경정신의학 질환 환자의 국소적 뇌 활동 분포를 측정할 수 있게 되었다.[13] 이 기술은 말하기, 읽기, 시각 또는 청각적 인지, 자발적인 움직임 등으로부터 뇌 활동을 반영하는 이미지를 구성하는 데 사용되었다.[14]
1970년대에는 핵의학 절차를 통해 신체 대부분의 기관을 시각화할 수 있게 되었다. 1971년 미국 의학협회는 핵의학을 의학 전문 분야로 공식 인정했다.[17] 1972년 미국 핵의학위원회가, 1974년 미국 정골의학 핵의학위원회가 설립되면서 핵의학은 독립적인 의학 전문 분야로 자리매김했다.
1980년대에는 심장 질환 진단에 사용하기 위한 방사성 의약품이 개발되었다. 같은 시기에 단일 광자 방출 컴퓨터 단층 촬영(SPECT)의 개발은 심장의 3차원 재구성과 핵 심장학 분야의 확립으로 이어졌다.
최근 핵의학의 발전에는 PET 스캐너의 발명이 포함된다. 1950년대 후반 데이비드 E. 쿨과 로이 에드워즈에 의해 단일 광자 방출 컴퓨터 단층 촬영(SPECT)으로 발전한 방출 및 투과 단층 촬영의 개념이 소개되었다. 이들의 연구는 펜실베이니아 대학교에서 여러 단층 촬영 장비의 설계 및 제작으로 이어졌다. 단층 촬영 기술은 워싱턴 대학교 의과대학에서 더욱 발전되었다. 이러한 혁신은 캘리포니아 대학교 샌프란시스코 캠퍼스의 Bruce Hasegawa에 의한 SPECT 및 CT와의 융합 영상 및 1998년 피츠버그 대학교의 D. W. Townsend에 의한 최초의 PET/CT 프로토타입으로 이어졌다. PET/CT 영상은 종양학에서 진단, 병기 결정 및 치료 모니터링을 위한 필수적인 부분이 되었다. 2011년 초부터는 완전히 통합된 MRI/PET 스캐너가 시장에 출시되었다.
4. 1. 초기 역사
4. 2. 인공 방사성핵종의 발견
4. 3. 핵의학의 발전
4. 4. 핵의학의 확산
4. 5. 뇌 혈류 지도 개발
4. 6. 핵의학의 공식 인정
4. 7. SPECT와 PET의 발전
4. 8. 융합 영상 기술의 발전
5. 방사성핵종의 출처
핵의학에 사용되는 방사성핵종은 주로 원자로나 사이클로트론에서 생산된다.[18] 99mTc는 몰리브덴-99을 포함하는 방사성핵종 발생기를 통해 병원에 공급되며, 99Mo는 원자로에서 235U의 핵분열 생성물로 얻어진다.[18] 전 세계 의료 동위원소 공급량의 상당 부분은 네덜란드의 페텐 원자로와 캐나다 챌크리버의 챌크리버 연구소에서 생산되었으나, 챌크리버 연구소는 2018년 영구 폐쇄되었다.[18]18F와 같은 일부 방사성 동위원소는 사이클로트론에서 생산된다.[18] 사이클로트론은 양성자를 가속하여 18O에 충돌시키는 방식으로 18F를 생산하며, 이는 FDG 생성에 사용된다.
핵의학 검사에는 방사성핵종을 체내에 투여하는 과정이 포함되며, 정맥 주사, 섭취, 흡입 등 다양한 방식으로 투여된다. 진단용 방사성핵종은 주로 감마선을 방출하며, 치료용으로는 베타 입자가 사용된다.
| 동위원소 | 원자번호 | 반감기 | 붕괴 방식 | 감마선 에너지 (keV) | 최대 베타 에너지 (keV) / 풍부도[22] | |
|---|---|---|---|---|---|---|
| 명칭 | 기호 | |||||
| 영상 | ||||||
| 플루오린-18 | 18F | 9 | 109.77 m | β+ | 511 (193%) | 634 (97%) |
| 갈륨-67 | 67Ga | 31 | 3.26 d | 전자포획 | 93 (39%), 185 (21%), 300 (17%) | - |
| 크립톤-81m | 81mKr | 36 | 13.1 s | 이성질체 전이 | 190 (68%) | - |
| 루비듐-82 | 82Rb | 37 | 1.27 m | β+ | 511 (191%) | 3381 (81.8%) 2605 (13.1%) 1906 (0.14%) 1209 (0.32%) |
| 질소-13 | 13N | 7 | 9.97 m | β+ | 511 (200%) | 1198 (99.8%) |
| 테크네튬-99m | 99mTc | 43 | 6.01 h | 이성질체 전이 | 140 (89%) | - |
| 인듐-111 | 111In | 49 | 2.80 d | 전자포획 | 171 (90%), 245 (94%) | - |
| 아이오딘-123 | 123I | 53 | 13.3 h | 전자포획 | 159 (83%) | - |
| 크세논-133 | 133Xe | 54 | 5.24 d | β− | 81 (31%) | 346 (99.1%) 267 (0.9%) |
| 탈륨-201 | 201Tl | 81 | 3.04 d | 전자포획 | 69–83* (94%), 167 (10%) | - |
| 치료 | ||||||
| 이트륨-90 | 90Y | 39 | 2.67 d | β− | - | 2279 (99.98%) |
| 아이오딘-131 | 131I | 53 | 8.02 d | β− | 364 (81%) | 807 (0.4%) 606 (89.4%) 334 (7.2%) 248 (2.1%) |
| 루테튬-177 | 177Lu | 71 | 6.65 d | β− | 113 (6.6%) 208 (11%) | 498 (79.3%) 385 (9.1%) 177 (11.6%) |
| style="text-align:left;" colspan="7"| | ||||||
5. 1. 테크네튬-99m 생산
5. 2. 플루오린-18 생산
5. 3. 기타 방사성 동위원소
6. 정책 및 절차
6. 1. 방사선량
핵의학 절차를 받는 환자는 방사선량을 받게 된다. 현재 국제 지침에 따르면 아무리 적은 양의 방사선량이라도 위험이 있다고 가정한다.[24] 핵의학 검사에서 환자에게 조사되는 방사선량은 증명되지는 않았지만, 일반적으로 암을 유발할 위험이 매우 낮다고 받아들여진다. 이 점에서 X선 검사의 위험과 유사하지만, X선 기계와 같은 외부 공급원이 아닌 체내에서 방사선량이 전달된다는 점과, 방사선량이 X선보다 일반적으로 훨씬 높다는 점이 다르다.핵의학 검사로 인한 방사선량은 시버트(Sv) 단위의 유효선량으로 표현되며(일반적으로 밀리시버트(mSv)로 표시됨) 표시된다.[24] 검사로 인한 유효선량은 메가베크렐(MBq) 단위로 투여되는 방사능의 양, 사용되는 방사성의약품의 물리적 특성(반감기), 신체 내 분포 및 신체에서의 제거 속도에 영향을 받는다. 유효선량은 사구체 여과율 측정을 위한 3 MBq 크롬-51 EDTA 측정의 경우 6 μSv(0.006 mSv)에서부터 80 MBq 탈륨-201 심근 영상 검사의 경우 11.2 mSv(11,200 μSv)까지 다양하다. 테크네튬-99m MDP 600 MBq를 사용하는 일반적인 골 스캔의 유효선량은 약 2.9 mSv(2,900 μSv)이다.[24]
이전에는 다음과 같은 측정 단위를 사용했다.
- 퀴리(Ci): 3.7 × 1010 Bq와 같으며, 1.0그램의 라듐(Ra-226)과도 같다.
- 래드(rad)(흡수선량): 현재는 그레이(Gy)로 대체되었다.
- 렘(rem)(Röntgen equivalent man): 현재는 시버트(Sv)로 대체되었다.[25]
래드와 렘은 거의 모든 핵의학 절차에서 본질적으로 동일하며, 훨씬 높은 상대생물학적 효과(RBE) 때문에 알파 방사선만이 더 높은 렘 또는 Sv 값을 생성한다. 알파 방출체는 오늘날 핵의학에서 거의 사용되지 않지만, 원자로와 가속기로 생성된 방사성핵종이 등장하기 전에는 광범위하게 사용되었다. 인체에 대한 방사선 노출과 관련된 개념은 방사선 방호 분야에서 다루며, 안전하고 효과적인 핵의학 기술의 개발과 실천은 의료 물리학의 주요 초점이다.
6. 2. 규제 체계 및 지침
여러 국가와 국제기구는 핵의학 관련 규제 체계를 유지하고 있다. 국제원자력기구(International Atomic Energy Agency, IAEA)와 같은 국제 기구는 핵의학 분야의 모범 사례에 대한 다양한 논문과 지침을 정기적으로 발표하고 핵의학의 신기술에 대한 보고서도 발표하고 있다.[28][29] 국제방사선방호위원회(International Commission on Radiological Protection)와 같은 단체는 밀봉되지 않은 방사성핵종을 가진 환자의 병원 퇴원 관리 방법에 대한 정보를 발표했다.[30]예를 들어 미국에서는 미국 원자력 규제 위원회(Nuclear Regulatory Commission, NRC)와 미국 식품의약국(Food and Drug Administration, FDA)이 병원이 따라야 할 지침을 마련하고 있다.[26] NRC의 경우, X선과 같이 방사성 물질이 관련되지 않은 경우에는 해당 기관에서 규제하지 않고 각 주에서 규제한다.[27]
참조
[1]
웹사이트
Nuclear Radiology
https://www.texaschi[...]
[2]
웹사이트
What is nucleology?
https://www.answers.[...]
[3]
웹사이트
Nuclear Medicine
https://web.archive.[...]
2015-08-20
[4]
웹사이트
scintigraphy
http://medical-dicti[...]
Saunders; Saunders; The McGraw-Hill Companies
[5]
웹사이트
Nuclear Wallet Cards
http://www.nndc.bnl.[...]
2015-08-20
[6]
논문
Tumor-localizing radionuclides in retrospect and prospect
[7]
웹사이트
Donner Laboratory: The Birthplace of Nuclear Medicine
http://jnm.snmjourna[...]
[8]
웹사이트
Important Moments in the History of Nuclear Medicine
https://web.archive.[...]
2012-01-03
[9]
논문
Radioactive iodine in the study of thyroid physiology; the use of radioactive iodine therapy in hyperthyroidism
1946-05-00
[10]
논문
Radioactive iodine therapy; effect on functioning metastases of adenocarcinoma of the thyroid
1946-12-00
[11]
서적
Nuclear Medicine
Mosby
1996
[12]
논문
Quantitative determination of regional cerebral blood-flow in man
[13]
논문
Distribution of cerebral activity in chronic schizophrenia
http://www.thelancet[...]
1974-12-00
[14]
논문
Brain Function and Blood Flow
1978-10-00
[15]
논문
Supplementary motor area and other cortical areas in organization of voluntary movements in man
1980-01-00
[16]
논문
Localization of cortical areas activated by thinking
http://jn.physiology[...]
[17]
웹사이트
What is nuclear medicine
https://web.archive.[...]
2009-01-17
[18]
뉴스
Canada permanently closes NRU research reactor
https://www.neimagaz[...]
2018-04-06
[19]
서적
MIRD: Radionuclide Data and Decay Schemes
Society for Nuclear Medicine
[20]
웹사이트
Table of Radioactive Isotopes
https://web.archive.[...]
[21]
논문
Production of (177)Lu for Targeted Radionuclide Therapy: Available Options
2015-06-00
[22]
웹사이트
Données atomiques et nucléaires
http://www.lnhb.fr/d[...]
2022-10-24
[23]
웹사이트
Technegas
https://web.archive.[...]
[24]
웹사이트
ARSAC notes for guidance
https://www.gov.uk/g[...]
Public Health England
2021-02-19
[25]
뉴스
Explained: rad, rem, sieverts, becquerels
https://news.mit.edu[...]
2021-04-25
[26]
서적
An Overview of the Regulations of Radiopharmaceuticals
https://doi.org/10.1[...]
Springer International Publishing
2021-04-25
[27]
웹사이트
Nuclear Medicine: What It Is – and Isn't
https://www.nrc.gov/[...]
2021-04-25
[28]
웹사이트
IAEA Safety Standards and medical exposure
https://www.iaea.org[...]
2021-04-25
[29]
웹사이트
Human Health Campus – Nuclear Medicine
https://humanhealth.[...]
2021-04-25
[30]
논문
Release of patients after therapy with unsealed radionuclides
2004-06-00
관련 사건 타임라인
( 최근 20개의 뉴스만 표기 됩니다. )
본 사이트는 AI가 위키백과와 뉴스 기사,정부 간행물,학술 논문등을 바탕으로 정보를 가공하여 제공하는 백과사전형 서비스입니다.
모든 문서는 AI에 의해 자동 생성되며, CC BY-SA 4.0 라이선스에 따라 이용할 수 있습니다.
하지만, 위키백과나 뉴스 기사 자체에 오류, 부정확한 정보, 또는 가짜 뉴스가 포함될 수 있으며, AI는 이러한 내용을 완벽하게 걸러내지 못할 수 있습니다.
따라서 제공되는 정보에 일부 오류나 편향이 있을 수 있으므로, 중요한 정보는 반드시 다른 출처를 통해 교차 검증하시기 바랍니다.
문의하기 : help@durumis.com