아나톡신-a
"오늘의AI위키"의 AI를 통해 더욱 풍부하고 폭넓은 지식 경험을 누리세요.
1. 개요
아나톡신-a는 시아노박테리아에 의해 생성되는 강력한 신경독으로, 근육형 니코틴성 아세틸콜린 수용체의 작용제이다. 1960년대 초 캐나다에서 소 떼의 죽음으로 처음 발견되었으며, 동물과 사람에게 독성을 나타낸다. 아나톡신-a는 섭취 시 호흡 마비와 사망을 유발하며, 물과 토양, 수생 식물 등 다양한 환경에서 발견된다. 자외선에 의해 분해되며, 생물학적 및 화학적 처리를 통해 제거할 수 있다. 의학 연구에서 아세틸콜린 관련 질환 치료를 위한 약리학적 탐침으로 사용되며, 다양한 합성 방법이 연구되고 있다.
더 읽어볼만한 페이지
- 고리가 2개인 헤테로고리 화합물 - 렘데시비르
렘데시비르는 길리어드 사이언스에서 개발한 항바이러스제로, 에볼라 바이러스 치료제로 개발되었으나 코로나19 치료제로 주목받았으며, 임상 시험에서 일부 긍정적 결과가 있었지만 상반된 결과도 존재하고, 여러 국가에서 코로나19 치료를 위해 승인되었으며, 체내에서 활성 대사체로 전환되어 작용하고, 활성체는 고양이 코로나바이러스 감염 치료에도 효과가 있다. - 고리가 2개인 헤테로고리 화합물 - 아마톡신
아마톡신은 8개의 아미노산 고리가 2개의 큰 고리에 연결된 구조를 가진 화합물로, RNA 중합효소 II를 억제하여 세포 용해를 일으키며, 광대버섯속 등의 버섯에서 발견되어 섭취 시 간, 신장 등 장기에 손상을 주고 심할 경우 사망에 이를 수 있다. - 사이클로알켄 - 시클로헥센
시클로헥센은 벤젠 부분 수소화 반응으로 주로 생산되거나 실험실에서 시클로헥산올 탈수 반응으로 얻을 수 있는, 다양한 화학 물질 전구체이자 용매, 도시 가스 부취제로 쓰이는 고리형 불포화 탄화수소이다. - 사이클로알켄 - 엔드린
엔드린은 1950년 J. 하이먼 & 컴퍼니에서 개발한 살충제로 농업용, 살서제, 조류 구충제 등으로 널리 쓰였으나 독성이 강해 현재는 대부분 국가에서 사용이 금지되었고 대한민국을 포함한 많은 국가에서 규제되며 잔류성 유기 오염 물질로 지정되었다. - 니코틴 작용제 - 담배
담배는 마야, 아즈텍인들이 종교 의식에 사용하던 잎담배에서 유래하여 유럽에 전파된 후 기호식품으로 유행하고 궐련 기술과 세계 대전을 거치며 확산되었지만, 유해 성분과 니코틴 중독성으로 인해 건강과 사회적 문제를 야기하여 전 세계적으로 금연 정책과 치료가 시행되고 있는 궐련, 전자담배 등의 다양한 형태를 가진 식물이다. - 니코틴 작용제 - 아세틸콜린
아세틸콜린은 말초신경계와 중추신경계에서 신경전달물질로 작용하는 유기 분자로, 콜린 아세틸전이효소에 의해 합성되고 아세틸콜린에스터레이스에 의해 분해되며, 1936년 노벨 생리학·의학상을 수상한 헨리 핼릿 데일과 오토 뢰비에 의해 발견 및 확인되었다.
2. 역사
아나톡신-a는 1960년대 초 캐나다 온타리오 주의 서스캐처원 호수에서 독성 조류 번식이 일어난 물을 마신 여러 소 떼가 죽은 사건을 계기로 P.R. 고럼이 처음 발견했다.[1] 1972년 J.P. 데블린은 남세균 ''아나베나 플로스-아퀘''에서 아나톡신-a를 분리했다.[1]
2. 1. 발견
아나톡신-a는 1960년대 초 캐나다 온타리오 주의 서스캐처원 호수에서 독성 조류 번식이 일어난 물을 마신 여러 소 떼가 죽은 사건을 계기로 P.R. 고럼이 처음 발견했다.[1] 1972년 J.P. 데블린은 남세균 ''아나베나 플로스-아퀘''에서 아나톡신-a를 분리했다.[1]2. 2. 초기 연구
아나톡신-a는 1960년대 초, 캐나다 온타리오 주의 서스캐처원 호수에서 독성 조류 번식을 포함한 물을 마시고 여러 소 떼가 죽은 후 P.R. 고럼에 의해 처음 발견되었다. 1972년 J.P. 데블린은 남세균 ''아나베나 플로스-아퀘''에서 이를 분리했다.[8]1977년, 카마이클(Carmichael), 고럼(Gorham), 빅스(Biggs)는 아나톡신-a에 대한 실험을 진행했다. 그들은 독성 배양액인 ''A. flos-aquae''를 두 마리의 어린 수송아지 위장에 투여했는데, 몇 분 안에 근육 연축과 협동 운동 능력 상실이 발생했으며, 호흡 부전으로 인한 사망은 수 분에서 수 시간 사이에 일어났다. 또한, 그들은 장기간의 인공 호흡으로는 해독이 이루어지지 않고, 자연적인 신경근 기능이 회복되지 않는다는 것을 확인했다. 이 실험을 통해, 그들은 송아지에 대한 경구 최소 치사량(MLD) (아나톡신 분자가 아닌 조류)을 대략 체중 1kg당 420mg으로 계산했다.[8]
같은 해, 데블린(Devlin)과 동료들은 아나톡신-a의 이환식 2급 아민 구조를 발견했다. 그들은 또한 쥐를 대상으로 카마이클 등의 실험과 유사한 실험을 수행했다. 그 결과 아나톡신-a는 복강 내 주사 후 2~5분 이내에 경련, 근육 경련, 마비, 호흡 정지를 일으켜 쥐를 사망에 이르게 한다는 것을 발견했으며, 이에 따라 매우 빠른 사망 인자라는 이름이 붙여졌다.[9] 그들은 쥐에 대한 LD50을 체중 1kg당 250μg으로 결정했다.[1]
1980년 스피박(Spivak) 등이 개구리를 대상으로 한 전기 생리학적 실험에서 아나톡신-a가 근육형(α1)2βγδ nAChR의 강력한 효능제임이 밝혀졌다. 아나톡신-a는 탈분극 신경근 차단, 개구리 복직근의 수축, 개구리 넙다리 근육의 탈분극, 둔감화, 그리고 활동 전위의 변화를 유발했다. 이후, 토마스(Thomas) 등은 1993년 쥐 M 10 세포에서 발현된 닭 α4β2 nAChR 서브유닛과 ''Xenopus laevis'' 난모세포에서 발현된 닭 α7 nAChR을 이용한 연구를 통해 아나톡신-a가 신경 nAChR의 강력한 효능제이기도 하다는 것을 보였다.[1]
3. 생성 및 분포
아나톡신-a는 전 세계 담수에서 발견되는 여러 속의 시아노박테리아에 의해 생성되는 신경독이다.[43] 일부 담수 시아노박테리아는 염분에 대한 내성을 가지고 있어, 기수 등 염분이 있는 환경에서도 발견될 수 있다.[3]
아나톡신-a를 생성하는 시아노박테리아는 토양 및 수생 식물에서도 발견된다. 아나톡신-a는 점토질의 유기물이 풍부한 토양의 음전하 부위에 잘 흡착되며, 모래 토양에는 약하게 흡착된다. 네브래스카의 한 연구에 따르면, 12개 저수지에서 채취한 수생 식물의 38%에서 결합된 아나톡신-a와 자유 아나톡신-a가 모두 발견되었으며, 자유 아나톡신-a보다 결합된 형태의 발생 빈도가 훨씬 높았다.[7]
3. 1. 생성 시아노박테리아
아나바에나(돌리코스페르뭄)[42], 아파니조메논[30], 실린드로스페르몹시스[43], 실린드로스페르뭄, 링비아[44], 마이크로시스티스[45], 노스톡[43], 오실라토리아[44], 포르미디움(Microcoleus)[44], 플랑크토트릭스[44], 라피디오옵시스[44], 티코네마[46], 워로니키니아[44] 등 다양한 속의 시아노박테리아가 아나톡신-a를 생성한다.3. 2. 분포 환경
아나톡신-a는 전 세계의 담수에서 발견되는 여러 속의 시아노박테리아에 의해 생성되는 신경독이다.[43] 일부 담수 시아노박테리아는 염분에 대한 내성을 가지고 있는 것으로 알려져 있어, 아나톡신-a가 기수 또는 기타 염분이 있는 환경에서도 발견될 수 있다.[3] 아나톡신-a를 포함한 다양한 시아노독소를 생성하는 시아노박테리아의 대량 번식은 기온 상승, 수층 분리 및 영양염류 유출에 의한 부영양화로 인해 빈도가 증가하고 있다.[4] 이러한 광범위한 시아노박테리아 유해 조류 번식 (cyanoHABs)은 주변 수역의 시아노독소 양을 증가시켜 수생 생물과 육상 생물의 건강을 위협한다.[5]아나톡신-a를 생성하는 일부 시아노박테리아 종은 표층 수에서 번식하지 않고 대신 저서 매트를 형성한다. 해안가로 밀려온 분리된 저서 시아노박테리아 매트를 섭취하여 아나톡신-a와 관련된 동물의 사망 사례가 많이 발생했다.[6] 아나톡신-a를 생성하는 시아노박테리아는 토양 및 수생 식물에서도 발견되었다. 아나톡신-a는 점토질의 유기물이 풍부한 토양의 음전하 부위에 잘 흡착되며, 모래 토양에는 약하게 흡착된다. 한 연구에 따르면, 네브래스카의 12개 저수지에서 채취한 수생 식물의 38%에서 결합된 아나톡신-a와 자유 아나톡신-a가 모두 발견되었으며, 자유 아나톡신-a보다 결합된 아나톡신-a의 발생 빈도가 훨씬 높았다.[7]
4. 독성
아나톡신-a는 신경근 접합부와 중추신경계에 존재하는 니코틴성 아세틸콜린 수용체(nAChR)의 강력한 작용제이다.[1] 1977년 카마이클(Carmichael) 등은 독성 배양액 ''A. flos-aquae''를 두 마리의 어린 수송아지에게 투여하는 실험을 통해 근육 연축, 협동 운동 능력 상실, 호흡 부전으로 인한 사망을 확인했다. 인공 호흡으로는 해독이 되지 않았고, 자연적인 신경근 기능도 회복되지 않았다. 송아지의 경구 최소 치사량(MLD)은 체중 1kg당 약 420mg(아나톡신 분자가 아닌 조류)이었다.[8]
같은 해 데블린(Devlin) 등은 쥐를 대상으로 한 실험에서 아나톡신-a가 복강 내 주사 후 2~5분 안에 경련, 근육 경련, 마비, 호흡 정지를 일으켜 사망에 이르게 한다는 것을 발견하고, '매우 빠른 사망 인자'라는 이름을 붙였다.[9] 쥐의 LD50은 체중 1kg당 250μg이었다.[1]
1980년 스피박(Spivak) 등은 개구리를 이용한 전기 생리학적 실험에서 아나톡신-a가 근육형(α1)2βγδ nAChR의 강력한 효능제임을 밝혔다. 1993년 토마스(Thomas) 등은 쥐와 ''Xenopus laevis'' 난모세포를 이용한 연구를 통해 아나톡신-a가 신경 nAChR의 강력한 효능제이기도 하다는 것을 보였다.[1]
4. 1. 작용 기전
아나톡신-a는 중추신경계(CNS)에 존재하는 신경 α4β2 및 α4 니코틴성 아세틸콜린 수용체(nAChR)와 신경근 접합부에 존재하는 (α1)2βγδ 근육형 nAchR의 작용제이다.[1] 근육형 수용체에 대해 아세틸콜린보다 약 20배 더 높은 친화력을 보인다.[2] 그러나 무스카린성 아세틸콜린 수용체에 미치는 영향은 미미하며, nAchR에 비해 100배 낮은 선택성을 보인다.[19] 신경근 접합부보다 중추신경계에서 훨씬 낮은 효능을 보이는데, 해마 및 뇌간 뉴런에서는 PNS에서 요구되는 것보다 5~10배 더 높은 농도의 아나톡신-a가 nAchR을 활성화하는 데 필요하다.[19]정상적인 상황에서 아세틸콜린은 시냅스 후 뉴런 막의 nAchR에 결합하여 수용체의 세포 외 도메인에 형태적 변화를 일으키고, 채널 기공을 열어 Na+ 및 Ca2+ 이온이 뉴런으로 이동하게 한다. 이로 인해 세포 탈분극이 일어나고 활동 전위가 생성되어 근육 수축이 가능해진다. 이후 아세틸콜린은 nAchR에서 해리되고, 아세틸콜린에스터라제에 의해 아세테이트와 콜린으로 빠르게 분해된다.[20]
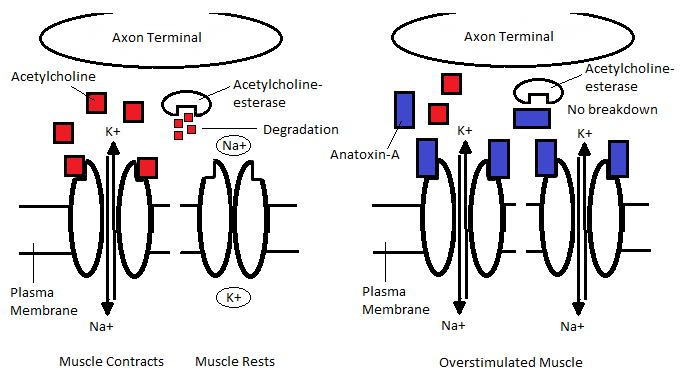
아나톡신-a가 nAchR에 결합하면 뉴런에 동일한 효과가 발생한다. 그러나 아나톡신-a의 결합은 비가역적이며, 아나톡신-a nAchR 복합체는 아세틸콜린에스터라제에 의해 분해될 수 없다. 따라서 nAchR은 일시적으로 열린 상태로 고정되어 지속적인 활동 전위 생성으로 인한 과도한 자극을 유발한다.[19]
아나톡신-a의 두 가지 입체 이성질체 중, 양성 거울상 이성질체인 (+)-아나톡신-a는 합성된 음성 거울상 이성질체인 (−)-아나톡신-a보다 150배 더 강력하다.[19] 이는 s-''시스'' 엔온 형태의 (+)-아나톡신-a가 질소와 카르보닐 그룹 사이의 거리가 6.0 Å으로, 아세틸콜린의 질소와 산소를 분리하는 5.9 Å 거리와 잘 일치하기 때문이다.[1]
호흡 정지로 인한 뇌 산소 공급 부족은 아나톡신-a의 가장 명백하고 치명적인 영향이다.[19] 쥐, 새, 개, 송아지에게 아나톡신-a의 치사량을 주사하면 사망 전에 근육 섬유다발 연축, 움직임 감소, 붕괴, 과장된 복부 호흡, 청색증, 경련이 나타난다.[2] 쥐에서 아나톡신-a는 혈압과 심박수에 심각한 영향을 미치고 심각한 산증을 유발한다.[1]
1977년, 카마이클(Carmichael), 고럼(Gorham), 빅스(Biggs)는 아나톡신-a 실험을 통해 독성 배양액 ''A. flos-aquae''를 투여받은 두 마리 어린 수송아지에게서 근육 연축, 협동 운동 능력 상실, 호흡 부전으로 인한 사망이 발생함을 확인했다. 인공 호흡으로는 해독이 이루어지지 않고, 자연적인 신경근 기능이 회복되지 않는다는 것도 확인했다. 송아지에 대한 경구 최소 치사량(MLD)은 대략 체중 1kg당 420mg(아나톡신 분자가 아닌 조류)으로 계산되었다.[8]
같은 해, 데블린(Devlin)과 동료들은 쥐 대상 실험에서 아나톡신-a가 복강 내 주사 후 2~5분 이내에 경련, 근육 경련, 마비, 호흡 정지를 일으켜 사망에 이르게 한다는 것을 발견하고, '매우 빠른 사망 인자'라는 이름을 붙였다.[9] 쥐에 대한 LD50은 체중 1kg당 250μg으로 결정되었다.[1]
1980년 스피박(Spivak) 등은 개구리 대상 전기 생리학적 실험에서 아나톡신-a가 근육형(α1)2βγδ nAChR의 강력한 효능제임을 밝혔다. 아나톡신-a는 탈분극 신경근 차단, 개구리 복직근의 수축, 개구리 넙다리 근육의 탈분극, 둔감화, 활동 전위 변화를 유발했다. 이후, 토마스(Thomas) 등(1993)은 쥐 M 10 세포에서 발현된 닭 α4β2 nAChR 서브유닛과 ''Xenopus laevis'' 난모세포에서 발현된 닭 α7 nAChR을 이용한 연구를 통해 아나톡신-a가 신경 nAChR의 강력한 효능제이기도 하다는 것을 보였다.[1]
4. 2. 중독 증상
아나톡신-a 중독의 대표적인 증상은 근육 다발 수축, 떨림, 비틀거림, 숨 가쁨, 호흡 마비이며, 수분 내에 사망에 이를 수 있다.[10]1977년, 카마이클(Carmichael) 등은 독성 배양액을 두 마리의 어린 수송아지 위장에 투여하는 실험을 진행했다. 그 결과, 몇 분 안에 근육 연축과 협동 운동 능력 상실이 발생했으며, 수 분에서 수 시간 사이에 호흡 부전으로 사망했다. 인공 호흡으로는 해독이 이루어지지 않았고, 자연적인 신경근 기능 회복도 되지 않았다. 송아지에 대한 경구 최소 치사량(MLD)은 대략 체중 1kg당 420mg으로 계산되었다.[8]
같은 해, 데블린(Devlin) 등은 쥐를 대상으로 비슷한 실험을 수행했다. 아나톡신-a는 복강 내 주사 후 2~5분 안에 경련, 근육 경련, 마비, 호흡 정지를 일으켜 쥐를 사망에 이르게 했다. 쥐에 대한 LD50은 체중 1kg당 250μg으로 결정되었다.[1]
사람의 경우, 아나톡신-a를 생성할 수 있는 시아노박테리아가 포함된 시냇물과 호수의 물을 섭취했을 때 치명적이지 않은 중독 사례가 있었다. 주로 메스꺼움, 구토, 설사 및 복통과 같은 위장 관련 증상이 나타났다.[11] 시아노박테리아에 오염된 연못에 뛰어든 10대의 사례처럼, 심각한 경우에는 호흡 곤란, 마비 등으로 사망에 이를 수 있다.[12]
아나톡신-a는 뇌에 산소 공급 부족을 초래하는 호흡 정지를 일으켜 가장 치명적인 영향을 준다.[19] 쥐, 새, 개, 송아지에게 아나톡신-a의 치사량을 주사한 결과, 사망 전에 근육 섬유다발 연축, 움직임 감소, 붕괴, 과장된 복부 호흡, 청색증, 경련이 나타났다.[2] 쥐의 경우, 혈압과 심박수에 심각한 영향을 미치고 산증을 유발했다.[1]
아나톡신-a는 중추신경계와 신경근 접합부에 존재하는 니코틴성 아세틸콜린 수용체의 작용제이다.[1] 아세틸콜린보다 약 20배 더 높은 친화력을 가진다.[2] 아나톡신-a가 수용체에 결합하면, 아세틸콜린에스터라제에 의해 분해될 수 없어 과도한 자극을 유발한다.[19]
아나톡신-a로 인한 야생동물과 가축의 사망 사례도 여러 건 보고되었다. 개, 소 등의 사망 사례가 미국, 캐나다, 핀란드, 뉴질랜드, 프랑스, 스코틀랜드, 아일랜드, 독일 등 여러 국가에서 보고되었다.[2][21][22][23][24][25] 케냐 보고리아 호수의 작은홍학 사례는 특히 주목할 만한데, 1999년 하반기에 약 3만 마리의 홍학이 시아노톡신으로 인해 죽었으며, 매년 대량 사망을 초래하고 있다.[26]

4. 3. 노출 경로
아나톡신-a에 노출되는 주요 경로는 다음과 같다.- 섭취: 아나톡신-a에 오염된 식수나 레크리에이션용 물(강, 호수 등)을 마시면 중독될 수 있다. 동물 실험에서 아나톡신-a는 위장관을 통해 빠르게 흡수되는 것으로 밝혀졌다.[13] 호수나 강에서 아나톡신-a에 오염된 물을 마시고 동물이 사망한 사례가 수십 건 기록되었으며, 사람의 사망 원인으로 의심되는 사례도 있다.[14] 섭취 시 나노몰(nM) 농도의 아나톡신-a가 아세틸콜린 수용체에 결합하여 독성 효과를 유발할 수 있다는 연구 결과도 있다.[15]
- 사람의 경우, 아나톡신-a를 생성하는 시아노박테리아가 포함된 시냇물이나 호수의 물을 마시고 중독된 사례가 있었다. 주된 증상은 메스꺼움, 구토, 설사, 복통 등 위장 관련 문제였다.[11] 시아노박테리아에 오염된 연못에 뛰어든 10대가 사망한 사례도 보고되었다.[12]
- 피부 접촉: 조류 번식으로 오염된 강, 개울, 호수 물에 노출되면 피부 자극이나 발진이 생길 수 있다.[16] 아나톡신-a가 사람 각질 세포에 미치는 영향을 연구한 결과, 낮은 농도(0.1μg/mL, 1μg/mL)에서는 영향이 없었지만, 장기간(48시간) 노출 시 10μg/mL 농도에서 약한 독성 효과가 나타났다.[17]
- 흡입: 아나톡신-a의 흡입 독성에 대한 자료는 아직 없지만, 다른 남세균 신경독소인 삭시톡신이 포함된 물보라를 흡입한 수상 스키 선수가 심각한 호흡 곤란을 겪은 사례가 있다.[18] 따라서 아나톡신-a가 포함된 물보라를 흡입하는 것도 유사한 결과를 초래할 수 있다.
실험용 쥐에게 복강 내 주사로 아나톡신-a를 투여했을 때, 근육 다발 수축, 떨림, 비틀거림, 숨 가쁨, 호흡 마비 등의 급성 중독 증상이 나타났으며, 수분 내에 사망했다.[10] 아나톡신-a에 오염된 물에 노출된 제브라피시는 심박수가 변동했다.[10]
5. 안정성 및 분해
아나톡신-a는 물 속이나 다른 자연 조건에서 불안정하며, 자외선 조건에서 광분해되어 독성이 없는 디하이드로아나톡신-a와 에폭시아나톡신-a로 분해된다. 아나톡신-a의 광분해는 pH와 빛의 강도에 의존하지만, 산소 농도와는 무관하다. 따라서 빛에 의한 분해가 광산화에 의한 것은 아님이 밝혀졌다.[48]
일부 미생물은 아나톡신-a를 분해할 수 있다는 연구 결과가 있다. 1991년 Kiviranta 등의 연구에 따르면, 세균의 일종인 ''Pseudomonas''는 하루에 2μg/ml~10μg/ml의 속도로 아나톡신-a를 분해할 수 있었다.[28] Rapala 등(1994)의 실험에서도 유사한 결과가 나왔다. 22일 동안 멸균된 퇴적물과 멸균되지 않은 퇴적물이 아나톡신-a 분해에 미치는 영향을 비교한 결과, 멸균된 퇴적물이 있는 시험관에서는 아나톡신-a의 농도가 실험 초기와 비슷했지만, 멸균되지 않은 퇴적물이 있는 시험관에서는 25~48% 감소했다.[19]
6. 검출 방법
아나톡신-a 검출 방법에는 크게 두 가지 범주가 있다. 생물학적 방법은 시료를 생쥐 및 브라인 슈림프(`Artemia salina`), 담수 갑각류 `Thamnocephalus platyurus` 유충, 다양한 곤충 유충과 같이 생태독성 검사에 더 일반적으로 사용되는 다른 유기체에 투여하는 것이다. 이러한 방법의 문제점은 그 결과로 나타나는 사망이 아나톡신-a 때문인지 다른 신경독 때문인지를 판단할 수 없다는 것이다. 또한 이러한 검사에는 많은 양의 시료가 필요하다. 생물학적 방법 외에도 과학자들은 아나톡신-a 검출을 위해 크로마토그래피를 사용해 왔다. 이는 독소의 빠른 분해와 아나톡신-a에 대한 상업적으로 이용 가능한 표준 물질의 부족으로 인해 복잡하다.[19]
7. 공중 보건
아나톡신-a는 다른 시아노톡신에 비해 발생 빈도는 낮지만, 독성이 매우 강하여 육상 및 수생 생물, 특히 가축과 인간에게 심각한 위협이 된다. 사람에 대한 치사량은 알려져 있지 않으나, 성인 남성의 경우 5mg 미만으로 추정된다.[29] 아나톡신-a는 적어도 한 사람의 사망에 연루된 것으로 의심된다.[14] 비료 유출로 인한 호수와 강의 부영양화, 그리고 지구 온난화로 인해 시아노박테리아 번성이 더 자주, 더 널리 발생함에 따라 아나톡신-a와 다른 시아노톡신이 제기하는 위협은 증가하고 있다.[19]
7. 1. 국제적 규제 현황
세계 보건 기구와 미국 환경 보호국(EPA)은 1999년과 2006년에 아나톡신-a에 대한 공식적인 허용 일일 섭취량(TDI) 수준을 설정하기에 충분한 독성 데이터가 부족하다는 결론을 내렸지만, 일부 지역에서는 자체적으로 기준치를 시행하고 있다.[30][31]캐나다 퀘벡주는 아나톡신-a에 대한 식수 최대 허용 기준치를 3.7μg/L로 정하고 있다.[35] 뉴질랜드는 아나톡신-a에 대한 식수 최대 허용 기준을 6μg/L로 설정하고 있다.[36]
7. 2. 수처리
과학자들은 복잡한 기술이 필요 없고 유지보수 및 운영 비용이 낮은 생물학적 처리 방법을 선호한다. 아나톡신-a에 대해 특별히 테스트된 생물학적 처리 옵션은 거의 없지만, 2–10 μg ml−1 d−1의 속도로 아나톡신-a를 생분해할 수 있는 ''Pseudomonas'' 종이 확인되었다. 생물학적 (입상) 활성탄 (BAC) 또한 생분해 방법으로 테스트되었지만, 생분해가 일어났는지 아니면 아나톡신-a가 단순히 활성탄에 흡착되었는지에 대해서는 결론이 나지 않았다.[37] 다른 연구자들은 활성탄을 효과적으로 사용하는 방법에 대한 추가 연구를 요구했다.[39]화학적 처리 방법은 생물학적 처리에 비해 식수 처리에서 더 일반적이며, 아나톡신-a에 대해 다양한 공정이 제안되었다. 산화제인 과망간산 칼륨, 오존, 고급 산화 공정 (AOP) 등은 아나톡신-a의 수준을 낮추는 데 효과가 있었지만, 광촉매 작용, UV 광분해,[39] 및 염소 처리[40] 등은 큰 효과를 보이지 않았다.
물 처리 과정에서 물리적 처리를 통해 시아노박테리아를 직접 제거하는 것(예: 막 여과)도 다른 옵션인데, 블룸이 성장할 때 아나톡신-a의 대부분이 세포 내에 포함되어 있기 때문이다. 그러나 시아노박테리아가 노쇠하고 용해되면 아나톡신-a가 시아노박테리아에서 물로 방출되므로, 물리적 처리가 현재 존재하는 모든 아나톡신-a를 제거하지 못할 수 있다.[41] 더 신뢰할 수 있고 효율적인 검출 및 처리 방법을 찾기 위해 추가 연구가 필요하다.[39]
8. 실험적 연구
1977년, 카마이클(Carmichael), 고럼(Gorham), 빅스(Biggs)는 아나톡신-a 실험을 통해 송아지에 대한 경구 최소 치사량(MLD)을 체중 1kg당 420mg으로 계산했다.[8] 같은 해, 데블린(Devlin) 등은 아나톡신-a의 이환식 2급 아민 구조를 발견하고, 쥐에 대한 LD50을 체중 1kg당 250μg으로 결정했다.[9][1]
1980년 스피박(Spivak) 등은 개구리 대상 전기 생리학적 실험에서 아나톡신-a가 근육형(α1)2βγδ nAChR의 강력한 효능제임을 밝혔다. 이후, 토마스(Thomas) 등은 (1993) 쥐 M 10 세포에서 발현된 닭 α4β2 nAChR 서브유닛과 ''Xenopus laevis'' 난모세포에서 발현된 닭 α7 nAChR을 이용한 연구를 통해 아나톡신-a가 신경 nAChR의 강력한 효능제이기도 하다는 것을 보였다.[1]
아나톡신-a는 근이영양증, 중증 근무력증, 알츠하이머병, 파킨슨병과 같이 아세틸콜린 수치가 낮은 질환 연구에 약리학적 탐침으로 사용된다.[2]
8. 1. 합성 연구
코카인은 아나톡신-a와 유사한 입체 화학을 가지고 있어, 트로판 확장을 위한 초기 물질로 사용된다. 코카인은 먼저 사이클로프로판의 엔도 이성질체로 변환된 다음, 광분해되어 알파, 베타 불포화 케톤을 얻는다. 디에틸 아조디카르복실레이트를 사용하여 케톤을 탈메틸화하고 아나톡신-a를 형성한다. 이와 유사한, 더 최근의 합성 경로는 코카인으로부터 2-트로피논을 생성하고 생성물을 에틸 클로로포름산염으로 처리하여 이환식 케톤을 생성하는 것이다. 이 생성물은 트리메틸실릴디아질메탄, 유기알루미늄 루이스산 및 트리메틸시닐 에놀 에테르와 결합하여 트로피논을 생성한다. 이 방법은 몇 단계를 더 거쳐 유용한 중간체와 최종 생성물인 아나톡신-a를 생성한다.[2]
아나톡신-a를 시험관 내에서 합성하는 데 사용된 최초이자 가장 광범위하게 연구된 접근 방식인 사이클로옥텐 고리화는 1,5-사이클로옥타디엔을 초기 원료로 사용한다. 이 출발 물질은 반응하여 메틸 아민을 형성하고, 차아염소산과 결합하여 아나톡신-a를 형성한다. 동일한 실험실에서 개발된 또 다른 방법은 아미노알코올을 아세트산 수은(II) 및 붕수소화나트륨과 함께 사용하는 것이다. 이 반응의 생성물은 알파, 베타 케톤으로 변환되었고 에틸 아조디카르복실레이트에 의해 산화되어 아나톡신-a를 형성했다.[2]
이미늄 이온 고리화 반응은 아나톡신-a를 생성하기 위해 여러 가지 다른 경로를 사용하지만, 각 경로는 피롤리딘 이미늄 이온을 생성하고 진행한다. 각 경로의 주요 차이점은 이미늄 이온을 생성하는 데 사용되는 전구체와 최종 과정에서 아나톡신-a의 총 수율과 관련이 있다. 이러한 개별 경로는 알킬 이미늄 염, 아실 이미늄 염 및 토실 이미늄 염의 생성을 포함한다.[2]
아나톡신-a의 엔아인 메타테시스는 고리 닫힘 메커니즘을 사용하며, 아나톡신-a 합성의 가장 최근 발전 중 하나이다. 이 경로를 사용하는 모든 방법에서, 파이로글루탐산이 그리브스 촉매와 함께 출발 물질로 사용된다. 이미늄 고리화와 유사하게, 이 경로를 사용한 아나톡신-a의 첫 번째 시도된 합성은 2,5-시스-피롤리딘을 중간체로 사용했다.[2]
참조
[1]
논문
Neurotoxic cyanobacterial toxins
2010-10
[2]
서적
Phycotoxins: Chemistry and Biochemistry
Blackwell Publishing
2007-03
[3]
웹사이트
Health Effects Support Document for the Cyanobacterial Toxin Anatoxin-A
https://www.epa.gov/[...]
2015-06
[4]
논문
Harmful cyanobacterial blooms: causes, consequences, and controls
2013-05
[5]
논문
Cyanobacterial Toxins of the Laurentian Great Lakes, Their Toxicological Effects, and Numerical Limits in Drinking Water
2017-06
[6]
웹사이트
Cyanobacterial toxins: Anatoxin-a
https://www.who.int/[...]
2019-11
[7]
논문
Co-occurrence of the cyanotoxins BMAA, DABA and anatoxin-a in Nebraska reservoirs, fish, and aquatic plants
2014-01
[8]
논문
Two laboratory case studies on the oral toxicity to calves of the freshwater cyanophyte (blue-green alga) Anabaena flos-aquae NRC-44-1
1977-03
[9]
논문
Anatoxin-a, a toxic alkaloid from Anabaena flos-aquae NRC-44h
2011-02-04
[10]
논문
Cyanotoxins: bioaccumulation and effects on aquatic animals
2011-12
[11]
서적
Algae and Man
http://link.springer[...]
Springer US
2020-10-25
[12]
논문
Freshwater harmful algal blooms: toxins and children's health
2014
[13]
논문
A review of: "Detection Methods for Cyanobacterial Toxins"
1995
[14]
간행물
Toxicological Reviews of Cyanobacterial Toxins: Anatoxin-A
http://ofmpub.epa.go[...]
U.S. Environmental Protection Agency
2018-09-22
[15]
논문
The Chemistry and Pharmacology of Anatoxin-a and Related Homotropanes with respect to Nicotinic Acetylcholine Receptors
2006-04-06
[16]
논문
Phytoremediation of anatoxin-a by aquatic macrophyte Lemna trisulca L
2014-10
[17]
논문
Effects of cylindrospermopsin, its decomposition products, and anatoxin-a on human keratinocytes
2020-10
[18]
논문
Potential impact on human health of toxic cyanobacteria 1
1996
[19]
논문
Toxicology and detection methods of the alkaloid neurotoxin produced by cyanobacteria, anatoxin-a
2007-11
[20]
서적
Neuroscience
Sinauer Associates, Inc.
2012
[21]
논문
First report of homoanatoxin-a and associated dog neurotoxicosis in New Zealand
2007-08
[22]
논문
First report in a river in France of the benthic cyanobacterium Phormidium favosum producing anatoxin-a associated with dog neurotoxicosis
2005-06
[23]
논문
Diagnosis of anatoxin-a poisoning in dogs from North America
2008-01
[24]
논문
Fatal Neurotoxicosis in Dogs Associated with Tychoplanktic, Anatoxin-a Producing Tychonema sp. in Mesotrophic Lake Tegel, Berlin
2018-02
[25]
논문
Mass Occurrence of Anatoxin-a- and Dihydroanatoxin-a-Producing Tychonema sp. In Mesotrophic Reservoir Mandichosee (River Lech, Germany) as a Cause of Neurotoxicosis in Dogs
[26]
논문
Contribution of hot spring cyanobacteria to the mysterious deaths of Lesser Flamingos at Lake Bogoria, Kenya
2003-03
[27]
논문
Evidence that Biosynthesis of the Neurotoxic Alkaloids Anatoxin-a and Homoanatoxin-a in the Cyanobacterium Oscillatoria PCC 6506 Occurs on a Modular Polyketide Synthase Initiated by l-Proline
American Chemical Society (ACS)
2009-05-13
[28]
논문
Production and biodegradation of cyanobacterial toxins-a laboratory study.
https://researchport[...]
1991
[29]
논문
Brief review of natural nonprotein neurotoxins.
http://www.asanltr.c[...]
2002
[30]
웹사이트
2015 Drinking Water Health Advisories for Two Cyanobacterial Toxins
https://19january201[...]
2015-06
[31]
서적
Toxic cyanobacteria in water: a guide to their public health consequences, monitoring, and management
E & FN Spon
1999
[32]
웹사이트
Rules and Regulations: Drinking Water HABs Response Plan
https://deq.utah.gov[...]
2020-10-14
[33]
웹사이트
Drinking Water Contaminant Candidate List 3-Final
https://www.federalr[...]
2020-09-27
[34]
웹사이트
Washington State Recreational Guidance for Microcystins (Provisional) and Anatoxin-a (Interim/Provisional)
https://www.doh.wa.g[...]
2008-07
[35]
논문
Vulnerability of Quebec drinking-water treatment plants to cyanotoxins in a climate change context
https://iwaponline.c[...]
2010-09
[36]
논문
State of knowledge and concerns on cyanobacterial blooms and cyanotoxins
2013-09
[37]
논문
Biological treatment options for cyanobacteria metabolite removal--a review
2012-04
[38]
논문
The toxicity of cyanobacterial toxins in the mouse: II anatoxin-a
1999-03
[39]
논문
A review of cyanobacteria and cyanotoxins removal/inactivation in drinking water treatment
2010-07
[40]
논문
State of the art on cyanotoxins in water and their behaviour towards chlorine
2010-04
[41]
논문
Widespread anatoxin-a detection in benthic cyanobacterial mats throughout a river network
2018-05-18
[42]
웹사이트
Notification of Recent Name Changes for Cyanobacteria Adopted and Reported by AWQC
https://www.awqc.com[...]
2015-12-04
[43]
논문
Freshwater neurotoxins and concerns for human, animal, and ecosystem health: A review of anatoxin-a and saxitoxin
2020-09
[44]
논문
Harmful cyanobacterial blooms: causes, consequences, and controls
http://link.springer[...]
2013-05
[45]
논문
Hepatotoxin (microcystin) and neurotoxin (anatoxin-a) contained in natural blooms and strains of cyanobacteria from Japanese freshwaters
1993
[46]
논문
Anatoxin-a producing Tychonema (Cyanobacteria) in European waterbodies
http://nbn-resolving[...]
2015-02
[47]
서적
Phycotoxins: Chemistry and Biochemistry
Blackwell Publishing
2007
[48]
논문
Toxicology and detection methods of the alkaloid neurotoxin produced by cyanobacteria, anatoxin-a
2007
본 사이트는 AI가 위키백과와 뉴스 기사,정부 간행물,학술 논문등을 바탕으로 정보를 가공하여 제공하는 백과사전형 서비스입니다.
모든 문서는 AI에 의해 자동 생성되며, CC BY-SA 4.0 라이선스에 따라 이용할 수 있습니다.
하지만, 위키백과나 뉴스 기사 자체에 오류, 부정확한 정보, 또는 가짜 뉴스가 포함될 수 있으며, AI는 이러한 내용을 완벽하게 걸러내지 못할 수 있습니다.
따라서 제공되는 정보에 일부 오류나 편향이 있을 수 있으므로, 중요한 정보는 반드시 다른 출처를 통해 교차 검증하시기 바랍니다.
문의하기 : help@durumis.com
