탈분극
"오늘의AI위키"의 AI를 통해 더욱 풍부하고 폭넓은 지식 경험을 누리세요.
1. 개요
탈분극은 세포막 전위가 덜 음전하를 띠게 되어 활동 전위 생성을 촉진하는 생리학적 과정이다. 세포가 휴지 상태일 때 이온의 이동을 통해 휴지 전위를 유지하며, 전압 개폐 나트륨 통로가 열리면서 나트륨 이온이 유입되어 탈분극이 시작된다. 이 과정은 나트륨 통로의 비활성화 기전에 의해 종료되며, 재분극, 과분극 단계를 거쳐 휴지 전위가 회복된다. 신경 세포에서 탈분극은 정보를 전달하는 데 중요한 역할을 하며, 자극의 통합, 활동 전위의 발생으로 이어진다. 눈의 간상 세포, 혈관 내피 세포, 심장 세포 등 다양한 세포에서도 탈분극이 나타나며, 탈분극 차단제는 신경근 접합부에서 지속적인 탈분극을 유발하여 근육 마비를 일으킨다.
더 읽어볼만한 페이지
- 전기화학 - 태양광 발전
태양광 발전은 태양빛을 직류 전기로 변환 후 교류 전기로 변환하여 사용하는 기술로, 다양한 종류의 태양전지 개발과 활용이 증가하고 있으나 초기 투자비용, 간헐성, 환경적 영향 등의 과제를 안고 있다. - 전기화학 - 광전 효과
광전 효과는 빛이 물질에 닿을 때 전자가 방출되는 현상으로, 빛 에너지가 광자라는 덩어리로 양자화되어 있고, 아인슈타인의 광양자 가설로 설명되며, 다양한 기술에 응용되지만 문제도 야기한다. - 막생물학 - 포스파티딜에탄올아민
포스파티딜에탄올아민은 세포막의 주요 인지질로서 동물세포에서 심장 기능, 지단백질 분비, 혈액 응고, 아난다마이드 합성에 관여하고, 세균에서는 막 인지질의 음전하 중화, 막 단백질 구조 형성, 다약물 수송체 기능에 필수적이며, 식품 내 마이야르 반응을 통해 산화 스트레스 유발 및 혈관 질환, 당뇨병과의 연관성이 연구된다. - 막생물학 - 소포 (세포)
소포는 막으로 둘러싸인 작은 주머니 모양의 구조물로, 세포 내 물질 수송, 소화, 분비, 세포간 신호 전달, 세포 외부 물질 소화 및 배출 등 다양한 기능을 수행하며, 특히 세포외소포체는 질병과의 연관성으로 주목받고 있고, 클라트린, COPI, COPII, SNARE 단백질 등이 소포 형성 및 수송에 관여한다. - 신경과학 - 인공 일반 지능
인공 일반 지능(AGI)은 추론, 지식 표현, 학습 등의 능력을 갖춘 인공지능 시스템을 의미하며, 기아와 빈곤 해결 등의 이점을 제공하지만 통제력 상실과 같은 위험도 존재한다. - 신경과학 - 계산신경과학
계산신경과학은 컴퓨터 과학과 신경과학의 융합 분야로, 뇌의 정보 처리 과정을 계산 모델로 연구하며, 뇌 기능 설명, 뉴런 및 신경망 모델링, 인공지능 활용 비교 연구, 계산 임상 신경과학 발전 등을 포함한다.
| 탈분극 | |
|---|---|
| 정의 | |
| 설명 | 분극의 반대 현상으로, 세포의 막 전위가 0을 향해 변화하는 현상이다. |
| 원리 | |
| 이온 채널 | 세포막의 이온 채널 개폐를 통해 이온의 흐름이 변화하여 발생한다. |
| 역할 | 신경 세포, 근육 세포 등 흥분성 세포에서 신호 전달에 중요한 역할을 한다. |
| 메커니즘 | |
| 전압 개폐 나트륨 채널 | 전압 개폐 나트륨 채널이 열려 나트륨 이온이 세포 안으로 유입되어 막 전위가 상승한다. |
| 막 전위 변화 | 막 전위가 역치 값 이상으로 상승하면 활동 전위가 발생한다. |
| 관련 용어 | |
| 과분극 (hyperpolarization) | 막 전위가 더욱 음전하를 띠게 되는 현상이다. |
| 저분극 (hypopolarization) | 막 전위가 약간 탈분극되는 현상을 의미한다. (일반적으로 사용되는 용어는 아니다.) |
| 막 전위 (membrane potential) | 세포막을 경계로 세포 안팎의 전위차를 의미한다. |
| 활동 전위 (action potential) | 신경 세포나 근육 세포에서 발생하는 전기적 신호이다. |
2. 생리학적 기전
세포의 탈분극 과정은 대부분의 세포가 가진 고유한 전기적 특성에 전적으로 의존한다. 세포가 휴지 상태일 때, 세포는 휴지 전위라고 알려진 상태를 유지한다. 거의 모든 세포에서 생성되는 휴지 전위는 세포 내부가 세포 외부에 비해 음전하를 띠게 한다. 이러한 전기적 불균형을 유지하기 위해, 이온들이 세포의 세포막을 가로질러 수송된다.[3] 이온의 세포막 수송은 세포 안팎으로 이온 통로 역할을 하는 세포막에 내장된 여러 종류의 막횡단 단백질, 예를 들어 이온 통로, 나트륨-칼륨 펌프, 전압 개폐 이온 통로 등을 통해 이루어진다.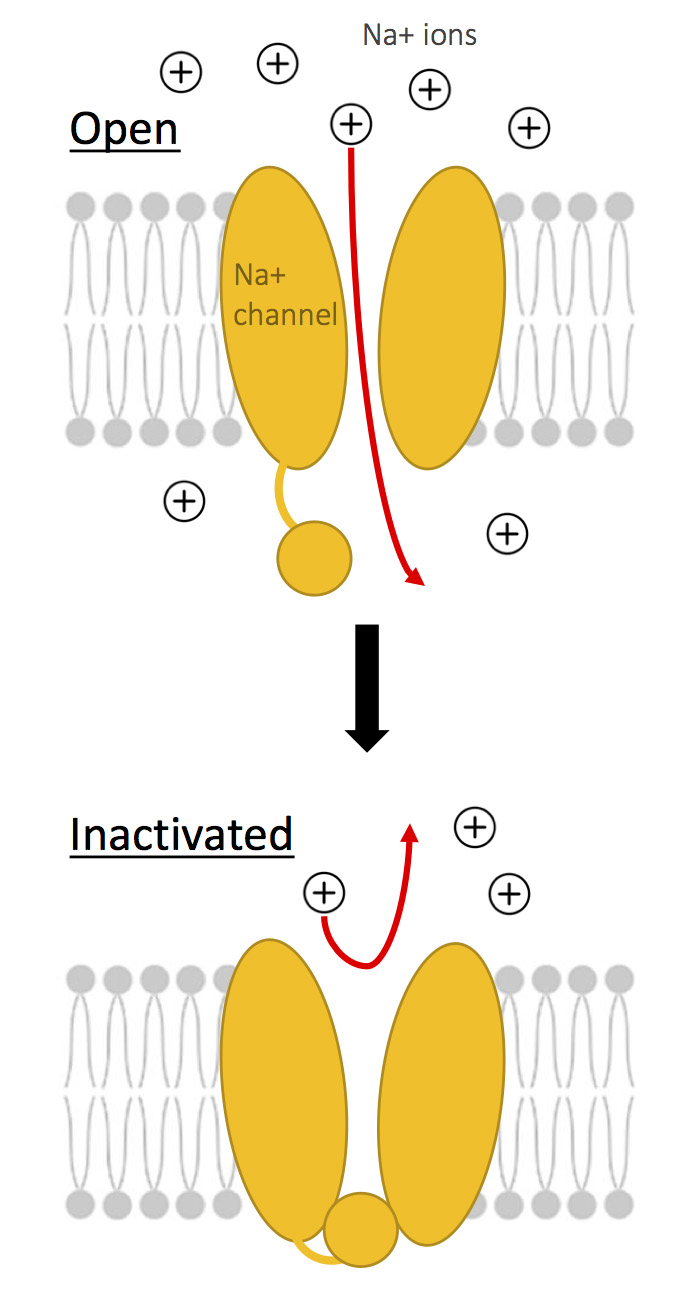
세포가 안정 전위를 확립한 후, 해당 세포는 탈분극을 겪을 수 있는 능력을 갖게 된다. 탈분극은 막 전위가 덜 음전하를 띠게 되어 활동 전위의 생성을 촉진하는 과정이다.[6] 이러한 급격한 변화가 세포 내부에서 일어나기 위해서는 세포의 원형질막을 따라 여러 사건이 발생해야 한다.
나트륨-칼륨 펌프가 계속 작동하는 동안, 세포가 안정 전위에 있을 때 닫혀 있던 전압 개폐 나트륨 및 칼슘 통로[7]는 전압의 초기 변화에 반응하여 열린다.[6] 신경 세포의 전하 변화는 전압 개폐 나트륨 통로의 개방으로 이어지며, 이는 나트륨 이온이 전기화학적 기울기를 따라 유입되는 결과를 낳는다. 나트륨 이온은 세포 내부로 들어가 세포 내부에 양전하를 기여하여 막 전위를 음전하에서 양전하로 변화시킨다. 초기 나트륨 이온 유입은 추가적인 나트륨 통로의 개방을 유발하여 (양성 피드백 고리), 더 많은 나트륨 이온이 세포로 이동하여 양의 평형 전위에 도달할 때까지 탈분극 과정을 지속시킨다.[8]
나트륨 통로는 막이 탈분극 상태를 유지하는 동안에도 재빠르게 닫히도록 하는 고유의 비활성화 기전을 가지고 있다. 이러한 평형 상태 동안, 나트륨 통로는 비활성화 상태로 들어가, 막 전위가 다시 음전하를 띠게 될 때까지 나트륨 이온의 유입을 일시적으로 중단시킨다. 세포 내부가 충분히 양전하를 띠게 되면, 탈분극이 종료되고 통로는 다시 닫힌다.[6]
2. 1. 휴지 전위
세포는 안정 상태에서 세포 안팎의 이온 농도 차이로 인해 휴지 전위를 유지한다. 이러한 휴지 전위는 이온 채널, 이온 펌프, 전압 개폐 이온 채널을 통해 형성된다.[4] 나트륨-칼륨 펌프는 세포 밖으로 3개의 나트륨 이온(Na+)을 내보내고, 세포 안으로 2개의 칼륨 이온(K+)을 들여보내는 과정에서 ATP를 사용하여 휴지 전위 형성에 기여한다.[5] 이 과정은 세포 밖의 나트륨 농도를 높이고 세포 안의 칼륨 농도를 높여 농도 기울기를 형성한다.[5]세포 내부에 과도한 양의 칼륨 이온이 존재하고, 세포 외부에 나트륨 이온이 존재하지만, 안정 막 전위는 세포막의 전압 개폐 이온 채널을 닫힌 상태로 유지시킨다. 이는 막을 가로질러 펌핑된 이온의 확산을 막고, 칼륨 누출 채널을 통해 제어된 칼륨 이온 유출을 가능하게 하여 음전하를 띤 안정 막 전위 형성에 기여한다.[6] 또한, 대부분의 세포는 음전하를 띤 내부 구성 요소를 포함하고 있어 세포 안은 상대적으로 음전하를 띠게 된다.
2. 2. 탈분극
세포가 안정 전위를 확립한 후, 해당 세포는 탈분극을 겪을 수 있는 능력을 갖게 된다. 탈분극은 막 전위가 덜 음전하를 띠게 되어 활동 전위의 생성을 촉진하는 과정이다.[6] 이러한 급격한 변화가 세포 내부에서 일어나기 위해서는 세포의 원형질막을 따라 여러 사건이 발생해야 한다.
나트륨-칼륨 펌프가 계속 작동하는 동안, 세포가 안정 전위에 있을 때 닫혀 있던 전압 개폐 나트륨 및 칼슘 통로[7]는 전압의 초기 변화에 반응하여 열린다.[6] 신경 세포의 전하 변화는 전압 개폐 나트륨 통로의 개방으로 이어지며, 이는 나트륨 이온이 전기화학적 기울기를 따라 유입되는 결과를 낳는다. 나트륨 이온은 세포 내부로 들어가 세포 내부에 양전하를 기여하여 막 전위를 음전하에서 양전하로 변화시킨다. 초기 나트륨 이온 유입은 추가적인 나트륨 통로의 개방을 유발하여 (양성 피드백 고리), 더 많은 나트륨 이온이 세포로 이동하여 양의 평형 전위에 도달할 때까지 탈분극 과정을 지속시킨다.[8]
나트륨 통로는 막이 탈분극 상태를 유지하는 동안에도 재빠르게 닫히도록 하는 고유의 비활성화 기전을 가지고 있다. 이러한 평형 상태 동안, 나트륨 통로는 비활성화 상태로 들어가, 막 전위가 다시 음전하를 띠게 될 때까지 나트륨 이온의 유입을 일시적으로 중단시킨다. 세포 내부가 충분히 양전하를 띠게 되면, 탈분극이 종료되고 통로는 다시 닫힌다.[6]
2. 3. 재분극
탈분극 후, 전압 개폐성 나트륨 채널은 불활성화되고, 전압 개폐성 칼륨 채널이 열린다.[9] 칼륨 이온(K+)은 전기화학적 기울기를 따라 세포 밖으로 유출되면서 세포막 전위는 다시 음전하로 돌아간다.[9][20] 이 과정에서 나트륨-칼륨 펌프는 지속적으로 작용하여 세포 안팎의 이온 농도를 원래 상태로 회복시킨다.[9]2. 4. 과분극
재분극 과정에서 칼륨 이온이 신경 섬유 밖으로 계속 이동하면 세포 전위가 안정 전위를 초과하여 휴지 전위보다 더 낮아지는 과분극 상태가 된다.[10] 모든 전압 의존성 이온 채널이 닫히고, 나트륨-칼륨 이온 펌프가 활동함으로써 최종적으로 휴지 전위가 회복된다.[21] 과분극은 신경 세포의 흥분성을 일시적으로 감소시킨다.3. 신경 세포에서의 탈분극
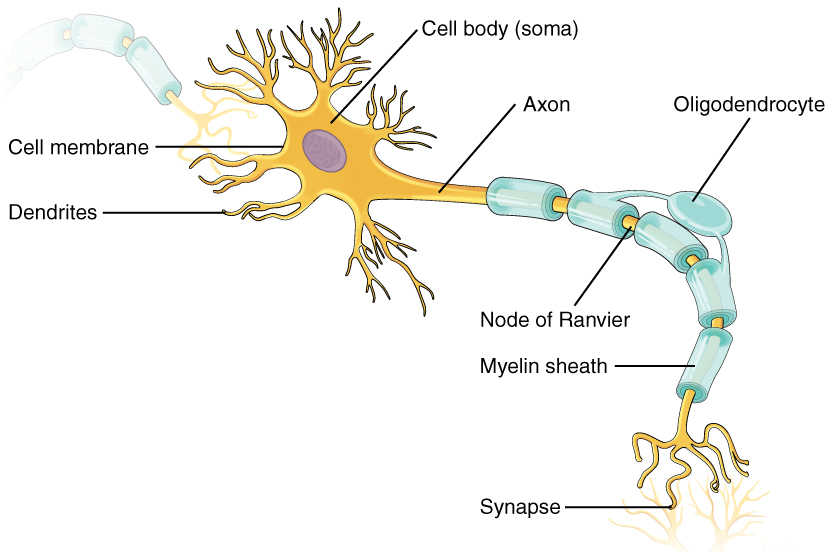
신경 세포(뉴런)는 탈분극을 통해 정보를 전달하는 흥분성 세포이다. 탈분극은 인체의 많은 세포 기능에 필수적이며, 그 예시로 신경 세포 (뉴런) 내부, 그리고 두 신경 세포 간의 자극 전달을 들 수 있다. 자극의 수용, 이러한 자극들의 신경 통합, 그리고 자극에 대한 신경 세포의 응답은 모두 신경 세포 내 또는 신경 세포 간에 자극을 전달하기 위해 탈분극을 이용하는 신경 세포의 능력에 의존하고 있다.
;자극에 대한 반응
신경 세포에 대한 자극은 물리적, 전기적 또는 화학적일 수 있으며 자극을 받는 신경 세포를 억제하거나 흥분시킬 수 있다. 억제성 자극은 신경 세포의 과분극을 유발하여 신경 세포의 수상돌기로 전달된다. 억제성 자극에 따른 과분극은 신경 세포 내 전압을 휴지 전위보다 더 감소시킨다. 신경 세포를 과분극시킴으로써 억제성 자극은 탈분극이 발생하기 위해 극복해야 하는 더 큰 음전하를 초래한다.
반면, 흥분성 자극은 신경 세포의 전압을 증가시켜 휴지 상태의 동일한 신경 세포보다 탈분극이 더 쉬운 신경 세포를 생성한다. 흥분성이든 억제성이든 자극은 통합을 위해 신경 세포의 수상돌기를 따라 세포체로 이동한다.
;자극의 통합
수상돌기에서 발생한 전위 변화는 세포체로 모여 축삭 언덕에서 수렴되며, 여기서 가중되어 신경 반응을 결정한다.[23] 여러 자극의 합이 역치 전위로 알려진 특정 전압에 도달하면 탈분극이 축삭둔덕에서 축삭 아래로 이어진다.[23]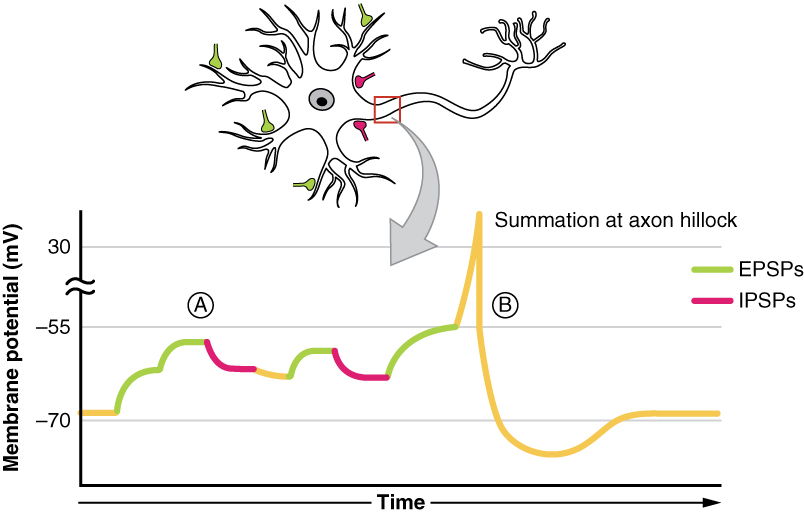
;활동 전위
탈분극의 급증은 축삭 구릉에서 축삭 종말로 이동하며, 이를 활동 전위라고 한다. 활동 전위는 축삭 종말에 도달하여 신경 세포에서 신경전달물질의 방출을 유도한다. 축삭에서 방출된 신경전달물질은 다른 신경 세포나 근육 세포와 같은 다른 세포를 계속 자극한다. 활동 전위 발생 후에는 신경 세포의 회복 기간이 필요하며, 이 기간 동안 신경 세포는 다른 활동 전위를 전달할 수 없다.
3. 1. 자극에 대한 반응
신경 세포에 대한 자극은 물리적, 전기적 또는 화학적일 수 있으며 자극을 받는 신경 세포를 억제하거나 흥분시킬 수 있다. 억제성 자극은 신경 세포의 과분극을 유발하여 신경 세포의 수상돌기로 전달된다. 억제성 자극에 따른 과분극은 신경 세포 내 전압을 휴지 전위보다 더 감소시킨다. 신경 세포를 과분극시킴으로써 억제성 자극은 탈분극이 발생하기 위해 극복해야 하는 더 큰 음전하를 초래한다.반면, 흥분성 자극은 신경 세포의 전압을 증가시켜 휴지 상태의 동일한 신경 세포보다 탈분극이 더 쉬운 신경 세포를 생성한다. 흥분성이든 억제성이든 자극은 통합을 위해 신경 세포의 수상돌기를 따라 세포체로 이동한다.
3. 2. 자극의 통합
수상돌기에서 발생한 전위 변화는 세포체로 모여 축삭 언덕에서 수렴되며, 여기서 가중되어 신경 반응을 결정한다.[23] 여러 자극의 합이 역치 전위로 알려진 특정 전압에 도달하면 탈분극이 축삭둔덕에서 축삭 아래로 이어진다.[23]3. 3. 활동 전위
탈분극의 급증은 축삭 구릉에서 축삭 종말로 이동하며, 이를 활동 전위라고 한다. 활동 전위는 축삭 종말에 도달하여 신경 세포에서 신경전달물질의 방출을 유도한다. 축삭에서 방출된 신경전달물질은 다른 신경 세포나 근육 세포와 같은 다른 세포를 계속 자극한다. 활동 전위 발생 후에는 신경 세포의 회복 기간이 필요하며, 이 기간 동안 신경 세포는 다른 활동 전위를 전달할 수 없다.4. 다양한 세포에서의 탈분극
4. 1. 눈의 간상 세포
눈의 간상 세포는 어두운 환경에서 탈분극 상태를 유지하는 독특한 특징을 가지고 있다.[11] 간상 세포의 높은 전압은 이온 채널을 열린 상태로 유지하여 칼슘과 나트륨 이온이 세포 내로 자유롭게 유입되도록 한다. 이러한 이온 유입은 간상 세포의 탈분극 상태를 지속시키고, 신경 전달 물질을 계속 방출하게 만든다.[11] 방출된 신경 전달 물질은 간상 세포와 연결된 신경을 자극한다.그러나 간상 세포가 빛을 흡수하면, 나트륨과 칼슘 이온의 유입을 돕던 채널이 닫히면서 변화가 일어난다. 채널이 닫히면 간상 세포는 신경 전달 물질의 생산을 줄이게 되고, 뇌는 이를 빛의 증가로 인식한다. 즉, 간상 세포의 경우 탈분극은 신호 전달을 억제하는 역할을 한다.[11]
4. 2. 혈관 내피 세포
내피(혈관이나 림프관의 내면을 덮고 있는 단층 편평 상피세포의 얇은 층)는 혈류와 혈압의 힘을 받으며 견뎌야 한다.[25] 이러한 힘에 견디기 위해 내피 세포는 순환의 힘을 견딜 수 있는 구조를 가지면서도 구조 강성에 가소성을 유지해야 한다.[25] 혈관 내피 세포는 구조 강도를 변화시켜 혈관의 긴장도를 유지하고, 혈관 경화를 방지하며, 혈압을 조절한다.[25] 내피 세포는 탈분극을 통해 구조적 강도를 변화시켜 이러한 기능을 수행한다.[25] 탈분극은 내피 세포의 구조적 완전성과 혈관 긴장 조절, 혈관 경화 방지, 혈압 조절 능력에 필수적이다.[25]4. 3. 심장 세포
심장 세포는 규칙적인 탈분극과 재분극을 통해 심장 박동을 생성한다. 탈분극은 심장의 네 개의 방에서 발생하며, 먼저 양쪽 심방에서, 이어서 양쪽 심실에서 순차적으로 발생한다.[13][27]# 오른쪽 심방 벽에 있는 동방 결절은 오른쪽 및 왼쪽 심방에서 탈분극을 시작하여 수축을 유발하며, 이는 심전도에서 P파에 해당한다.[13][27]
# 동방 결절에서 시작된 탈분극 파동은 방실 결절로 전달된다. 방실 결절은 약 100ms의 지연 시간을 두고 심방이 수축을 완료하도록 한 다음, 양쪽 심실에서 수축을 유발하며, 이는 심전도의 QRS파에서 나타난다. 동시에 심방은 재분극되어 이완된다.[13][27]
# 심실은 T파에서 재분극되어 이완된다.[13][27]
이 과정은 심장에 문제가 없는 한 규칙적으로 계속된다.[13][27] 심전도는 이러한 심장 세포의 탈분극 및 재분극 과정을 기록한 것이다.[26]
5. 탈분극 차단제
탈분극 차단제는 신경근 접합부에서 탈분극을 지속시켜 근육 마비를 유발하는 약물이다.[14] 니코틴성 수용체 효능제인 석시닐콜린과 데카메토늄이 대표적인 예시이다.[14] 이들은 니코틴 작용제로서, 니코틴 수용체에 작용하여 탈분극을 유도하고, 지속적인 탈분극 상태를 유지시켜 재분극을 방해한다.
참조
[1]
서적
Psychobiology of Personality
https://books.google[...]
Cambridge University Press
1991-05-31
[2]
서적
Environmental Toxicology and Risk Assessment: 2nd volume
https://books.google[...]
ASTM International
1993-01-01
[3]
간행물
The Ionic Basis of the Resting Membrane Potential
https://www.ncbi.nlm[...]
Sinauer Associates
2001
[4]
간행물
Physiology, Resting Potential
http://www.ncbi.nlm.[...]
StatPearls Publishing
2024
[5]
간행물
Physiology, Sodium Potassium Pump
http://www.ncbi.nlm.[...]
StatPearls Publishing
2024
[6]
간행물
Ion Channels and the Electrical Properties of Membranes
https://www.ncbi.nlm[...]
Garland Science
2002
[7]
문서
Calcium-Dependent Regulation of Ion Channels
2006
[8]
간행물
Physiology, Action Potential
http://www.ncbi.nlm.[...]
StatPearls Publishing
2024
[9]
서적
Molecular Cell Biology
https://archive.org/[...]
W. H. Freeman and Company
2000
[10]
서적
Salters-Nuffield Advanced Biology for Edexcel A2 Biology
Pearson Wducation
2009
[11]
서적
Molecular Cell Biology
https://archive.org/[...]
W. H. Freeman and Company
2000
[12]
논문
Membrane potential depolarization decreases the stiffness of vascular endothelial cells
2011-06-01
[13]
서적
Human anatomy & physiology
Pearson Education Inc.
2014
[14]
서적
Pharmacology
Churchill Livingstone
2003
[15]
서적
Psychobiology of Personality
https://books.google[...]
Cambridge University Press
1991-05-31
[16]
서적
Environmental Toxicology and Risk Assessment: 2nd volume
https://books.google[...]
ASTM International
1993-01-01
[17]
웹사이트
12.4 The Action Potential
https://openstax.org[...]
Rice University
2023-11-29
[18]
서적
Psychobiology of Personality
https://books.google[...]
Cambridge University Press
1991-05-31
[19]
서적
Environmental Toxicology and Risk Assessment: 2nd volume
https://books.google[...]
ASTM International
1993-01-01
[20]
서적
Molecular Cell Biology
https://archive.org/[...]
W. H. Freeman and Company
2000
[21]
서적
Salters-Nuffield Advanced Biology for Edexcel A2 Biology
Pearson Wducation
2009
[22]
웹사이트
12.2 Nervous Tissue
https://openstax.org[...]
Rice University
2023-11-29
[23]
웹사이트
12.5 Communication Between Neurons
https://openstax.org[...]
Rice University
2023-11-29
[24]
서적
Molecular Cell Biology
https://archive.org/[...]
W. H. Freeman and Company
2000
[25]
논문
Membrane potential depolarization decreases the stiffness of vascular endothelial cells
2011-06-01
[26]
웹사이트
19.2 Cardiac Muscle and Electrical Activity
https://openstax.org[...]
Rice University
2023-11-29
[27]
서적
Human anatomy & physiology
Pearson Education Inc.
2014
[28]
서적
Pharmacology
Churchill Livingstone
2003
본 사이트는 AI가 위키백과와 뉴스 기사,정부 간행물,학술 논문등을 바탕으로 정보를 가공하여 제공하는 백과사전형 서비스입니다.
모든 문서는 AI에 의해 자동 생성되며, CC BY-SA 4.0 라이선스에 따라 이용할 수 있습니다.
하지만, 위키백과나 뉴스 기사 자체에 오류, 부정확한 정보, 또는 가짜 뉴스가 포함될 수 있으며, AI는 이러한 내용을 완벽하게 걸러내지 못할 수 있습니다.
따라서 제공되는 정보에 일부 오류나 편향이 있을 수 있으므로, 중요한 정보는 반드시 다른 출처를 통해 교차 검증하시기 바랍니다.
문의하기 : help@durumis.com