5-메틸사이토신
"오늘의AI위키"의 AI를 통해 더욱 풍부하고 폭넓은 지식 경험을 누리세요.
1. 개요
5-메틸사이토신은 사이토신에 메틸기가 결합된 유도체로, 1898년 결핵균에서 처음 발견되었다. 세균, 식물, 진균, 동물 등 다양한 생물체에서 발견되며, DNA 메틸화 과정에 관여하여 유전자 발현 조절, DNA 보호 등의 기능을 수행한다. 5-메틸사이토신은 DNA 내에서 사이토신과 유사하게 작용하지만, 탈아미노화 시 티민으로 변환되어 돌연변이를 유발할 수 있다. 또한, 암세포에서 DNA 메틸화 이상과 관련되어 있으며, 암 발생 및 진행에 중요한 역할을 한다. 아황산 수소염 시퀀싱을 통해 DNA 메틸화 패턴 분석에 활용되기도 한다.
더 읽어볼만한 페이지
- 바이오마커 - 맞춤의학
맞춤의학은 환자의 유전적, 분자 생물학적, 세포적 특징을 고려하여 개인에게 최적화된 치료법을 제공하는 의료 모델로, 더 나은 진단과 효율적인 약물 개발, 표적화된 치료법을 제공하지만 데이터 관련 문제와 규제 및 윤리적 문제 등의 과제를 안고 있다. - 바이오마커 - C-반응성 단백질
C-반응성 단백질(CRP)은 간에서 생성되는 단백질로, 염증 반응의 지표로 사용되며, 세균 감염, 조직 손상, 자가면역 질환 등에서 혈중 농도가 증가하여 면역 반응에 기여한다. - 핵염기 - 티민
티민은 DNA의 네 가지 염기 중 하나로, 아데닌과 수소 결합을 통해 DNA 구조를 안정화시키며, DNA 복제, 돌연변이, 암 치료제 표적, 그리고 우주 기원 연구와 관련되어 있다. - 핵염기 - 아데닌
아데닌은 DNA의 티민, RNA의 유라실과 상보적으로 결합하는 퓨린 염기로, 아데노신 삼인산 형태로 에너지 대사에 중요한 역할을 하며 공업적으로 생산되는 생명의 기원 연구 물질이다. - 피리미딘 - 이마티닙
이마티닙은 Bcr-Abl 티로신 키나아제를 포함한 여러 티로신 키나아제의 활성을 선택적으로 억제하는 표적 항암제로, 만성 골수성 백혈병과 위장관기질종양 치료에 주로 사용되며, FDA 승인 후 CML 환자의 생존율을 크게 향상시켰고, 사회경제적 논란에도 불구하고 암 치료에 획기적인 발전을 가져온 약물로 평가받는다. - 피리미딘 - 티민
티민은 DNA의 네 가지 염기 중 하나로, 아데닌과 수소 결합을 통해 DNA 구조를 안정화시키며, DNA 복제, 돌연변이, 암 치료제 표적, 그리고 우주 기원 연구와 관련되어 있다.
| 5-메틸사이토신 - [화학 물질]에 관한 문서 | |
|---|---|
| 일반 정보 | |
 | |
| IUPAC 이름 | 4-아미노-5-메틸-3H-피리미딘-2-온 |
| 기타 이름 | 4-아미노-5-메틸피리미딘-2(1H)-온 |
| 식별자 | |
| ChemSpider ID | '58551' |
| 3DMet | B00435 |
| EINECS | 209-058-3 |
| Beilstein 등록 번호 | '120387' |
| KEGG | C02376 |
| InChI | 1/C5H7N3O/c1-3-2-7-5(9)8-4(3)6/h2H,1H3,(H3,6,7,8,9) |
| InChIKey | LRSASMSXMSNRBT-UHFFFAOYAO |
| SMILES | Cc1cnc(=O)[nH]c1N |
| 표준 InChI | 1S/C5H7N3O/c1-3-2-7-5(9)8-4(3)6/h2H,1H3,(H3,6,7,8,9) |
| 표준 InChIKey | LRSASMSXMSNRBT-UHFFFAOYSA-N |
| CAS 등록번호 | '554-01-8' |
| PubChem CID | '65040' |
| UNII | 6R795CQT4H |
| ChEBI | '27551' |
| MeSH 이름 | 5-메틸사이토신 |
| 특성 | |
| 분자식 | C5H7N3O |
| 겉모습 | 해당 없음 |
| 밀도 | 해당 없음 |
| 녹는점 | 해당 없음 |
| 끓는점 | 해당 없음 |
| 용해도 | 해당 없음 |
| 위험성 | |
| GHS 그림 문자 | '' |
| 신호어 | 경고 |
| H 문구 | '' |
| P 문구 | '' |
| 주요 위험 | 해당 없음 |
| 인화점 | 해당 없음 |
| 자연 발화 온도 | 해당 없음 |
| 관련 화합물 | |
| 관련 DNA 염기 | 사이토신 |
| 기타 | |
| 참고 문헌 | Wu, Xiaoji; Zhang, Yi (2017년 9월). TET-mediated active DNA demethylation: mechanism, function and beyond. Nature Reviews. Genetics. 18 (9): 517–534. doi:10.1038/nrg.2017.33. ISSN 1471-0064. PMID 28555658. |
2. 발견
1898년, W.G. 루펠은 결핵균에서 독소를 분리하는 과정에서 투베르쿨린산(tuberculinic acid)이라는 새로운 핵산을 분리했는데,[64] 이 핵산은 메틸화된 뉴클레오티드를 일부 포함하고 있었다. 1925년, T.B. 존슨과 R.D. 코힐은 결핵균 핵산의 가수분해 생성물로서 5-메틸사이토신을 극소량 검출하는 데 성공했다.[65][66] 그러나 이들의 방법은 일반적으로 재현할 수 없었기에 해당 핵산을 분리하는 일반적인 방법으로 인정받지 못했다.[67] 1948년, R.D. 핫키스는 종이 크로마토그래피를 사용하여 송아지의 흉선에서 DNA 핵산을 분리했다.[68] 그로부터 70년 후, 정확한 역할은 불확실하나 다른 RNA 분자에서도 공통적으로 존재한다는 것이 밝혀졌다.[69]
5-메틸사이토신의 기능은 종에 따라 크게 다르다.[71] 세균, 식물, 진균 및 동물에서 5-메틸사이토신이 발견되는 위치와 역할은 차이를 보인다.
3. 제법
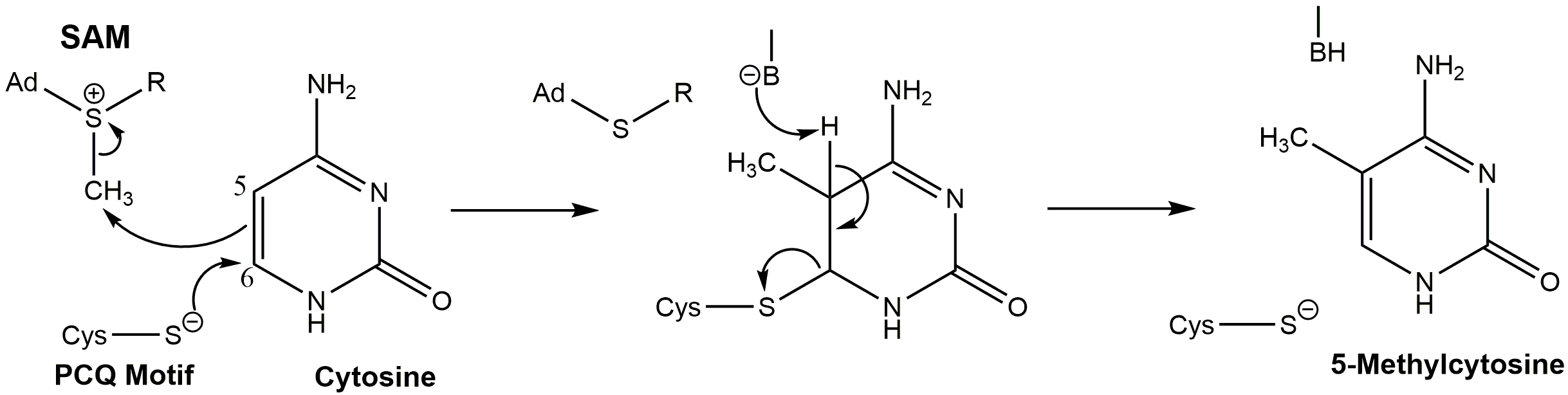
단백질에 널리 분포하는 DNA메틸기전달효소(DNMT)의 PCQ 시스테인 잔기(cysteine residue)가 사이토신의 6번 탄소 결합 부위에 친핵성 공격을 가할 경우 S-아데노실메싸이오닌(S-Adenosylmethionine)이 메틸기를 사이토신 5번 탄소 결합 부위에 기여한다. 그 후 DNMT 효소의 염기가 사이토신 5번 탄소 결합 부위에 붙어있는 양자화된 상태의 수소를 탈양자화하여 5번 결합 부위와 6번 결합 부위 사이에 이중결합을 형성한다. 이렇게 될 경우 S-아데노실메싸이오닌은 떨어져 나가고, 사이토신은 메틸화된다.[70]
사이토신과 요오드화메틸 및 알코올칼리를 함께 가열하면 생성되며, 다른 방법으로는 소맥 배아에서 추출한 천연 데옥시리보핵산을 가수 분해하여 얻어낼 수 있다.
4. 생체 내 기능
4. 1. 세균
세균에서 5-메틸사이토신은 다양한 위치에서 발견될 수 있으며, 종종 메틸화 특이적인 제한 효소(methylation-sensitive restriction enzyme, '''MSRE''')에 의해 DNA가 절단되는 것을 보호하기 위한 표지자로 사용된다.[71]
4. 2. 식물
5-메틸사이토신은 식물에서 CpG, CpHpG, CpHpH 서열에서 발견된다(여기서 H는 아데닌(A), 사이토신(C), 티민(T) 중 하나이다).[71][8][38]
4. 3. 진균과 동물
진균과 동물에서 5-메틸사이토신은 주로 CpG 디뉴클레오타이드에서 발생한다.[71] 대부분의 진핵생물은 이 부위에서 아주 작은 비율만을 메틸화하지만, 척추동물의 경우는 CpG 사이토신의 70-80%에서 메틸화된다.[72] 5-메틸사이토신은 전체 포유류 DNA에서 1%의 비중을 차지하고 있다.[10]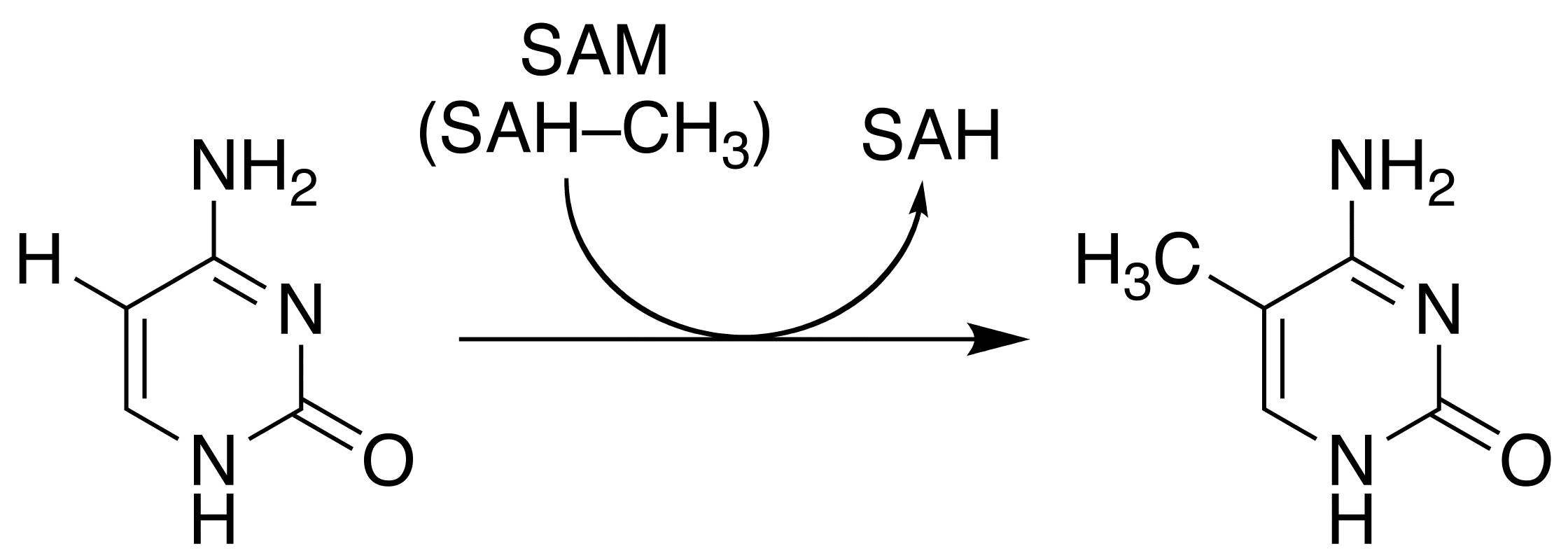
사이토신이 자발적인 탈아미노화를 거쳐서 우라실(U)이 될 경우 DNA 복구 효소가 이를 제거하지만, 5-메틸사이토신의 탈아미노화는 티민(T)을 형성한다. 5-메틸사이토신은 DNA 내에서 사이토신으로 작용하나 위와 같은 반응이 있을 경우 5-메틸사이토신은 티민으로 작용할 수 있기에 DNA 염기에서 전이 돌연변이를 야기할 수 있다.[73] 또한, 사이토신의 활성 효소적 탈아미노화와 사이토신 탈아미노제의 APOBEC 패밀리 집단에 의한 5-메틸사이토신은 다양한 세포 과정 및 유기체 진화에 유리한 영향을 미칠 수 있다.[74]
5. 생체 외 기능
5-메틸사이토신은 중아황산염 처리(bisulfite treatment)를 할 경우 탈아미노화에 대한 저항성을 가진다. 이러한 특성을 이용하여 DNA 내 사이토신의 메틸화 패턴을 분석하는 재료로 사용할 수 있다.[75] 5-메틸사이토신에서 NH2기는 아질산과 같은 시약을 사용하여 제거(탈아미노화)되어 티민을 형성할 수 있다. 사이토신은 유사한 조건에서 탈아미노화되어 우라실(U)이 된다.
5-메틸사이토신은 사이토신 잔기를 탈아미노화하는 아황산 수소염 처리에 저항성이 있다. 이러한 특성은 종종 아황산 수소염 시퀀싱을 사용하여 DNA 사이토신 메틸화 패턴을 분석하는 데 활용된다.[13][43]
6. 탈메틸화
사이토신이 5mC로 메틸화된 후, 여러 메커니즘을 통해 원래 상태로 되돌릴 수 있다. 수동적 DNA 탈메틸화는 DNMT에 의한 유지 부족으로 복제를 통해 표지를 점진적으로 제거한다. 능동적 DNA 탈메틸화 과정에서 일련의 산화 반응을 통해 5-하이드록시메틸사이토신(5hmC), 5-폼일사이토신(5fC), 5-카복실사이토신(5caC)으로 변환되며, 후자 두 가지는 결국 티민 DNA 글리코실라제(TDG)에 의해 잘려나가고, 염기 절제 복구(BER)를 통해 사이토신을 복원한다.[1] TDG 녹아웃은 5hmC 수준에 통계적으로 유의미한 변화 없이 5fC가 2배 증가하는 결과를 낳았으며, 이는 5mC가 완전한 탈메틸화 전에 적어도 두 번 반복적으로 산화되어야 함을 나타낸다.[18]
산화는 TET(Ten-eleven translocation) 계열 다이옥시게나제를 통해 발생하며, 이 효소는 5mC, 5hmC, 5fC를 산화된 형태로 변환할 수 있다. 그러나 이 효소는 5mC에 대한 선호도가 가장 높으며, TET2를 이용한 5hmC 및 5fC 변환의 초기 반응 속도는 4.9~7.6배 느리다.[19] TET는 보조 인자로 Fe(II), 기질로 산소 및 α-케토글루타르산(α-KG)을 필요로 하며, 후자의 기질은 효소 이소시트르산 탈수소효소(IDH)에 의해 이소시트르산으로부터 생성된다.[20] 그러나 암은 2-하이드록시글루타르산(2HG)을 생성하여 α-KG와 경쟁하고, TET 활성을 감소시키며, 결과적으로 5mC를 5hmC로의 변환을 감소시킬 수 있다.[21]
7. 인간에서의 역할
5-메틸사이토신(5mC)은 생물 종에 따라 그 기능이 크게 다르다.[38]
- 세균에서 5mC는 게놈의 다양한 위치에 존재하며, 종종 자신의 DNA를 메틸화에 민감한 제한 효소로부터 보호하는 마커로 기능한다.
- 식물에서 5mC는 CpG 사이트, CpHpG, CpHpH 서열에 국한된다(H = A, C, T).
- 균류 및 동물에서 5mC는 주로 CpG 디뉴클레오타이드 형태로 존재한다. 많은 진핵생물에서 CpG 사이트의 메틸화율은 낮지만, 척추동물의 경우 CpG 중 시토신의 70~80%가 메틸화되어 있다.[39] 포유류의 경우 게놈 내 염기의 약 1%가 5mC이다.[40]
시토신(C)이 자발적으로 탈아미노화되면 우라실(U)이 되고, DNA 복구 효소에 의해 제거된다. 반면 5mC가 탈아미노화되면 티민(T)이 생성된다. 이러한 염기 전환(C→T)은 염기 전이형 돌연변이를 일으킬 수 있다.[41] 또한, APOBEC 패밀리 효소에 의한 시토신 및 5mC의 탈아미노화는 세포 내 과정이나 생물 종의 진화에 관여할 가능성이 있다.[42] 한편, 5-히드록시메틸사이토신의 탈아미노화 의의 및 상세는 불분명하다.
5mC의 메틸기는 DNA 메틸트랜스퍼라제(DNMT)를 통해 게놈 DNA 내 시토신에 부착된다. 인간 게놈 내에는 DNMT1, DNMT2, DNMT3A, DNMT3B, DNMT3L의 5가지 DNMT가 알려져 있다. 조류 및 균류에는 DNMT4, DNMT5, DNMT6의 3가지가 더 존재한다.[44]
DNMT1에는 RFTS(replication foci targeting sequence)와 5mC 마크 추가를 촉매하는 CXXC 도메인이 포함되어 있다. RFTS는 DNMT1을 DNA 복제 위치로 이끌어 DNA 복제 중 딸 가닥 상의 5mC 유지를 돕는다. CXXC는 DNA에 메틸화를 ''de novo''로 추가하기 위한 징크 핑거 도메인을 포함한다.[45] 많은 인간 체조직에서 DNMT1이 지배적인 DNA 메틸트랜스퍼라제인 것으로 알려져 있다.[46] DNMT3A와 DNMT3B는 주로 ''de novo'' 메틸화를 담당하며, DNMT1은 복제 후 5mC 마크를 유지하는 역할을 한다.[47] DNMT는 서로 상호 작용하여 메틸화 능력을 높인다. 예를 들어, 2개의 DNMT3L은 2개의 DNMT3A와 복합체를 형성하여 DNA와의 상호 작용을 개선하고 메틸화를 촉진한다.[48] DNMT 발현 변화는 비정상적인 메틸화를 야기한다. 과도한 발현은 메틸화 증가를 가져오고, 반대로 효소를 파괴하면 메틸화 수준이 저하된다.[46]
메틸기 추가 메커니즘은 다음과 같다.[49]
# DNMT의 PCQ 모티프 시스테인 잔기가 메틸화되는 시토신 뉴클레오타이드의 탄소 6에 친핵성 공격을 일으킨다.
# S-아데노실메티오닌은 메틸기를 탄소 5에 제공한다.
# DNMT 효소의 염기는 5번 탄소의 잔류 수소를 탈프로톤화하여 5번과 6번 탄소 사이의 이중 결합을 복원하여 5-메틸사이토신 염기쌍을 생성한다.
시토신이 5mC로 메틸화된 후, 여러 메커니즘을 통해 원래 상태로 되돌릴 수 있다. 수동적 DNA 탈메틸화는 DNMT에 의한 유지를 억제하여, 게놈 복제를 통해 서서히 메틸화된 시토신을 희석시키는 것이다. 능동적 DNA 탈메틸화는 산화 과정을 통해 5-히드록시메틸사이토신(5hmC), 5-포르밀사이토신(5fC), 5-카르복실사이토신(5caC)으로 변환되고, 후자 2개는 최종적으로 티민 DNA 글리코실라제(TDG) 및 시토신 복원을 위한 염기 제거 복구 효소(BER)에 의해 뉴클레오시드에서 절단된다.[50] TDG를 녹아웃한 실험에서 5hmC에는 통계적으로 유의미한 변화가 없었지만, 5fC는 2배 증가했다.[51]
5mC, 5hmC, 5fC로의 산화 반응은 TET(Ten-eleven translocation) 패밀리 디옥시게나제를 통해 발생한다. 이 효소는 5mC를 우선적으로 처리하며, TET2에서 5hmC 및 5fC 변환의 초기 반응 속도는 4.9~7.6배 느려진다.[52] TET에는 보조 인자로서 Fe(II), 기질로서 산소 및 α-케토글루타르산(α-KG)이 필요하며, 후자의 기질은 이소구연산 탈수소효소(IDH)에 의해 이소구연산으로부터 생성된다.[53] 악성 종양(암세포)에서는 α-KG와 경쟁하는 2-히드록시글루타레이트(2HG)를 생성하여 TET 활성을 저하시킴으로써 5mC에서 5hmC로의 변환을 저하시키는 가능성이 보고되었다.[54]
"후성적 연령"은 연령과 DNA 메틸화 수준 간의 관계를 나타낸다.[59] "clock CpG"라고 불리는 특정 CpG 영역의 DNA 메틸화 수준과 특정 연령대 집단의 게놈 전체 메틸화율을 회귀하는 알고리즘을 결합하여 후성적 연령 예측이 가능하다. 젊은이(0~20세)의 경우 DNA 메틸화의 변화는 발달과 성장이 진행됨에 따라 더 빠른 속도로 발생하며, 노년기에는 변화가 느려지기 시작한다.
후성적 연령의 추정 방법은 여러 가지가 제안되었다. "Horvath 시계"는 여러 조직 유래의 353개의 CpG 세트를 측정한다. 이 세트에서 절반은 연령과 양의 상관관계를 가지며, 나머지 절반은 후성적 연령을 추정하기 위해 음의 상관관계를 가진다.[60] "Hannum 시계"는 성인의 혈액 샘플을 사용하여 71개의 CpG 사이트의 직교 기반으로 연령을 계산한다.[61] DNAm PhenoAge로 알려진 "Levine 시계"는 513개의 CpG 사이트에 의존하며, 사망률과 수명을 예측하는 데 있어 다른 연령 추정 기법보다 높은 점수를 얻었지만, 비혈액 조직에는 편향을 보인다.[62] 또한, ELOVL2 유전자라는 하나의 CpG만의 메틸화 상태를 기반으로 한 연령 추정기가 보고되었다.[63] 연령 추정을 통해 5mC 메틸화 마커를 기반으로 개인이 영향을 받을 수 있는 연령 관련 상태의 예상으로부터 수명을 예측할 수 있다.
7. 1. 암
DNA는 암에서 과도하게 메틸화되어 과메틸화되거나, 과소 메틸화되어 저메틸화될 수 있다.[22] 유전자 프로모터와 겹치는 CpG 섬은 ''de novo'' 메틸화되어 종양 억제와 관련된 유전자의 비정상적인 불활성화를 초래한다.[23] 종양과 정상 조직을 비교했을 때, 종양은 메틸전이효소 DNMT1, DNMT3A, 그리고 DNMT3B의 수치가 높았으며, 이들은 모두 암에서 5mC의 비정상적인 수준과 관련이 있다.[16]위성 DNA, Alu 배열, 그리고 긴 산재 반복 서열(LINE)을 포함한 게놈의 반복 서열은 암에서 종종 저메틸화된 것으로 나타나 침묵된 유전자의 발현을 초래하며, 그 수준은 종양 진행의 중요한 지표이다.[22] 과메틸화와 저메틸화 사이에는 연관성이 있다는 가설이 제기되었다. DNA 메틸전이효소의 과도한 활성으로 비정상적인 ''de novo'' 5mC 메틸화가 생성되면 메틸화 제거로 보상될 수 있다. 그러나 메틸화 제거는 비효율적이어서 게놈 전체의 저메틸화를 초과하게 된다. 반대의 경우도 가능하다. 저메틸화의 과발현은 게놈 전체의 과메틸화에 의해 침묵될 수 있다.[22]
암의 특징적인 능력은 암세포와 종양 미세 환경 내의 주변 종양 연관 기질 모두에서 5mC를 변경하는 후성 유전적 변화를 통해 획득될 가능성이 높다.[24] 항암제 시스플라틴은 5mC와 반응하는 것으로 보고되었다.[25]
참조
[1]
논문
TET-mediated active DNA demethylation: mechanism, function and beyond
2017-05-30
[2]
서적
Physiological Chemistry
https://books.google[...]
Williams & Wilkins Company/
[3]
논문
The discovery of 5-methyl-cytosine in tuberculinic acid, the nucleic acid of the ''Tubercle bacillus''
[4]
간행물
Nucleic Acids Are Not Boring Long Polymers of Only Four Types of Nucleotides: A Guided Tour
https://www.ncbi.nlm[...]
Landes Bioscience
[5]
논문
Microbial nucleic acids: the desoxypentose nucleic acids of avian tubercle bacilli and yeast
[6]
논문
The quantitative separation of purines, pyrimidines and nucleosides by paper chromatography
[7]
논문
Widespread occurrence of 5-methylcytosine in human coding and non-coding RNA
[8]
논문
Eukaryotic DNA methylation as an evolutionary device
[9]
논문
CpG-rich islands and the function of DNA methylation
1986-05-01
[10]
논문
5-Methylcytosine in eukaryotic DNA
1981-06-19
[11]
논문
Mutagenic consequences of cytosine alterations site-specifically embedded in the human genome
[12]
논문
Crosstalk between genetic and epigenetic information through cytosine deamination
[13]
논문
High sensitivity mapping of methylated cytosines
[14]
논문
Evolutionary Diversification of DNA Methyltransferases in Eukaryotic Genomes
https://academic.oup[...]
2005-04-01
[15]
논문
The DNA methyltransferase family: a versatile toolkit for epigenetic regulation
2018-02-01
[16]
논문
The human DNA methyltransferases (DNMTs) 1, 3a and 3b: coordinate mRNA expression in normal tissues and overexpression in tumors.
1999-06-01
[17]
논문
Structure of Dnmt3a bound to Dnmt3L suggests a model for de novo DNA methylation
2007-09-01
[18]
논문
Genome-wide profiling of 5-formylcytosine reveals its roles in epigenetic priming
2013-04-25
[19]
논문
Tet Proteins Can Convert 5-Methylcytosine to 5-Formylcytosine and 5-Carboxylcytosine
2011-09-02
[20]
논문
TET Family Proteins: Oxidation Activity, Interacting Molecules, and Functions in Diseases
2015-02-12
[21]
논문
Oncometabolite 2-Hydroxyglutarate Is a Competitive Inhibitor of α-Ketoglutarate-Dependent Dioxygenases
2011-01-18
[22]
논문
DNA hypomethylation in cancer cells
2009-12-01
[23]
논문
DNA Methylation Errors and Cancer
https://cancerres.aa[...]
1996-06-01
[24]
논문
Hallmarks of Cancer: The Next Generation
https://infoscience.[...]
2011-03-04
[25]
논문
Formation of Cisplatin Adducts with the Epigenetically-relevant Nucleobase 5-Methylcytosine
2020-10-23
[26]
논문
DNA methylation-based biomarkers and the epigenetic clock theory of ageing
2018-06-01
[27]
논문
DNA methylation age of human tissues and cell types
2013-12-10
[28]
논문
Genome-wide Methylation Profiles Reveal Quantitative Views of Human Aging Rates
2013-01-24
[29]
논문
An epigenetic biomarker of aging for lifespan and healthspan
2018-04-17
[30]
논문
Methylation of ELOVL2 gene as a new epigenetic marker of age
2012-01-01
[31]
논문
TET-mediated active DNA demethylation: mechanism, function and beyond
https://www.ncbi.nlm[...]
2017-09-01
[32]
서적
Physiological Chemistry
Williams & Wilkins Company/[http://www.amazon.com/Physiological-chemistry-text-book-manual-students/dp/1130145379/ref=sr_1_6?s=books&ie=UTF8&qid=1361261416&sr=1-6 RareBooksClub.com]
[33]
논문
The discovery of 5-methyl-cytosine in tuberculinic acid, the nucleic acid of the ''Tubercle bacillus''
[34]
간행물
Nucleic Acids Are Not Boring Long Polymers of Only Four Types of Nucleotides: A Guided Tour
http://www.ncbi.nlm.[...]
Landes Bioscience
[35]
논문
Microbial nucleic acids: the desoxypentose nucleic acids of avian tubercle bacilli and yeast
[36]
논문
The quantitative separation of purines, pyrimidines and nucleosides by paper chromatography
[37]
논문
Widespread occurrence of 5-methylcytosine in human coding and non-coding RNA
http://www.ncbi.nlm.[...]
[38]
논문
Eukaryotic DNA methylation as an evolutionary device
[39]
논문
CpG-rich islands and the function of DNA methylation
https://www.ncbi.nlm[...]
1986-05-15
[40]
논문
5-Methylcytosine in eukaryotic DNA
https://www.ncbi.nlm[...]
1981-06-19
[41]
논문
Mutagenic consequences of cytosine alterations site-specifically embedded in the human genome
https://genesenviron[...]
2016-09-01
[42]
논문
Crosstalk between genetic and epigenetic information through cytosine deamination
[43]
논문
High sensitivity mapping of methylated cytosines
[44]
논문
Evolutionary Diversification of DNA Methyltransferases in Eukaryotic Genomes
https://academic.oup[...]
2005-04-01
[45]
논문
The DNA methyltransferase family: a versatile toolkit for epigenetic regulation
2018-02-01
[46]
논문
The human DNA methyltransferases (DNMTs) 1, 3a and 3b: coordinate mRNA expression in normal tissues and overexpression in tumors.
1999-06-01
[47]
논문
TET-mediated active DNA demethylation: mechanism, function and beyond
2017-05-30
[48]
논문
Structure of Dnmt3a bound to Dnmt3L suggests a model for de novo DNA methylation
2007-09-01
[49]
논문
The DNA methyltransferase family: a versatile toolkit for epigenetic regulation
2018-02-01
[50]
논문
TET-mediated active DNA demethylation: mechanism, function and beyond
2017-05-30
[51]
논문
Genome-wide profiling of 5-formylcytosine reveals its roles in epigenetic priming
2013-04-25
[52]
논문
Tet Proteins Can Convert 5-Methylcytosine to 5-Formylcytosine and 5-Carboxylcytosine
2011-09-02
[53]
논문
TET Family Proteins: Oxidation Activity, Interacting Molecules, and Functions in Diseases
2015-02-12
[54]
논문
Oncometabolite 2-Hydroxyglutarate Is a Competitive Inhibitor of α-Ketoglutarate-Dependent Dioxygenases
2011-01-18
[55]
논문
DNA hypomethylation in cancer cells
2009-12-01
[56]
논문
DNA Methylation Errors and Cancer
https://cancerres.aa[...]
1996-06-01
[57]
논문
The human DNA methyltransferases (DNMTs) 1, 3a and 3b: coordinate mRNA expression in normal tissues and overexpression in tumors.
1999-06-01
[58]
논문
Hallmarks of Cancer: The Next Generation
https://www.cell.com[...]
2011-03-04
[59]
논문
DNA methylation-based biomarkers and the epigenetic clock theory of ageing
2018-06-01
[60]
논문
DNA methylation age of human tissues and cell types
2013-12-10
[61]
논문
Genome-wide Methylation Profiles Reveal Quantitative Views of Human Aging Rates
2013-01-24
[62]
논문
An epigenetic biomarker of aging for lifespan and healthspan
2018-04-17
[63]
논문
Methylation of ELOVL2 gene as a new epigenetic marker of age
2012-01-01
[64]
서적
Physiological Chemistry
https://books.google[...]
Williams & Wilkins Company/
[65]
논문
The discovery of 5-methyl-cytosine in tuberculinic acid, the nucleic acid of the ''Tubercle bacillus''
[66]
간행물
Nucleic Acids Are Not Boring Long Polymers of Only Four Types of Nucleotides: A Guided Tour
https://www.ncbi.nlm[...]
Landes Bioscience
[67]
논문
Microbial nucleic acids: the desoxypentose nucleic acids of avian tubercle bacilli and yeast
https://archive.org/[...]
[68]
논문
The quantitative separation of purines, pyrimidines and nucleosides by paper chromatography
https://archive.org/[...]
[69]
논문
Widespread occurrence of 5-methylcytosine in human coding and non-coding RNA
[70]
논문
The DNA methyltransferase family: a versatile toolkit for epigenetic regulation
2018-02-01
[71]
논문
Eukaryotic DNA methylation as an evolutionary device
[72]
논문
5-Methylcytosine in eukaryotic DNA
1981-06-19
[73]
논문
Mutagenic consequences of cytosine alterations site-specifically embedded in the human genome
[74]
논문
Crosstalk between genetic and epigenetic information through cytosine deamination
[75]
논문
High sensitivity mapping of methylated cytosines
본 사이트는 AI가 위키백과와 뉴스 기사,정부 간행물,학술 논문등을 바탕으로 정보를 가공하여 제공하는 백과사전형 서비스입니다.
모든 문서는 AI에 의해 자동 생성되며, CC BY-SA 4.0 라이선스에 따라 이용할 수 있습니다.
하지만, 위키백과나 뉴스 기사 자체에 오류, 부정확한 정보, 또는 가짜 뉴스가 포함될 수 있으며, AI는 이러한 내용을 완벽하게 걸러내지 못할 수 있습니다.
따라서 제공되는 정보에 일부 오류나 편향이 있을 수 있으므로, 중요한 정보는 반드시 다른 출처를 통해 교차 검증하시기 바랍니다.
문의하기 : help@durumis.com