삼산화 이비소
"오늘의AI위키"의 AI를 통해 더욱 풍부하고 폭넓은 지식 경험을 누리세요.
1. 개요
삼산화 이비소(As₂O₃)는 무미, 무취의 흰색 고체로, 양쪽성 산화물이며 물에 녹아 약산성을 띤다. 급성 전골수성 백혈병 치료에 사용되며, 과거에는 전통 의학에서 사용되거나 쥐약, 살충제 등의 독성 물질로 활용되었다. 비소 화합물로 산업적 용도로 사용되며, 제조 및 처리 과정에서 환경 오염을 유발하기도 한다. 섭취 시 치명적일 수 있으며, 만성 중독 시 피부암 등을 유발할 수 있다.
더 읽어볼만한 페이지
- 비소(III) 화합물 - 아비산
아비산은 삼산화 비소의 가수분해로 만들어지는 독성이 강한 약산성 삼각뿔형 분자로, 과거 살충제나 쥐약, 심지어 독살에도 사용되었으며 대한민국에서 집단 사망 사건을 일으키기도 했다. - 항암제 - 아자티오프린
아자티오프린은 장기 이식 거부 반응 예방 및 자가면역 질환 치료에 사용되는 면역억제제이며, 다양한 질환에 사용되지만 부작용과 유전자형에 따른 차이가 보고되었고, 사이클로스포린 등의 도입으로 사용이 일부 대체되었다. - 항암제 - 표적 치료
표적 치료는 세포 증식 관련 특정 분자를 억제하여 질병을 치료하는 방법으로, 단클론항체 개발 이후 저분자 의약품 및 항체의약품 등으로 발전하여 암, 자가면역질환 등 다양한 질환 치료에 활용되지만 부작용 발생 가능성도 존재한다. - 삼이산화물 - 삼산화 이질소
삼산화 이질소는 질소 산화물 중 하나로 질소의 산화수가 +3인 화합물이며, 저온에서 일산화 질소와 이산화 질소를 혼합하여 얻을 수 있고, 액체 상태에서는 진한 청색을 띠며, 고온에서는 분해되고 물에 녹으면 아질산으로 가수분해되는 특징을 가진 평면형 구조의 화합물이다. - 삼이산화물 - 산화 철(III)
산화 철(III)은 철과 산소의 화합물로, 여러 결정 구조의 동질이상 형태로 존재하며, 철광석인 적철광으로서 강철 생산 원료, 안료, 자기 기록 매체 등 산업과 의료 분야에 활용되는 다양한 화학 반응에 관여하는 물질이다.
| 삼산화 이비소 - [화학 물질]에 관한 문서 | |
|---|---|
| 일반 정보 | |
 | |
 | |
| 발음 | Ar se nik tri OKS id |
| 상품명 | 트라이세녹스, 기타 |
| CAS 등록번호 | 1327-53-3 |
| PubChem 식별자 | 261004 |
| DrugBank | DB01169 |
| ChemSpider ID | 452539 |
| UNII | S7V92P67HO |
| KEGG | C13619, D02106 |
| ChEMBL | 1200978 |
| 기타 이름 | 비소(III) 산화물 아비산 무수물 삼산화 이비소 비소 세스퀴옥사이드 아르센산 무수물 쥐약 흰색 비소 아쿠아 토파니 |
| IUPAC 이름 | 삼산화 이비소 |
| SMILES | O1[As]3O[As]2O[As](O3)O[As]1O2 |
| 표준 InChI | 1S/As2O3/c3-1-4-2(3)5-1 |
| 표준 InChIKey | GOLCXWYRSKYTSP-UHFFFAOYSA-N |
| 약리학 | |
| 투여 경로 | 정맥 주사 |
| ATC 코드 | L01XX27 |
| 단백질 결합 | 75% |
| 배설 | 소변 |
| 물리화학적 성질 | |
| 분자식 | As₂O₃ |
| 몰 질량 | 197.841 g/mol |
| 외형 | 흰색 고체 |
| 밀도 | 3.74 g/cm³ |
| 용해도 | 20 g/L (25 °C) |
| 용해도 (기타) | 묽은 산과 알칼리에는 녹지만, 유기 용매에는 녹지 않음. |
| 녹는점 | 312.2 °C |
| 끓는점 | 465 °C |
| pKa | 9.2 |
| 열화학 | |
| 표준 생성 엔탈피 | -657.4 kJ/mol |
| 결정 구조 | |
| 결정계 | 입방정계 (α) < 180°C, 단사정계 (β) > 180°C |
| 쌍극자 모멘트 | 0 |
| 위험성 | |
| 신호어 | 위험 |
| EU 분류 | 부식성, 맹독성, 유해, 환경 위험성 |
| 주요 위험성 | 맹독성, 유해 |
| 인화점 | 불연성 |
| 법적 규제 현황 | |
| 대한민국 | 전문의약품 |
| 오스트레일리아 | S4 |
| 미국 | Rx-only |
| 유럽 연합 | Rx-only |
| 임신 위험도 (오스트레일리아) | X |
| 세계 보건 기구 필수 의약품 목록 | 등재됨 |
| 관련 화합물 | |
| 관련 음이온 | 삼플루오르화 비소 |
| 관련 양이온 | 삼산화 인, 삼산화 안티모니 |
| 기타 화합물 | 오산화 비소, 아비산 |
2. 성질
삼산화 이비소는 무미, 무취의 흰색 분말 형태의 고체이다.[23] 양쪽성 산화물로 산과 염기 모두와 반응한다.[22] 물에 녹으면 아비산(As(OH)₃)이 되어 약산성을 나타낸다.[22][23]
삼산화 이비소는 t(15;17) 전위 또는 PML/RAR-알파 유전자 발현이 특징인 급성 전골수성 백혈병(APL) 치료에 사용된다.[1][2][13] 특히, 트레티노인과 병용하여 새로 진단된 저위험 급성 전골수성 백혈병 환자 치료에 사용하며, 레티노이드 및 안트라사이클린 화학 요법에 반응하지 않거나 재발한 환자의 관해 유도 및 공고요법에도 사용된다.[1][2][13][7] 전-트랜스 레티노산(ATRA)에 반응하지 않는 경우와 새로 진단된 사례의 초기 치료에 모두 사용 가능하다.[7] 초기 치료에는 삼산화 이비소와 전-트랜스 레티노산(ATRA)의 병용 요법이 포함될 수 있다.[14] 효능은 경구 투여가 가능하고 더 저렴한 웅황/청대와 유사한 것으로 보인다.[15]
아비산염을 생성하기에 알칼리 용액에 쉽게 녹지만, 산에서는 용해도가 낮다. 하지만 염산에는 녹는다.[22]
무수 HF 및 HCl과 반응하여 AsF3와 삼염화물을 생성한다.[23]
:As2O3 + 6 HX → 2 AsX3 + 3 H2O (X = F, Cl)
오존, 과산화 수소, 질산과 같은 강력한 산화제와 반응하여 오산화 비소(As₂O₅) 또는 그에 해당하는 산을 생성한다.[23]
:2 HNO₃ + As₂O₃ + 2 H₂O → 2 H₃AsO₄ + N₂O₃
산화에 대한 저항성은 삼산화 인과는 다르게 오산화 인으로 쉽게 연소되지 않는다.
환원 반응은 조건에 따라 원소 비소 또는 아르신(AsH₃)을 생성한다.[23]
:As₂O₃ + 6 Zn + 12 HNO₃ → 2 AsH₃ + 6 Zn(NO₃)₂ + 3 H₂O
이 반응은 마쉬 검출법에 사용된다.
다량 섭취했을 경우, 급성 신부전으로 사망에 이를 수도 있다. 독성에 대한 자세한 내용은 비소 항목을 참조할수 있다. 가장 간단한 해독법은, 구토시켜 독물이 흡수되는 것을 막는 것이다.
3. 용도
삼산화 이비소는 레티노산 수용체 알파의 프로테아좀 분해를 촉진하고, 단백질을 핵 기질로 이동시키며, 유비퀴틴화를 증가시켜 작용한다.[16] 이러한 사용법은 1970년대 중국 연구원 장팅둥과 동료들이 발견했으며,[17] 2000년 미국에서 백혈병 치료제로 승인되었다.[18]
과거에는 전통 중국 의학에서 ''피솽''()으로 알려져 사용되었으며, 동종 요법에서는 아르세니쿰 알붐이라고 불린다. 일부 특허 의약품 (파울러 용액 등)에는 산화 비소의 유도체가 포함되어 있었다.[20] 아비산은 독성이 강하지만, 무기 비소 화합물은 "아세아환[34]"이나 "포울러 용액(Fowler's solution)[35]" 등의 처방으로 악성 종양이나 피부병의 한약으로 사용되어 왔다. 유기 비소 화합물인 살바르산은 매독 치료에 사용되었으나, 현재는 사용되지 않는다. 히포크라테스가 피부병에 사용했다는 기록이 있으며, 근현대에도 항암제 등의 요법이 발전하기 전까지는 백혈병의 유일한 치료제였다. 그러나 부작용으로 만성 비소 중독이나 암에 걸리는 경우가 많아 점차 쇠퇴했다.
최근에는 레티노산 저항성의 급성 전골수성 백혈병 치료약으로 아비산 제제가 2004년 10월 후생노동성에 승인되었다.
삼산화 이비소는 산업적 용도로 임산물 전구체, 무색 유리 생산, 전자 제품 등에 사용된다.[11] 비소의 주요 화합물로서, 원소 비소, 비소 합금, 비소화물 반도체의 전구체이다. 대량의 비소 기반 화합물인 아비산나트륨과 카코딜산나트륨은 삼산화 이비소에서 파생된다.
다양한 응용 분야에서 비소의 독성을 활용하며, 산화물을 목재 방부제로 사용한다. 삼산화 이비소에서 파생된 비산구리는 미국과 말레이시아에서 대규모로 목재 방부제로 사용되지만, 이러한 물질은 세계 여러 지역에서 금지되어 있다. 이 관행은 여전히 논란의 대상이다.[11] 아세트산구리(II)와 함께 삼산화 이비소는 페인트 및 살서제로 사용되는 파리 그린으로 알려진 생생한 안료를 생성한다.
독성을 이용하여 쥐약, 살충제, 농약 등에 사용되었으나, 안전성 및 환경 문제로 인해 사용은 감소 추세에 있다. 공업적으로 금속 비소 및 비소 화합물을 제조할 때의 원료 (전구체)가 된다.
3. 1. 의학적 용도
삼산화 이비소는 t(15;17) 전위 또는 PML/RAR-알파 유전자 발현이 특징인 급성 전골수성 백혈병(APL) 치료에 사용된다.[1][2][13] 특히, 트레티노인과 병용하여 새로 진단된 저위험 급성 전골수성 백혈병 환자 치료에 사용하며, 레티노이드 및 안트라사이클린 화학 요법에 반응하지 않거나 재발한 환자의 관해 유도 및 공고요법에도 사용된다.[1][2][13][7] 전-트랜스 레티노산(ATRA)에 반응하지 않는 경우와 새로 진단된 사례의 초기 치료에 모두 사용 가능하다.[7] 초기 치료에는 삼산화 이비소와 전-트랜스 레티노산(ATRA)의 병용 요법이 포함될 수 있다.[14] 효능은 경구 투여가 가능하고 더 저렴한 웅황/청대와 유사한 것으로 보인다.[15]
삼산화 이비소는 레티노산 수용체 알파의 프로테아좀 분해를 촉진하고, 단백질을 핵 기질로 이동시키며, 유비퀴틴화를 증가시켜 작용한다.[16] 이러한 사용법은 1970년대 중국 연구원 장팅둥과 동료들이 발견했으며,[17] 2000년 미국에서 백혈병 치료제로 승인되었다.[18]
과거에는 전통 중국 의학에서 ''피솽''()으로 알려져 사용되었으며, 동종 요법에서는 아르세니쿰 알붐이라고 불린다. 일부 특허 의약품 (파울러 용액 등)에는 산화 비소의 유도체가 포함되어 있었다.[20] 아비산은 독성이 강하지만, 무기 비소 화합물은 "아세아환[34]"이나 "포울러 용액(Fowler's solution)[35]" 등의 처방으로 악성 종양이나 피부병의 한약으로 사용되어 왔다. 유기 비소 화합물인 살바르산은 매독 치료에 사용되었으나, 현재는 사용되지 않는다. 히포크라테스가 피부병에 사용했다는 기록이 있으며, 근현대에도 항암제 등의 요법이 발전하기 전까지는 백혈병의 유일한 치료제였다. 그러나 부작용으로 만성 비소 중독이나 암에 걸리는 경우가 많아 점차 쇠퇴했다.
최근에는 레티노산 저항성의 급성 전골수성 백혈병 치료약으로 아비산 제제가 2004년 10월 후생노동성에 승인되었다.
3. 2. 산업적 용도
삼산화 이비소는 산업적 용도로 임산물 전구체, 무색 유리 생산, 전자 제품 등에 사용된다.[11] 비소의 주요 화합물로서, 원소 비소, 비소 합금, 비소화물 반도체의 전구체이다. 대량의 비소 기반 화합물인 아비산나트륨과 카코딜산나트륨은 삼산화 이비소에서 파생된다.
다양한 응용 분야에서 비소의 독성을 활용하며, 산화물을 목재 방부제로 사용한다. 삼산화 이비소에서 파생된 비산구리는 미국과 말레이시아에서 대규모로 목재 방부제로 사용되지만, 이러한 물질은 세계 여러 지역에서 금지되어 있다. 이 관행은 여전히 논란의 대상이다.[11] 아세트산구리(II)와 함께 삼산화 이비소는 페인트 및 살서제로 사용되는 파리 그린으로 알려진 생생한 안료를 생성한다.
독성을 이용하여 쥐약, 살충제, 농약 등에 사용되었으나, 안전성 및 환경 문제로 인해 사용은 감소 추세에 있다. 공업적으로 금속 비소 및 비소 화합물을 제조할 때의 원료 (전구체)가 된다.
4. 독성 및 위험성
삼산화 이비소는 다른 무기 비소 화합물과 마찬가지로 생물체에 유독하다. 소화 기관에 의해 쉽게 흡수되며, 0.1그램만 섭취해도 치명적일 수 있다.[11]
만성 비소 중독은 비소증으로 알려져 있다. 이 질환은 제련소 작업자, 식수에 높은 수준의 비소(0.3~0.4ppm)가 포함된 인구, 그리고 비소 기반 제약으로 장기간 치료를 받은 환자에게 영향을 미친다. 식수나 의료 치료로서 삼산화 이비소를 장기간 섭취하면 피부암을 유발할 수 있다. 구리 주조 공장의 직원이나 이웃으로서 삼산화 비소 먼지에 노출된 여성에 대한 한 연구에서 생식 문제(유산 발생률 증가, 저체중 출생, 선천적 기형)도 나타났다.
대한민국 산업안전보건법에서는 무기 비소 화합물의 작업장 허용 노출 기준을 0.010mg/m3로 규정하고 있다.
4. 1. 독성 이용 사례
비소의 독성은 방대한 문헌의 주제이다.[26][27][28] "이와미 은산"은 당시의 쥐약, 이른바 쥐덫의 판매명이었으며, 시대극에서도 익숙한 독약으로 등장하지만, 그 실체는 삼산화 이비소이다. "이와미 은산 쥐덫"이라고도 불린다. 에도 서민들에게 널리 사용되었기 때문에, 독살의 수단으로도 이용되었다.16세기경부터 유럽에서도 독살에 이용되었다. 무미무취에 수용성이 높고, 검출할 수단이 없었기 때문에, 와인이나 맥주에 혼합하여 마시게 함으로써, 당시로서는 완전 범죄에 가까운 범행을 가능하게 했다. 프랑스 등에서는, 유산 상속과 관련된 소송에서 종종 사용되었기 때문에 "유산 상속 독" 등으로도 불렸다. 나폴레옹도 삼산화 이비소에 의한 비소 중독으로 사망했다고 알려져 있다.
5. 환경 문제
제련 및 관련 광석 처리 과정에서 종종 삼산화 이비소가 생성되는데, 이는 환경에 위험을 초래한다. 예를 들어, 캐나다의 자이언트 광산은 상당량의 비소철석에 오염된 금광석을 처리했다. 일본 미야자키현 다카치호정에 있었던 토로쿠 광산에서는 비소산 제조로 광해가 발생하여 다수의 사망자가 나왔다. 광산을 경영하던 회사는 재판에서 책임을 전혀 인정하지 않고, 최종적으로 화해금을 지불하는 것으로 피해자와 화해했다. → 토로쿠 비소 공해 참조.
6. 구조
800 °C 이하의 액체 및 기체 상태에서 삼산화 이비소는 As₄O₆의 화학식을 가지며, P₄O₆와 동일한 구조를 갖는다.[24] 800 °C 이상에서는 As₄O₆가 분자 As₂O₃으로 현저하게 해리되며, 이는 N₂O₃와 동일한 구조를 취한다.[24]
고체 상태에서는 세 가지 형태(다형체)가 알려져 있다.[24] 고온 (> 110 °C)에서는 분자 As₄O₆을 포함하는 입방형 As₄O₆이, 그리고 두 개의 관련 중합체 형태가 존재한다.[24] 이 중합체는 모두 단사정계 결정으로 결정화되며, O 원자를 공유하는 삼각뿔형 AsO₃ 단위의 시트를 특징으로 한다.[25]
(입방)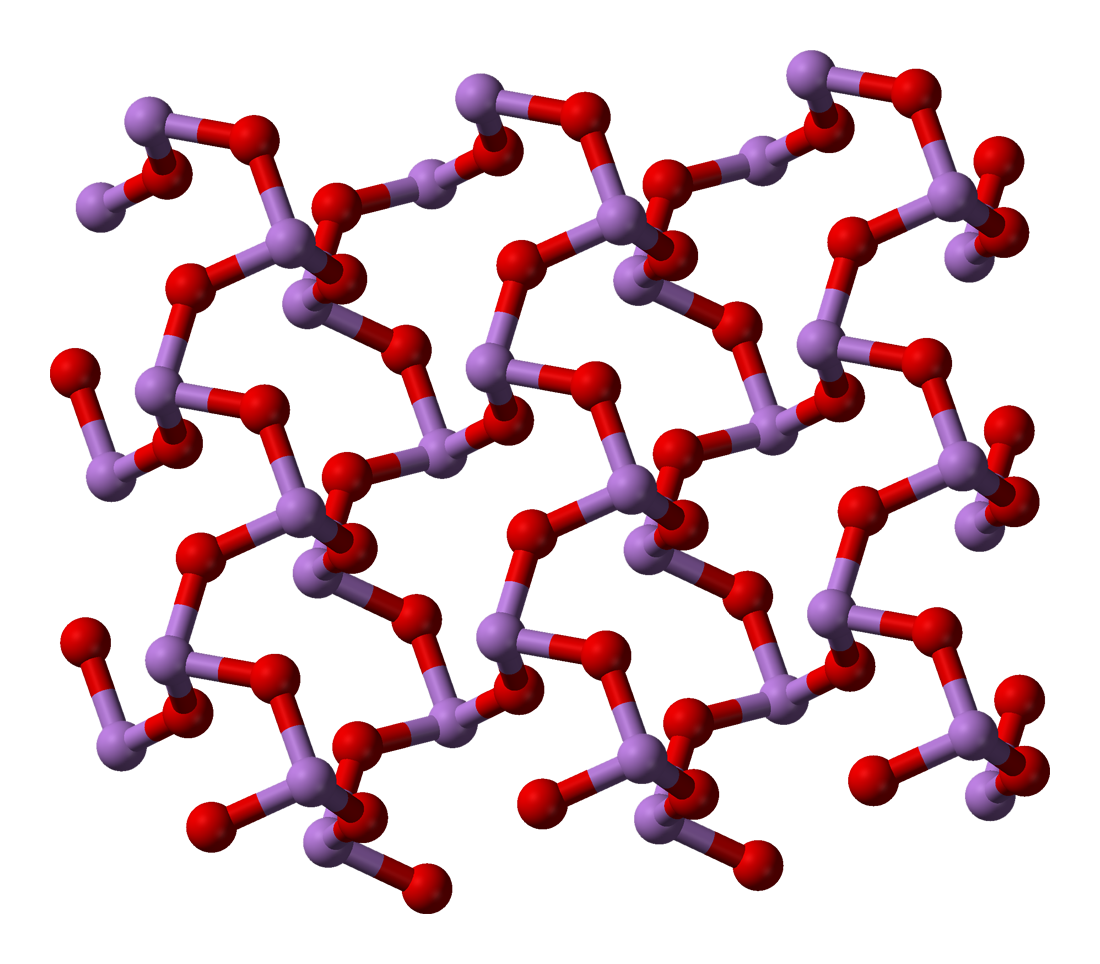
(단사정계)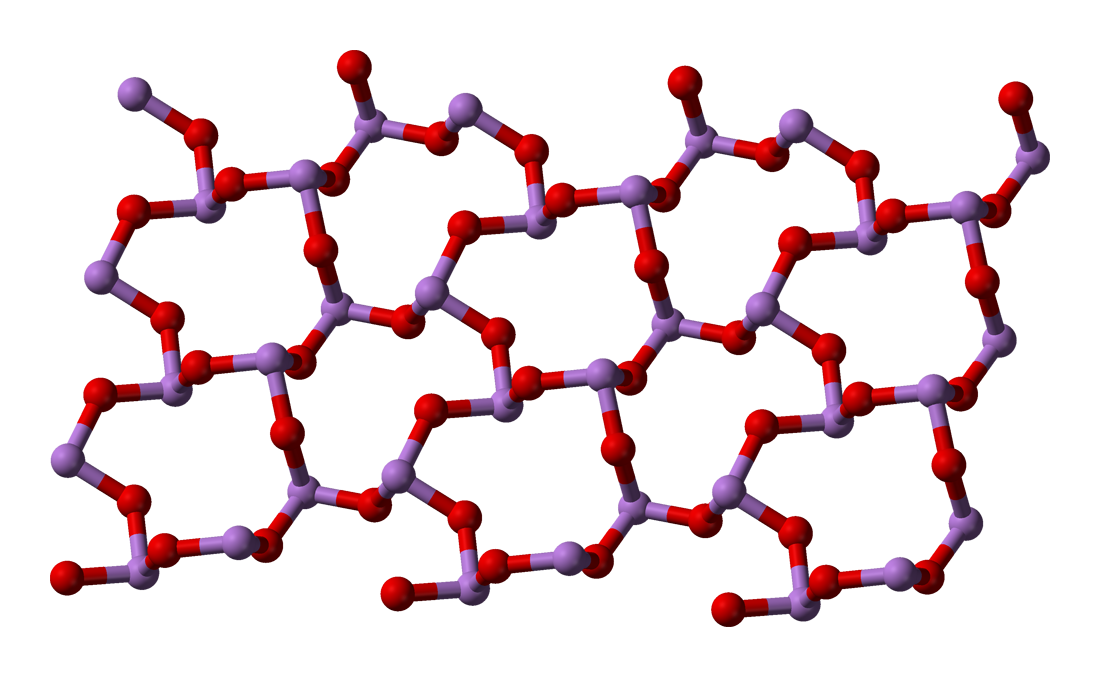
(단사정계)
7. 제조
삼산화 이비소는 공기중에서 비소 및 비소 함유 광물의 산화(연소)를 통해 생성될 수 있다. 황화비소 로스팅이 그 예시이다.[21]
:2 As2S3 + 9 O2 → 2 As2O3 + 6 SO2
대부분의 산화 비소는 다른 광석 처리 과정의 휘발성 부산물로 얻어진다. 금과 구리를 함유한 광석의 흔한 불순물인 자류철석은 공기 중에서 가열하면 삼산화 이비소를 방출하며, 이러한 광물의 처리로 인해 수많은 중독 사례가 발생했다.[21] 광산이 폐쇄된 후 남은 삼산화물 폐기물은 자이언트 광산의 경우처럼 환경적 위험을 초래한다. 중국에서만 의도적으로 비소 광석을 채굴한다.[11]
실험실에서는 삼염화 비소의 가수분해로 제조한다:[23]
:2 AsCl3 + 3 H2O → As2O3 + 6 HCl
삼산화 이비소(As2O3)는 두 가지 광물, 백비석(입방정계)과 클로데타이트(단사정계)로 자연적으로 발생한다.
8. 관련 사건 및 논란
8. 1. 토로쿠 비소 공해
미야자키현 다카치호정에 있었던 토로쿠 광산에서는 비소산 제조로 광해가 발생하여 다수의 사망자가 나왔다. 광산을 경영하던 회사는 재판에서 책임을 전혀 인정하지 않았으나, 최종적으로 화해금을 지불하는 것으로 피해자와 화해했다.8. 2. 자이언트 광산 (캐나다)
8. 3. 슈타이어마르크 비소 섭취자
오스트리아 슈타이어마르크에는 치사량 이상의 삼산화 이비소를 섭취하고도 건강하게 살아남은, 소위 "슈타이어마르크의 비소 섭취자"들이 있었다.[29][30][31][32] 비소는 알프스 등 고지대에서 고된 작업을 가능하게 하는 것으로 여겨진다.[29][30][31][32] 비소의 독성은 방대한 문헌의 주제이다.[26][27][28]참조
[1]
웹사이트
Trisenox- arsenic trioxide injection, solution
https://dailymed.nlm[...]
2024-02-03
[2]
웹사이트
Trisenox EPAR
https://www.ema.euro[...]
2024-02-03
[3]
웹사이트
Chemical of the Week: Arsenic
http://scifun.chem.w[...]
University of Wisconsin-Madison Chemistry Dept.
2008-08-03
[4]
웹사이트
Safety Data Sheet
https://www.american[...]
American Elements
2022-01-04
[5]
서적
Biological Chemistry of Arsenic, Antimony and Bismuth
https://books.google[...]
John Wiley & Sons
2023-03-18
[6]
서적
Chemicals in the Aquatic Environment: Advanced Hazard Assessment
https://books.google[...]
Springer Science & Business Media
2023-03-18
[7]
웹사이트
Arsenic Trioxide Monograph for Professionals
https://www.drugs.co[...]
2019-11-15
[8]
서적
British national formulary : BNF 76
Pharmaceutical Press
2018
[9]
웹사이트
Arsenic trioxide (Trisenox) Use During Pregnancy
https://www.drugs.co[...]
2019-11-16
[10]
서적
The selection and use of essential medicines 2023: web annex A: World Health Organization model list of essential medicines: 23rd list (2023)
World Health Organization
[11]
간행물
Arsenic and Arsenic Compounds
[12]
서적
Consolidated List of Products Whose Consumption And/or Sale Have Been Banned, Withdrawn, Severely Restricted Or Not Approved by Governments: Chemicals
https://www.un.org/e[...]
United Nations Publications
2009
[13]
웹사이트
Drug Approval Package: Trisenox (Arsenic Trioxide) NDA #21-248
https://www.accessda[...]
2024-02-03
[14]
논문
How acute promyelocytic leukaemia revived arsenic
2002-09
[15]
웹사이트
Proposal for the inclusion of arsenic therapies in the WHO Model List of Essential Medicines for the treatment of acute promyelocytic leukemia.
https://www.who.int/[...]
2019-11-15
[16]
논문
Arsenic-induced PML targeting onto nuclear bodies: implications for the treatment of acute promyelocytic leukemia
1997-04
[17]
논문
A drug from poison: how the therapeutic effect of arsenic trioxide on acute promyelocytic leukemia was discovered
2013-06
[18]
논문
Developing new drugs from annals of Chinese medicine
[19]
논문
Oral arsenic trioxide in the treatment of relapsed acute promyelocytic leukemia
2003-07
[20]
서적
Medicinal Organometallic Chemistry
[21]
웹사이트
Giant Mine – Northwest Territories Region – Indian and Northern Affairs Canada
http://nwt-tno.inac-[...]
2007-08-28
[22]
서적
Chemistry of the Elements
Butterworth-Heinemann
1997
[23]
서적
Handbook of Preparative Inorganic Chemistry
Academic Press
1963
[24]
서적
Structural Inorganic Chemistry
Oxford University Press
1984
[25]
서적
Inorganic Chemistry
Academic Press
[26]
웹사이트
Stanton v Benzler 9716830
http://caselaw.lp.fi[...]
U.S. 9th Circuit Court of Appeals
2008-06-09
[27]
서적
The Elements of Murder: A History of Poison
[[Oxford University Press]]
[28]
서적
[[Madame Bovary]]
[29]
뉴스
Arsenic Eaters
https://www.nytimes.[...]
2018-07-27
[30]
서적
Arsenik. Seine Geschichte in Österreich
Kleinmayr
[31]
논문
The arsenic eaters of Styria: a different picture of people who were chronically exposed to arsenic
[32]
서적
The Arsenic Century
https://archive.org/[...]
[[Oxford University Press]]
[33]
문서
Pradyot Patnaik. ''Handbook of Inorganic Chemicals''. McGraw-Hill, 2002, ISBN 0-07-049439-8
[34]
문서
三酸化二ヒ素を配合した[[丸剤|丸薬]]。[[疥癬]]などの皮膚病や梅毒の治療に使用。日本では昭和30年代半ばまで使用されていた。アジア丸、asiatic pillとも書く。[https://twitter.com/fluor_doublet/status/1559195547969368064 参考]
[35]
문서
{{仮リンク|亜ヒ酸カリウム|en|Potassium_arsenite}}[[水溶液]]。名称は開発した[[イギリス]]の医師Thomas Fowler(1736–1801)の名に因む。亜細亜丸同様の用途のほか、白血病の治療に用いられる事もあった。ホーレル水とも書く。
[36]
웹인용
Chemical of the Week: Arsenic
http://scifun.chem.w[...]
University of Wisconsin-Madison Chemistry Dept.
2008-08-03
본 사이트는 AI가 위키백과와 뉴스 기사,정부 간행물,학술 논문등을 바탕으로 정보를 가공하여 제공하는 백과사전형 서비스입니다.
모든 문서는 AI에 의해 자동 생성되며, CC BY-SA 4.0 라이선스에 따라 이용할 수 있습니다.
하지만, 위키백과나 뉴스 기사 자체에 오류, 부정확한 정보, 또는 가짜 뉴스가 포함될 수 있으며, AI는 이러한 내용을 완벽하게 걸러내지 못할 수 있습니다.
따라서 제공되는 정보에 일부 오류나 편향이 있을 수 있으므로, 중요한 정보는 반드시 다른 출처를 통해 교차 검증하시기 바랍니다.
문의하기 : help@durumis.com