표면장력
"오늘의AI위키"의 AI를 통해 더욱 풍부하고 폭넓은 지식 경험을 누리세요.
1. 개요
표면 장력은 액체 표면이 최소 면적을 가지려는 경향을 나타내는 현상으로, 단위 길이당 힘 또는 단위 면적당 에너지로 정의된다. 응집력으로 인해 발생하며, 액체 분자들이 서로 끌어당기는 힘과 표면 분자들이 내부로 당겨지는 힘의 불균형으로 인해 나타난다. 온도에 따라 감소하며, 불순물, 특히 계면활성제의 첨가에 의해 크게 영향을 받는다. 표면 장력은 물방울의 모양, 젖음성, 모세관 현상 등 다양한 현상을 결정하며, 두뇌 링 법, 빌헬미 평판법 등 다양한 측정 방법을 통해 측정할 수 있다.
더 읽어볼만한 페이지
- 표면과학 - 흡착
흡착은 엔트로피 감소를 동반하는 발열 반응으로, 흡착질이 흡착제 표면에 달라붙는 현상이며, 랭뮤어 및 BET 등온식 등으로 모델링하여 실리카겔, 제올라이트, 활성탄 등 다양한 흡착제를 활용, 기체 및 액체 분리, 정제, 저장 등에 사용되며 미래에는 수소 저장, 탄소 포집 등 다양한 분야에서 중요성이 커질 것으로 예상된다. - 표면과학 - 젖음
젖음은 액체와 고체 표면의 접촉 현상으로, 접촉각을 통해 정량적으로 측정되며, 표면 장력, 접착력, 응집력에 의해 결정되고 표면의 친수성, 소수성 등을 나타내는 데 중요한 역할을 한다. - 분자간 힘 - 소수성
소수성은 물을 기피하는 성질로, 생물학, 화학 등 다양한 분야에서 중요하게 다루어지며, 미셀 형성, 단백질 구조 형성, 초소수성 현상 등과 관련되어 자가 세척, 랩온어칩, 제약 분야 등에 응용된다. - 분자간 힘 - 반데르발스 힘
반데르발스 힘은 원자, 분자, 표면 간에 작용하는 인력으로, 입자들의 변동하는 극성화 상관관계에서 발생하며, 영구 다극자, 유도된 다극자, 순간 다극자 간 상호작용의 총합으로, 공유결합이나 이온결합보다 약하지만 물질의 물리적·화학적 특성, 생체 분자 상호작용, 도마뱀붙이의 벽면 부착 등에 중요한 역할을 한다. - 연속체역학 - 온도
온도는 물체의 뜨겁고 차가운 정도를 나타내는 물리량으로, 열역학적으로는 에너지 이동 방향으로 정의되며, 미시적으로는 분자 운동 에너지의 평균값으로 정의되고, 화학 반응 속도와 생명체에 큰 영향을 미친다. - 연속체역학 - 밀도
밀도는 단위 부피당 질량을 나타내는 물리량으로 질량을 부피로 나눈 값으로 계산되며, 온도와 압력에 따라 변하고, 진밀도, 겉보기밀도, 부피밀도, 탭밀도 등 여러 종류가 있고, 고대 그리스 시대부터 발전해왔다.
| 표면장력 | |
|---|---|
| 일반 정보 | |
 | |
| 기호 | γ, σ |
| SI 단위 | 킬로그램 매 초 제곱 (kg/s²) |
| CGS 단위 | 다인 매 센티미터 (dyn/cm) |
2. 정의
표면장력은 기호 ''γ''(또는 ''σ'' 또는 ''T'')로 나타내며, 단위 길이당 힘으로 측정된다. SI 단위는 미터당 뉴턴이지만, 센티미터당 다인이라는 cgs 단위도 사용된다.[6] 예를 들어,
표면장력은 힘 또는 에너지의 관점에서 정의할 수 있다.
- 힘의 관점: 액체의 표면 장력 γ는 단위 길이당 힘이다. 오른쪽 그림에서 세 개의 움직이지 않는 측면(검정색)으로 구성된 "U"자 모양의 직사각형 프레임과 오른쪽으로 미끄러질 수 있는 네 번째 움직이는 측면(파란색)이 있다. 표면 장력은 파란색 막대를 왼쪽으로 당긴다. 움직이는 측면을 고정하는 데 필요한 힘 F는 고정된 측면의 길이 L에 비례한다. 따라서 비율 F/L은 액체의 고유 특성(조성, 온도 등)에만 의존한다. 프레임 모양이 복잡하더라도, 움직이는 측면의 길이를 L, 미끄러지는 것을 막는 데 필요한 힘을 F라고 할 때, 비율 F/L은 모든 모양에 대해 동일하다. 따라서 표면 장력은 다음과 같이 정의된다.
:
:1/2인 이유는 막에 두 개의 면(두 개의 표면)이 있고 각각이 힘에 동등하게 기여하기 때문이다. 따라서 단일 면이 기여하는 힘은 γL = F/2이다.
- 에너지의 관점: 액체의 표면 장력 γ는 액체의 에너지 변화량과 액체의 표면적 변화량(에너지 변화를 야기한)의 비율이다. 이는 힘에 대한 이전 정의와 쉽게 관련될 수 있다.[7] 측면이 미끄러지기 ''시작하는 것을'' 막는 데 필요한 힘 F는 측면을 ''일정한 속도로 미끄러지는'' 상태로 유지하는 힘이기도 하다(뉴턴의 제2법칙). 측면이 오른쪽(힘이 가해지는 방향)으로 움직이면, 늘어난 액체의 표면적이 증가하고, 가해진 힘이 액체에 일을 한다. 즉, 표면적이 증가하면 필름의 에너지가 증가한다. 힘 F가 거리 Δx만큼 측면을 이동시키는 데 한 일은 W = FΔx이고, 동시에 필름의 총 면적은 ΔA = 2LΔx만큼 증가한다(액체에는 두 개의 면이 있으므로 계수 2가 곱해진다). 따라서 γ = (1/2)(F/L)의 분자와 분모에 Δx를 곱하면 다음을 얻는다.
:
:이 일 W는, 일반적인 논의에 의해, 퍼텐셜 에너지로 저장되는 것으로 해석된다. 따라서 표면 장력은 SI 단위계에서는 제곱미터당 줄(joules per square meter)로, CGS 단위계에서는 제곱센티미터당 에르그(ergs per cm2)로 측정할 수 있다. 역학적 계는 최소 퍼텐셜 에너지 상태를 찾으려고 하기 때문에, 자유로운 액체 방울은 주어진 부피에 대해 표면적이 최소인 구형을 자연스럽게 취한다.
단위 면적당 에너지 측정과 단위 길이당 힘 측정의 등가성은 차원 분석으로 증명할 수 있다.[13]
2. 1. 열역학적 정의
열역학에서 표면장력은 넓은 의미를 가진다.표면장력 σ영어은 온도 T와 장력 p에서 바뀌지 않는 상태에 있는 기브스 자유 에너지 G에 대한 면적 A의 편미분이다:
:
기브스 자유 에너지의 단위는 에너지 단위이고, 표면장력의 단위는 에너지/면적이다.
표면 장력의 정의에는 일반적으로 사용되는 세 가지 설명이 있다.[46]
- 맥스웰의 틀(ㄱ자 형태의 틀과 움직이는 막대 사이에 펼쳐진 액체 막)을 생각하자. 움직이는 막대에는 표면에 평행하게, 막을 수축시키는 방향으로 힘이 작용한다. 단위 길이당 이 수축력을 표면장력이라고 한다. 토머스 영이 시작한 사고방식이다.
- 마찬가지로 맥스웰의 틀의 움직이는 막대를 움직여 표면을 단위 면적만큼 증가시킬 때 필요한 일의 양. 이러한 생각은 A. 듀프레(1869)가 처음이라고 한다.
- 열역학에서는 자유 에너지를 사용하여 정의된다. 이러한 생각은 19세기 말부터 W. D. 허킨스(1917) 사이에 제시된 것으로 여겨진다. 이 경우 표면장력은 다음 식[47]으로 표현된다.
- :
- 여기서 는 깁스 자유 에너지, 는 표면적, 첨자는 온도 , 압력 일정의 열평형 상태를 나타낸다. 고체 표면에 대한 는 새로운 표면을 만드는 데 필요한 에너지를 나타내며, '''표면 에너지'''라고도 불린다.[48]
- 헬름홀츠 자유 에너지 를 사용하여 표현할 수도 있다.
- :
- 여기서 첨자는 온도 , 부피 일정의 열평형 상태를 나타낸다.
3. 원인 및 이론적 배경
분자간 힘은 분자와 분자 사이에 작용하는 인력이다. 액체 속의 분자는 모든 방향에서 다른 분자로부터 분자간 힘의 작용을 받아 자유 에너지가 낮은 상태에 있다. 반면, 표면에 있는 분자는 내부의 분자로부터는 작용을 받지만, 기체 분자로부터는 거의 작용을 받지 않는다. 즉, 표면에 있는 분자는 내부의 분자에 비해 큰 자유 에너지를 가지게 되고, 더 불안정한 상태에 있다고 할 수 있다. 그 결과, 표면을 가능한 한 작게 하려는 경향이 나타난다. Surface tension영어은 그 계면이 불안정할수록 커지기 때문에 계면활성제 등의 영향에 의해 변화한다.[2]
응집력 때문에, 표면에서 멀리 떨어진 분자는 인접한 액체 분자들에 의해 모든 방향에서 동일하게 당겨지므로, 알짜 힘은 0이 된다. 표면에 있는 분자들은 모든 면에 같은 분자가 있는 것이 아니므로 안쪽으로 당겨진다. 이는 일종의 내부 압력을 생성하고 액체 표면이 최소 면적으로 수축하게 만든다.[2]
물 분자의 응집력으로 인해 액체-공기 계면에서 표면과 평행한 장력도 존재하며, 이는 외부 힘을 저항한다.[2][3]
같은 종류의 분자 사이에 작용하는 인력을 응집력이라고 하고, 다른 종류의 분자 사이에 작용하는 인력을 부착력이라고 한다. 액체의 응집력과 용기 재료에 대한 부착력의 균형은 젖음성, 접촉각, 그리고 메니스커스의 모양을 결정한다. 응집력이 지배적인 경우(특히, 부착 에너지가 응집 에너지의 절반 미만인 경우) 젖음성이 낮고 메니스커스는 수직 벽에서 볼록하다(예: 유리 용기의 수은). 반면에 부착력이 지배적인 경우(부착 에너지가 응집 에너지의 절반 이상인 경우) 젖음성이 높고 메니스커스는 오목하다(예: 유리 용기의 물).
표면 장력은 액체 방울의 모양을 결정한다. 쉽게 변형될 수 있지만, 물방울은 표면층의 응집력 불균형에 의해 구형으로 당겨지는 경향이 있다. 다른 힘이 없다면, 거의 모든 액체의 방울은 대략 구형이 될 것이다. 구형은 라플라스 법칙에 따라 표면층의 필요한 "벽 장력"을 최소화한다.
표면 장력을 에너지 측면에서 보는 또 다른 방법이 있다. 이웃 분자와 접촉하는 분자는 혼자 있는 경우보다 에너지 상태가 낮다. 내부 분자는 가능한 한 많은 이웃을 가지고 있지만, 경계 분자는 (내부 분자와 비교하여) 이웃이 부족하므로 에너지가 더 높다. 액체가 에너지 상태를 최소화하려면, 에너지가 더 높은 경계 분자의 수를 최소화해야 한다. 경계 분자 수의 최소화는 최소 표면적을 초래한다.[5]
표면적 최소화의 결과로 표면은 매끄러운 모양을 취한다.
표면 장력을 이론적으로 구하려는 여러 가지 식이 있다.
- 토마스 영에 따르면 표면 장력은 반데르발스 상태 방정식에서의 내부 압력과 관계가 있다고 한다.[49][50]
- S. Sugden은 파라콜이라는 인자를 도입하여, 다음 식으로 표면 장력을 계산할 수 있다고 했다.[51]
:
: 여기서 D는 액체 밀도, d는 기체 밀도, M은 분자량이다. 단, OH기를 가지고 회합하는 물질은 적용 대상이 아니다.
:
:
: 여기서 ε = Qv/NA이고, NA는 아보가드로 수, ns는 단위 면적의 표면에 존재하는 분자 수, α는 화합물에 따라 0.25~0.6의 값을 취하는 보정 계수(예를 들어 물과 같은 OH기가 있는 물질에서는 α = 0.4)이다.
4. 성질
표면 장력은 온도, 불순물, 계면활성제의 영향을 받는다.
- 온도: 온도가 올라가면 분자 운동이 활발해져 분자 간 인력이 약해지기 때문에 표면 장력은 감소한다. 임계 온도에서는 표면 장력이 0이 된다.
- 불순물: 계면활성제와 같이 표면을 활성화시키는 물질은 표면 장력을 크게 감소시킨다.
- 계면활성제:
- 비누 거품은 계면활성제 덕분에 안정화된다. 계면활성제는 물의 표면 장력을 3배 이상 감소시킨다.
- 에멀션은 순수한 물에 기름 방울이 형성될 수 있도록 계면 장력을 감소시킨다.
- 용질: 용질은 표면과 용질의 성질에 따라 표면 장력에 서로 다른 영향을 미칠 수 있다.
용질의 영향[1]
| 영향 | 예시 (물-공기 계면) |
|---|---|
| 거의 또는 전혀 영향을 미치지 않음 | 설탕 |
| 표면 장력 증가 | 대부분의 무기 염 |
| 비단조 변화 | 대부분의 무기산 |
| 표면 장력의 점진적인 감소 | 대부분의 양친매성 물질 (예: 알코올) |
| 특정 임계 농도까지 표면 장력 감소, 그 이후에는 영향 없음 | 마이셀을 형성하는 계면활성제 |
깁스 흡착 등온식은 용질에 의한 표면 장력 변화를 나타내는 식이다.[1]
두 상 사이에 전위차가 있으면 표면 장력이 변하는 전기모세관 현상이 나타난다.[1]
4. 1. 온도 의존성
표면 장력은 온도에 따라 달라지는데, 온도가 증가하면 표면 장력은 감소하는 경향을 보인다. 이는 온도가 올라가면 분자 운동이 활발해져 분자 간 인력이 약해지기 때문이다. 임계 온도에서는 표면 장력이 0이 된다.[22][23][24]
온도에 따른 표면 장력 변화를 나타내는 대표적인 식은 다음과 같다.
:
여기서 는 물질의 몰 부피, 는 임계 온도, 는 거의 모든 물질에 대해 유효한 상수이다.[22] 물의 경우 = 18 ml/mol, = 647 K (374 °C)이다.[25]
:
는 각 액체에 대한 상수이고 은 경험적 인자로, 유기 액체의 경우 이다.
에트뵈시 식과 구겐하임-카타야마 식은 모두 임계 온도에서 표면 장력이 0이 된다는 점을 고려하지만, Ramay와 Shields는 임계 온도에서 실제와 일치하지 않는다고 지적했다.
4. 2. 기타 요인에 의한 변화
표면 장력은 불순물의 영향을 받는다. 특히 계면활성제와 같이 표면을 활성화시키는 물질은 표면 장력을 크게 감소시킨다.[1]- 비누 거품: 매우 작은 질량에 비해 매우 큰 표면적을 가진다. 순수한 물 속의 거품은 불안정하지만, 계면활성제를 첨가하면 안정화된다. (마랑고니 효과 참조) 계면활성제는 물의 표면 장력을 3배 이상 감소시킨다.[1]
- 에멀션: 표면 장력이 작용하는 콜로이드 분산액의 일종이다. 순수한 물에 분산된 미세한 기름 방울은 자발적으로 합쳐져 상 분리가 일어나지만, 계면활성제를 첨가하면 계면 장력이 감소하여 물에 기름 방울이 형성될 수 있다. 이렇게 형성된 기름 방울의 안정성은 여러 화학적 및 환경적 요인에 따라 달라진다.[1]
용질은 표면과 용질의 성질에 따라 표면 장력에 서로 다른 영향을 미칠 수 있다. 용질이 용매 표면에서의 농도는 용액 내부의 농도와 다를 수 있으며, 이러한 차이는 용질-용매 조합마다 다르다.[1]
용질의 영향[1]
| 영향 | 예시 (물-공기 계면) |
|---|---|
| 거의 또는 전혀 영향을 미치지 않음 | 설탕 |
| 표면 장력 증가 | 대부분의 무기 염 |
| 비단조 변화 | 대부분의 무기산 |
| 표면 장력의 점진적인 감소 | 대부분의 양친매성 물질 (예: 알코올) |
| 특정 임계 농도까지 표면 장력 감소, 그 이후에는 영향 없음 | 마이셀을 형성하는 계면활성제 |
깁스 흡착 등온식은 특정 가정을 전제로 유도되므로, 두 성분으로 이루어진 이상적인(매우 묽은) 용액에만 적용할 수 있다.[1]
두 상 사이에 전위차가 있으면 표면 장력이 변하는 전기모세관 현상이 나타난다.[1]
5. 여러 가지 현상
표면 장력은 일상생활과 자연 현상에서 다양하게 나타난다.
- A. 잎과 같은 왁스 표면에 빗방울이 구슬처럼 맺히는 현상이 있다. 물은 왁스에는 약하게 부착하지만 자신에게는 강하게 부착하기 때문에 물방울이 뭉쳐진다. 표면 장력은 구가 가장 작은 표면적 대 부피 비를 가지고 있기 때문에 물방울에 거의 구형의 모양을 준다.
- B. 액체 덩어리가 늘어날 때 방울이 형성된다. 수도꼭지에 달라붙어 질량이 증가하는 물은 표면 장력이 더 이상 방울을 수도꼭지에 연결할 수 없을 때까지 늘어난다. 그런 다음 분리되고 표면 장력에 의해 방울이 구형으로 형성된다. 수도꼭지에서 물줄기가 흐르면 낙하하는 동안 물줄기가 방울로 끊어진다. 중력이 물줄기를 늘이고, 그다음 표면 장력이 물줄기를 구형으로 쪼갠다.[8]
- C. 물보다 밀도가 높은 물체의 부력은 물체가 비젖는 성질을 가지고 있고 그 무게가 표면 장력으로 인한 힘에 의해 지탱될 만큼 충분히 작을 때 발생한다.[5] 예를 들어, 물장군은 표면 장력을 이용하여 연못 표면을 걸어 다닌다. 물장군 다리의 비젖는 성질은 다리의 분자와 물의 분자 사이에 인력이 없음을 의미한다. 따라서 다리가 물을 누르면 물의 표면 장력은 다리로 인한 변형에서 평평함을 회복하려고만 한다. 물의 이러한 거동은 물장군을 위로 밀어 올리므로 물이 지탱할 수 있을 만큼 질량이 작으면 물 표면에 서 있을 수 있다. 물의 표면은 탄성 필름처럼 작용한다. 곤충의 발은 물 표면에 움푹 들어간 자국을 만들어 표면적을 증가시키고,[9] 물의 표면 곡률(따라서 면적)을 최소화하려는 경향은 곤충의 발을 위로 밀어 올린다.

- D. 기름과 물(이 경우 물과 액체 왁스)의 분리는 서로 다른 액체 사이의 표면의 장력에 의해 발생한다. 이러한 유형의 표면 장력을 "계면 장력"이라고 하지만 화학적 원리는 동일하다.
- E. 와인의 눈물은 알코올 음료가 담긴 잔의 측면에 방울과 가는 물줄기가 형성되는 현상이다. 그 원인은 물과 에탄올의 서로 다른 표면 장력 사이의 복잡한 상호 작용이다. 에탄올에 의한 물의 표면 장력 변화와 에탄올이 물보다 더 빨리 증발하는 것의 결합에 의해 유도된다.
표면 장력은 계면활성제를 사용할 때 더욱 두드러지게 나타난다.
- 비누 거품은 매우 작은 질량에 비해 매우 큰 표면적을 가지고 있다. 순수한 물 속의 거품은 불안정하지만, 계면활성제를 첨가하면 거품이 안정화될 수 있다(마랑고니 효과 참조). 계면활성제는 실제로 물의 표면 장력을 3배 이상 감소시킨다.
- 에멀션은 표면 장력이 역할을 하는 일종의 콜로이드 분산액이다. 순수한 물에 분산된 미세한 기름 방울은 자발적으로 합쳐져 상 분리가 일어난다. 계면활성제를 첨가하면 계면 장력이 감소하고 물 매질(또는 그 반대)에 기름 방울이 형성될 수 있다.
5. 1. 젖음 (Wetting)
젖음은 고체 표면에 액체가 퍼지는 현상이다. 젖음성은 고체와 액체 사이의 상호작용, 즉 표면장력에 의해 결정된다.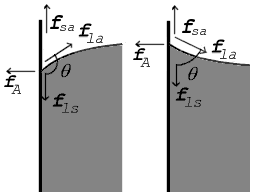
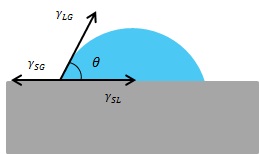
- '''접촉각''': 고체 표면과 액체 표면이 이루는 각을 접촉각()이라고 하며, 젖음성의 정도를 나타내는 척도로 사용된다.[60] 접촉각은 각 계면의 표면장력과 관련이 있으며, 표면장력이 큰 고체는 젖기 쉽고, 액체가 부착되었을 때 접촉각이 예각이 된다. 반대로, 표면장력이 작은 고체는 젖기 어렵고, 접촉각이 둔각이 된다.
- '''영의 방정식''': 접촉각과 각 계면(고체-기체, 액체-기체, 고체-액체)의 표면장력 사이의 관계를 나타내는 식은 다음과 같다.
:
::* :접촉각
::* :고체에 작용하는 표면장력
::* :액체에 작용하는 표면장력
::* :고체·액체 계면에 작용하는 계면장력
| 액체 | 고체 | 접촉각 |
|---|---|---|
| 물 | 소다석회 유리, 납 유리, 융용 실리카 | 0° |
| 에탄올, 디에틸 에테르, 사염화탄소, 글리세롤, 아세트산 | 소다석회 유리, 납 유리, 융용 실리카 | 0° |
| 물 | 파라핀 왁스 | 107° |
| 물 | 은 | 90° |
| 요오드화메틸 | 소다석회 유리 | 29° |
| 요오드화메틸 | 납 유리 | 30° |
| 요오드화메틸 | 융용 실리카 | 33° |
| 수은 | 소다석회 유리 | 140° |
5. 2. 모세관 현상
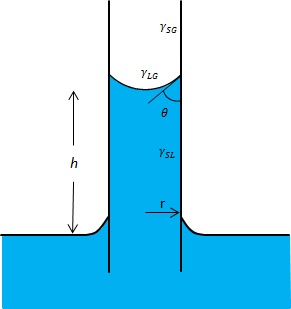
모세관 현상은 좁은 관(모세관) 속에서 액체 표면이 상승하거나 하강하는 현상이다. 이는 액체의 표면장력과 관 벽 사이의 부착력(또는 응집력)에 의해 발생한다.[13]thumb
관이 충분히 가늘고 액체의 벽에 대한 부착력이 충분히 강하면 표면 장력이 모세관 현상으로 유체를 관 위로 끌어올릴 수 있다.
모세관 현상은 영(Young)이 표면 장력의 존재를 밝히기 전부터 관찰되었던 현상이다. 모세관 현상이란 액체 속에 넣은 가는 관의 내부에서 액면이 외부의 자유 표면보다 상승(하강)하는 현상이다.
상승 높이모세관 내에서 액체가 상승하는 높이()는 다음 식으로 주어진다.
:
- : 액체가 들어올려지는 높이
- : 액체-공기 표면 장력
- : 액체의 밀도
- : 모세관의 반지름
- : 중력 가속도
- : 접촉각
즉, 이 작용은 액체가 고체 표면을 잘 적실수록 강하고, 또 틈이 좁을수록 강하다(상승의 경우). 유리 용기의 수은과 같이 가 90°보다 크면 액체는 들어올려지기보다는 내려간다.
5. 3. 물의 표면장력
물은 수소 결합에 의해 분자 간의 인력이 크기 때문에 다른 액체에 비해 표면 장력이 크다.[8] 물의 표면 장력을 감소시키는 간단한 실험을 할 수 있다. 바늘이 떠 있는 물에 계면활성제인 비눗물이 묻은 손가락을 넣으면 비누가 물의 표면 장력을 약화시키므로, 물 위에 떠 있던 바늘이 가라앉게 된다. 또한 비눗물과 접촉한 부분의 물의 표면 장력이 감소하면서 물 분자들이 인력이 강한 쪽으로 이동하므로, 바늘은 비눗물이 묻은 손가락으로부터 밀려난다.일반적인 물에서 볼 수 있는 표면 장력에 의한 현상은 다음과 같다.
- A. 잎과 같은 왁스 표면에 빗방울이 구슬처럼 맺히는 현상. 물은 왁스에는 약하게 부착하지만 자신에게는 강하게 부착하기 때문에 물방울이 뭉쳐진다. 표면 장력은 구가 가장 작은 표면적 대 부피 비를 가지고 있기 때문에 물방울에 거의 구형의 모양을 준다.
- B. 액체 덩어리가 늘어날 때 방울이 형성된다. 수도꼭지에 달라붙어 질량이 증가하는 물은 표면 장력이 더 이상 방울을 수도꼭지에 연결할 수 없을 때까지 늘어난다. 그런 다음 분리되고 표면 장력에 의해 방울이 구형으로 형성된다. 수도꼭지에서 물줄기가 흐르면 낙하하는 동안 물줄기가 방울로 끊어진다. 중력이 물줄기를 늘이고, 그다음 표면 장력이 물줄기를 구형으로 쪼갠다.[8]
- C. 물보다 밀도가 높은 물체의 부력은 물체가 비젖는 성질을 가지고 있고 그 무게가 표면 장력으로 인한 힘에 의해 지탱될 만큼 충분히 작을 때 발생한다.[5] 예를 들어, 물장군은 표면 장력을 이용하여 연못 표면을 걸어 다닌다. 물장군 다리의 비젖는 성질은 다리의 분자와 물의 분자 사이에 인력이 없음을 의미한다. 따라서 다리가 물을 누르면 물의 표면 장력은 다리로 인한 변형에서 평평함을 회복하려고만 한다. 물의 이러한 거동은 물장군을 위로 밀어 올리므로 물이 지탱할 수 있을 만큼 질량이 작으면 물 표면에 서 있을 수 있다. 물의 표면은 탄성 필름처럼 작용한다. 곤충의 발은 물 표면에 움푹 들어간 자국을 만들어 표면적을 증가시키고,[9] 물의 표면 곡률(따라서 면적)을 최소화하려는 경향은 곤충의 발을 위로 밀어 올린다.
- D. 기름과 물(이 경우 물과 액체 왁스)의 분리는 서로 다른 액체 사이의 표면의 장력에 의해 발생한다. 이러한 유형의 표면 장력을 "계면 장력"이라고 하지만 화학적 원리는 동일하다.
- E. 와인의 눈물은 알코올 음료가 담긴 잔의 측면에 방울과 가는 물줄기가 형성되는 현상이다. 그 원인은 물과 에탄올의 서로 다른 표면 장력 사이의 복잡한 상호 작용이다. 에탄올에 의한 물의 표면 장력 변화와 에탄올이 물보다 더 빨리 증발하는 것의 결합에 의해 유도된다.
5. 4. 물방울
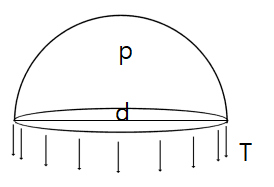
왼쪽 그림에서 표면장력을 T영어라고 하고 물방울 내부와 외부의 압력 차이를 p영어, 물방울 직경을 d영어라고 한다면, 표면장력에 의해 물방울의 잘라진 면의 원주에 작용하는 합력과 압력 차이에 의해 발생하는 힘이 평형을 이루기 때문에 이들의 관계를 다음과 같이 나타낼 수 있다.[63]
:
:
6. 측정 방법
표면장력은 다양한 현상으로 나타나기 때문에 측정 방법도 여러 가지가 있다. 어떤 방법이 최적인지는 측정 대상 액체의 성질, 장력을 측정하는 조건, 변형될 때 표면의 안정성에 따라 달라진다.
표면장력(surface tension영어)은 기호 γ (또는 σ 또는 T)로 나타내며, 단위 길이당 힘으로 측정된다. SI 단위는 미터당 뉴턴(N/m)이지만, 센티미터당 다인(dyn/cm)이라는 cgs 단위도 사용된다.[6] 예를 들어,
:
액체의 표면 장력 γ는 단위 길이당 힘으로 정의되는데, 이는 액체의 에너지 변화량과 액체의 표면적 변화량의 비율로도 나타낼 수 있다.[7] 역학적 계는 최소 퍼텐셜 에너지 상태를 찾으려고 하기 때문에, 자유로운 액체 방울은 주어진 부피에 대해 표면적이 최소인 구형을 자연스럽게 취한다.
표면장력 측정에는 두뇌 링 법(Du Noüy ring method), 빌헬미 평판법(Wilhelmy plate method), 회전 낙하법(Spinning drop method), 현수 낙하법(Pendant drop method), 기포압력법(Bubble pressure method), 액적 부피법(Drop volume method), 모세관 상승법(Capillary rise method), 스탈라그모미터법(Stalagmometric method), 정치 낙하법(Sessile drop method), 두뇌-패데이 법(Du Noüy–Padday method) 등 다양한 방법이 사용된다.[61]
몇 가지 측정 방법에 대한 추가적인 설명은 다음과 같다.
- 회전 낙하법(Spinning drop method): 낮은 계면 장력을 측정하는 데 적합하다. 두 상이 모두 회전하는 동안 무거운 상 내의 액적의 직경을 측정한다.
- 두뇌-패데이 법(Du Noüy–Padday method): 두뇌 링 법의 축소 버전으로, 링 대신 작은 직경의 금속 바늘을 사용하고 고감도 미량 저울을 사용하여 최대 인장력을 기록한다. 매우 작은 시료량(수십 마이크로리터까지)을 매우 높은 정밀도로, 최소 20초 이내에 측정할 수 있다는 장점이 있다.
- 부유 액적의 진동 주파수: 자기적으로 부유하는 액적의 자연 진동 주파수를 사용하여 초유체 4He의 표면 장력을 측정할 수 있다.
- 구형 및 반구형 액적의 공진 진동: 변조된 전기장에 의해 진동하는 구형 및 반구형 현수 액적의 공진 주파수를 측정하여 표면 장력과 점도를 평가한다.[31][32][33]
- 액적 반발법(Drop-bounce method): 분할 가능한 노즐 설계를 사용한 공기역학적 부양을 기반으로 한다. 안정적으로 부양된 액적을 플랫폼에 떨어뜨린 후, 시료는 변형되어 되튀어 오르며 표면적을 최소화하려고 하면서 공중에서 진동한다. 이 진동 거동을 통해 액체의 표면 장력과 점도를 측정할 수 있다.[34]
액체 방울이나 기포의 형태를 영-라플라스 방정식으로 근사하여 표면장력을 구하는 방법으로는 액적법, 매달린 방울법(펜던트 드롭법), 매달린 기포법(펜던트 버블법), 세실 기포법 등이 있다. 이러한 방법들은 액체 방울이나 기포가 정지해 있고 점성과 관성은 무시할 수 있다는 전제 조건이 필요하다.
최대 기포 압력법은 모세관에서 액체 속으로 기포를 밀어내는 데 필요한 압력으로부터 표면장력을 구하며, 액적 무게법은 기체 중의 모세관 바닥에 액체를 흘려 액체 방울을 성장시키고, 표면장력으로 지탱할 수 없게 되어 떨어지는 액체 방울의 무게로부터 표면장력을 구한다.
뒤 누이 원형 장력계는 젖음성이 좋은 원형 링을 액체 표면에서 들어 올리는 데 필요한 힘을 측정하며, 빌헬미 플레이트법은 젖음성이 좋은 얇은 판을 수직으로 물에 반만 담그고, 판에 작용하는 힘에서 판의 무게를 제외한 부분을 측정한다.
고체의 표면 에너지는 액체에 비해 측정이 어렵고, 얻어진 데이터의 정확도도 낮다.[48]
6. 1. 정적 측정법
표면장력계는 표면장력을 측정하는 기기이며, 정적 측정법에는 다음과 같은 방법들이 있다.- '''뒤 누이 원환법 (Du Noüy ring method)''': 표면에 링을 놓고 링을 들어 올리는 데 필요한 힘을 측정한다.[22] 젖음성은 이 측정 기술에 거의 영향을 미치지 않는다.
- '''빌헬미 평판법 (Wilhelmy plate method)''': 얇은 판을 액체에 수직으로 담갔을 때 판에 작용하는 힘을 측정한다. 장시간에 걸친 표면 장력 측정에 적합하다.
- '''정적 낙하법 (Sessile drop method)''': 기판 위에 액체 방울을 놓고 접촉각을 측정한다.[29]
- '''현수 낙하법 (Pendant drop method)''': 바늘 끝에 액체 방울을 매달아 그 형태를 측정한다. 고온 및 고압에서도 측정이 가능하다.
- '''최대 기포 압력법 (Bubble pressure method)''': 모세관을 통해 액체 속으로 기포를 밀어 넣는 데 필요한 압력을 측정한다.
- '''액적 부피법 (Drop volume method)''': 한 액체를 다른 액체에 펌핑하여 생성되는 액적 사이의 시간을 측정한다.
- '''모세관 상승법 (Capillary rise method)''': 모세관 내에서 액체가 상승하는 높이를 측정한다.[28]
6. 2. 동적 측정법
표면장력계를 사용하는 동적 측정법은 다음과 같다.- '''스탈라그모미터법(Stalagmometric method)''': 액체 방울의 무게를 측정한다.[28]
- '''진동 낙하법 (Oscillating drop method)''': 레일리가 발견한 방법으로 액체 방울의 진동 주파수를 측정하여 표면장력을 계산한다. 액체 방울(반지름 )의 제1진동 모드의 각진동수 는 점성을 무시하면 다음과 같다.[62]
:
7. 무차원 수
- 웨버 수 - 관성력과의 비
- 캐필러리 수 - 점성력과의 비
- 에오트뵈스 수 - 중력과의 비
참조
[1]
웹사이트
Surface Tension - an overview ScienceDirect Topics
https://www.scienced[...]
2021-12-30
[2]
웹사이트
Surface Tension (Water Properties) – USGS Water Science School
http://water.usgs.go[...]
US Geological Survey
2015-11-06
[3]
논문
The molecular mechanism of surface tension
https://michaelberry[...]
2020-07-08
[4]
서적
Physics, Volume 2
https://books.google[...]
John Wiley & Sons
2021-03-19
[5]
서적
Modern College Physics
https://archive.org/[...]
van Nostrand
[6]
웹사이트
MIT Lecture Notes on Surface Tension, lecture 1
http://web.mit.edu/1[...]
Massachusetts Institute of Technology
2004-04-00
[7]
웹사이트
Mechanical definition of surface tension
http://web.mit.edu/n[...]
MIT
2013-12-16
[8]
웹사이트
MIT Lecture Notes on Surface Tension, lecture 5
http://web.mit.edu/1[...]
Massachusetts Institute of Technology
2004-05-00
[9]
웹사이트
MIT Lecture Notes on Surface Tension, lecture 3
http://web.mit.edu/1[...]
Massachusetts Institute of Technology
2004-05-00
[10]
서적
Physics and Chemistry of Interfaces
Wiley
[11]
웹사이트
NP-complete Problems and Physical Reality
https://arxiv.org/ab[...]
2005-03-00
[12]
문서
In a mercury barometer, the upper liquid surface is an interface between the liquid and a vacuum containing some molecules of evaporated liquid.
[13]
서적
University Physics 2nd ed
Addison Wesley
[14]
서적
Capillarity and Wetting Phenomena—Drops, Bubbles, Pearls, Waves
Springer
[15]
간행물
The Scientific Papers of J. Willard Gibbs
Ox Bow Press
[16]
서적
Course of Theoretical Physics Volume 5: Statistical Physics I
Pergamon
1980
[17]
논문
Surface thermodynamics revisited
[18]
간행물
The thermodynamic theory of capillarity under the hypothesis of a continuous variation of density
[19]
간행물
Free energy of a nonuniform system. I. Interfacial free energy
[20]
간행물
New computational method in the theory of spinodal decomposition
[21]
Review article
Beyond Navier–Stokes equations: capillarity of ideal gas
https://www.research[...]
[22]
웹사이트
Surface Tension by the Ring Method (Du Nouy Method)
http://www.nikhef.nl[...]
PHYWE
2007-09-08
[23]
서적
The Physics and Chemistry of Surfaces, 3rd ed
Oxford University Press
[24]
웹사이트
Physical Properties Sources Index: Eötvös Constant
https://web.archive.[...]
2008-11-16
[25]
논문
International Tables of the Surface Tension of Water
https://web.archive.[...]
2017-07-13
[26]
서적
Physical Chemistry, 3rd ed
Prentice Hall
[27]
서적
Handbook of heterogeneous catalysis
Wiley-VCH, Weinheim
[28]
웹사이트
Surface Tension (physics lecture notes)
http://mysite.du.edu[...]
University of Denver
2007-09-08
[29]
웹사이트
Sessile Drop Method
http://www.dataphysi[...]
Dataphysics
2007-09-08
[30]
논문
Surface tension of liquid 4He as measured using the vibration modes of a levitated drop
[31]
논문
Droplet oscillations driven by an electric field
[32]
논문
Electrically Driven Resonant Oscillations of Pendant Hemispherical Liquid Droplet and Possibility to Evaluate the Surface Tension in Real Time
[33]
논문
Oscillations of a Hanging Liquid Drop, Driven by Interfacial Dielectric Force
[34]
논문
Novel Method for Surface Tension Measurement: the Drop-Bounce Method
2021-06-00
[35]
서적
Lange's Handbook of Chemistry (1967) 10th ed.
[36]
서적
Physical Chemistry of Surfaces
https://www.eng.uc.e[...]
Wiley-Interscience
1997-08-18
[37]
논문
On the Surface Tension of Liquid Helium II
[38]
논문
Activities and Surface Tension of Liquid AgCl-KCl Solutions
[39]
논문
Influence of Surface Reactions on the Interface Between Liquid Sodium and Molten Sodium Chloride + Calcium Chloride Mixtures
[40]
웹사이트
Revised Release on Surface Tension of Ordinary Water Substance
http://www.iapws.org[...]
2014-06-01
[41]
논문
Surface tension of seawater
http://dspace.mit.ed[...]
2014-11-01
[42]
논문
The composition of Standard Seawater and the definition of the Reference-Composition Salinity Scale
2008-01-01
[43]
기술보고서
Guideline on the Surface Tension of Seawater
http://www.iapws.org[...]
2019-10-01
[44]
서적
物理学辞典
培風館
2005-09-30
[45]
문서
井本、p.1
[46]
문서
井本、pp.1-18
[47]
문서
中島、p.17
[48]
서적
表面物性
共立出版
[49]
문서
ファンデルワールスの状態方程式#方程式
[50]
문서
井本、p.35
[51]
문서
井本、p.36
[52]
문서
井本、p.38
[53]
문서
井本、pp.40-48
[54]
문서
荻野、p.192
[55]
문서
中島、p.18
[56]
문서
中島、p.15
[57]
문서
荻野、p.7
[58]
문서
荻野、p.132
[59]
문서
荻野、p.133
[60]
문서
『物理学辞典』(三訂版)、1190頁。
[61]
서적
界面の物理と科学
丸善出版
[62]
문서
荻野、p.49
[63]
서적
토목기사 과년도 - 수리수문학
성안당
2015
[64]
서적
Lange's Handbook of Chemistry, 10th ed.
관련 사건 타임라인
( 최근 20개의 뉴스만 표기 됩니다. )
"물 위를 어떻게 달리지?"…소금쟁이 비밀 풀어낸 한국 로봇
본 사이트는 AI가 위키백과와 뉴스 기사,정부 간행물,학술 논문등을 바탕으로 정보를 가공하여 제공하는 백과사전형 서비스입니다.
모든 문서는 AI에 의해 자동 생성되며, CC BY-SA 4.0 라이선스에 따라 이용할 수 있습니다.
하지만, 위키백과나 뉴스 기사 자체에 오류, 부정확한 정보, 또는 가짜 뉴스가 포함될 수 있으며, AI는 이러한 내용을 완벽하게 걸러내지 못할 수 있습니다.
따라서 제공되는 정보에 일부 오류나 편향이 있을 수 있으므로, 중요한 정보는 반드시 다른 출처를 통해 교차 검증하시기 바랍니다.
문의하기 : help@durumis.com
