사이아노젠
"오늘의AI위키"의 AI를 통해 더욱 풍부하고 폭넓은 지식 경험을 누리세요.
1. 개요
사이아노젠은 두 개의 시아노기가 탄소 원자로 공유 결합된 구조(NCCN)를 가지는 무색 기체로, 특유의 냄새를 지닌다. 냉수와 반응하여 시안화 수소와 시안산을 생성하며, 에테르에 잘 녹고 염산과 반응하여 에틸렌디아민으로 환원된다. 산소와 혼합하여 연소 시 복숭아색 불꽃과 함께 고온을 내며, 고온에서 장시간 가열하면 중합체인 파라시안을 생성한다. 실험실에서는 시안화 수은 열분해, 구리(II) 염 용액에 시안화물 첨가, 오산화 이인에 의한 옥사미드 탈수 등으로 제조하며, 산업적으로는 시안화 수소의 산화, 질소와 아세틸렌의 반응으로 생성된다. 사이아노젠은 다른 시안 화합물과 마찬가지로 매우 유독하며, 흡입 시 치명적일 수 있다.
더 읽어볼만한 페이지
- 사이안화물 - 프러시안 블루
프러시안 블루는 1706년경 독일에서 우연히 합성된 최초의 안정적이고 내광성이 있는 파란색 안료로, 예술, 군복, 의약품, 분석 화학 등 다양한 분야에서 활용되며 최근에는 배터리 재료로도 연구되고 있다. - 사이안화물 - 치클론 B
치클론 B는 시안화수소를 주성분으로 하는 살충제로, 2차 세계 대전 중 나치 독일의 절멸 수용소에서 유대인 학살에 사용되어 악명이 높으며, 현재는 대부분의 국가에서 사용이 금지 또는 제한되었다. - 무기 탄소 화합물 - 이산화 탄소
이산화탄소(CO₂)는 탄소 원자 하나와 산소 원자 두 개로 이루어진 무색·무취의 기체로, 드라이아이스로 승화하며, 탄산 형성, 연소, 호흡, 광합성 등 다양한 과정에서 발생하고, 산업적으로 널리 사용되지만 지구 온난화의 주요 원인이자 고농도에서 인체에 유독한 물질이다. - 무기 탄소 화합물 - 이황화 탄소
이황화 탄소는 1796년 람파디우스가 합성한 무색 휘발성 액체로, 높은 굴절률과 우수한 용매 특성을 지니지만, 가연성과 독성으로 인해 건강 문제를 유발하여 사용량이 감소하고 법적 규제를 받고 있다.
2. 성질
시아노젠은 두 개의 시아노기가 탄소 원자끼리 공유 결합한 구조(NCCN)를 가지지만, 이성체로서 이소시아노젠(NCNC) 및 디이소시아노젠(CNNC)도 알려져 있다.
상온에서는 특유의 냄새를 가진 무색 기체이며, 냉수와 반응하여 시안화 수소와 시안산을 생성한다. 이는 디할로젠 분자(X2)와 유사한 성질을 나타내는 의할로젠의 특성이다. 에테르에 비교적 잘 녹으며, 염산 중에서 주석과 반응시키면 에틸렌디아민으로 환원된다.
산소와 적절히 혼합하여 연소시키면 복숭아색 불꽃을 내며 4600°C의 고온이 된다.[22]
:
이는 연소 과정에서 물이 생성되지 않기 때문이다. 반면 아세틸렌처럼 연소 시 물이 생성되면, 3000°C 정도에서 물 분자가 해리되어 그 이상의 고온을 얻기 어렵다.[22]
2. 1. 물리적 성질
시아노기 두 개가 탄소 원자끼리 공유 결합한 구조(NCCN)를 가지지만, 이성체로서 이소시아노젠(NCNC) 및 디이소시아노젠(CNNC)도 알려져 있다.상온에서는 특유의 냄새를 가진 무색 기체이다. 냉수와 반응하여 시안화 수소와 시안산을 생성하는 등, 디할로젠 분자(X2)와 유사한 성질을 나타내는 의할로젠이다. 에테르에 비교적 잘 녹는다.[22]
2. 2. 화학적 성질
시아노기 두 개가 탄소 원자끼리 공유 결합한 구조(NCCN)를 가지지만, 이성질체로 이소시아노젠(NCNC) 및 디이소시아노젠(CNNC)도 알려져 있다.상온에서는 특유의 냄새를 가진 무색 기체이다. 냉수와 반응하여 시안화 수소와 시안산을 생성하는 등, 디할로젠 분자(X2)와 유사한 성질을 나타내는 의할로젠이다.
에테르에 비교적 잘 녹는다. 염산 중에서 주석과 반응시키면 에틸렌디아민으로 환원된다.
산소와의 적절한 혼합기를 연소시키면 복숭아색 불꽃을 내며 4600°C라는 고온이 된다.[22]
:
이것은 연소에 의해 물이 생성되지 않기 때문이다. 한편 아세틸렌처럼 연소에 의해 물이 생성되면, 3000°C 정도로 물 분자가 해리되기 때문에 그 이상의 고온이 되지 않는다.[22]
고온에서 장시간 가열하면 중합체인 파라시안을 생성하며, 이 중합은 빛을 쬐면 촉진된다. 파라시안은 불용성 흑갈색 분말로, 800°C 이상으로 가열하면 다시 디시안을 유리한다.
2. 3. 이성질체
사이아노젠(NCCN)은 원자 순서가 다른 덜 안정적인 이성질체를 가진다. 이성질체로는 이소시아노젠(NCNC)과 디이소시아노젠(CNNC)이 있다.[22]3. 제조법
사이아노젠은 시안화물 화합물로부터 생성된다. 실험실에서는 시안화 수은(II) 열분해, 구리(II) 염 용액과 시안화물 반응, 오산화 이인에 의한 옥사미드(수산 아미드) 탈수, 탄소와 질소의 고온 가열 등을 통해 사이아노젠을 만든다.[10][23]
산업적으로는 시안화 수소를 산화시켜 생성하는데, 염소와 활성화된 이산화 규소 촉매를 사용하거나, 이산화 질소와 구리 염을 사용한다. 질소와 아세틸렌을 전기 불꽃이나 방전으로 반응시켜 사이아노젠을 얻기도 한다.[11][24]
3. 1. 실험실 제법
사이아노젠은 일반적으로 시안화물 화합물로부터 생성된다. 실험실에서 사이아노젠을 만드는 방법은 다음과 같다.- 시안화 수은(II) 열분해[10][23]
- 구리(II) 염 (예: 황산 구리(II)) 용액과 시안화물 반응: 불안정한 시안화 구리(II)가 생성되어 빠르게 시안화 구리(I)와 사이아노젠으로 분해된다.[10][23]
- 오산화 이인에 의한 옥사미드(수산 아미드, oxamide|옥사마이드영어) 탈수[23]
- 탄소와 질소의 고온 가열[23]
3. 2. 산업적 제법
산업적으로 사이아노젠은 시안화 수소를 산화시켜 생성한다. 이때 염소와 활성화된 이산화 규소 촉매를 사용하거나, 이산화 질소와 구리 염을 사용한다.[11][24] 또한, 질소와 아세틸렌을 전기 불꽃이나 방전으로 반응시켜 사이아노젠을 얻을 수 있다.[11][24]4. 파라시아노젠
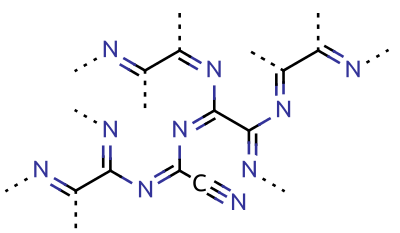
고온에서 장시간 가열하면 중합체인 파라시안을 생성하며, 이 중합은 빛을 쬐면 촉진된다. 파라시안은 불용성 흑갈색 분말로, 800°C 이상으로 가열하면 다시 디시안을 유리한다.
5. 역사
조제프 루이 게이뤼삭은 1815년에 시아노젠을 처음 합성하여 실험식을 결정하고 이름을 붙였다. 시아노젠이라는 이름은 그리스어 κυανός|kyanos|푸른색grc와 γεννάω|gennao|생성하다grc에서 유래되었는데, 이는 시안화물이 스웨덴 화학자 칼 빌헬름 셸레에 의해 프러시안 블루 색소에서 처음 분리되었기 때문이다.[14][26]
19세기 말 비료 산업이 성장하면서 시아노젠은 중요한 물질이 되었고, 현재까지도 많은 비료 생산에서 중요한 중간체로 남아있다. 니트로셀룰로스 생산의 안정제로도 사용된다.
1910년 핼리 혜성의 분광 분석 결과 혜성 꼬리에서 시아노젠이 발견되었다. 이로 인해 지구가 혜성 꼬리를 통과하면서 사람들이 중독될 것이라는 두려움이 생겼다. 뉴욕 사람들은 방독면을 착용했고, 상인들은 중독을 막는다는 돌팔이 "혜성 알약"을 팔기도 했다.[15] 그러나 혜성 꼬리는 극도로 희박하기 때문에 지구가 꼬리를 통과해도 아무런 영향이 없었다.[16][17]
6. 안전성
시아노젠은 다른 시안 화합물과 마찬가지로 매우 유독하다. 시안화물로 환원되어 시토크롬 c 산화 효소 복합체를 중독시켜 미토콘드리아의 전자 전달 연쇄를 방해한다.[18] 사이아노젠 가스는 눈과 호흡기를 자극한다. 흡입 시 노출 정도에 따라 두통, 현기증, 빠른 맥박, 메스꺼움, 구토, 의식 상실, 경련 및 사망을 초래할 수 있다.[18] 흡입 치사량은 일반적으로 100mg~150mg이다.
7. 기타
닥터 후의 "모비우스의 두뇌" 에피소드에서는 닥터가 시안화 수소를 사용하여 사이아노젠을 합성하는 장면이 나온다.[21] 1987년 영화 드래그넷에서는 악당들이 "가상 할로겐 화합물 사이아노젠"을 훔치는 내용이 나온다.[21]
참조
[1]
서적
Nomenclature of Organic Chemistry : IUPAC Recommendations and Preferred Names 2013 (Blue Book)
Royal Society of Chemistry
2014
[2]
웹사이트
oxalonitrile (CHEBI:29308)
https://www.ebi.ac.u[...]
European Bioinformatics Institute
2006-10-27
[3]
서적
NIOSH Pocket Guide to Chemical Hazards
Department of Health and Human Services, Centers for Disease Control, National Institute for Occupational Safety & Health
2007-09
[4]
서적
The Merck Index
https://archive.org/[...]
Merck & Co.
[5]
간행물
PGCH|0161
[6]
논문
Low-lying singlet excited states of isocyanogen
[7]
서적
Encyclopedia of Astrobiology
[8]
간행물
Cyanogen Bromide
http://www.orgsyn.or[...]
[9]
서적
Greenwood&Earnshaw2nd
[10]
논문
The Synthesis And Chemistry Of Cyanogen
[11]
논문
The Fixation of Atmospheric Nitrogen
https://zenodo.org/r[...]
1889-01
[12]
논문
Paracyanogen: its formation and properties. Part I
[13]
Submitted manuscript
Paracyanogen Reexamined
https://zenodo.org/r[...]
[14]
논문
Recherches sur l'acide prussique
https://books.google[...]
1815
[15]
웹사이트
Cometary Poison Gas Geyser Heralds Surprises
https://science.nasa[...]
2010-11-02
[16]
뉴스
Comet's Poisonous Tail
https://timesmachine[...]
1910-02-08
[17]
웹사이트
Halley's Comet 100 years ago
https://www.denverpo[...]
2010-05-25
[18]
서적
Hazards in the Chemical Laboratory
The Royal Institute of Chemistry
[19]
논문
Cyanogen Flames and the Dissociation Energy of N2
[20]
논문
The Temperature of the Cyanogen-Oxygen Flame
[21]
웹사이트
The trichlornitromethane and the pseudo-halogenic compound cyanogen
https://getyarn.io/y[...]
2021-08-18
[22]
논문
Cyanogen Flames and the Dissociation Energy of N2
[23]
논문
The Synthesis And Chemistry Of Cyanogen
[24]
논문
Showing the Progress and Development of Processes for the manufacture of Cyanogen and its Derivates (in: THE FIXATION OF ATMOSPHERIC NITROGEN)
[25]
서적
Greenwood&Earnshaw2nd
[26]
논문
Recherches sur l'acide prussique
https://books.google[...]
[27]
서적
Hazards in the Chemical Laboratory
The Royal Institute of Chemistry
[28]
서적
Nomenclature of Organic Chemistry : IUPAC Recommendations and Preferred Names 2013 (Blue Book)
The Royal Society of Chemistry
2014
[29]
웹인용
oxalonitrile (CHEBI:29308)
https://www.ebi.ac.u[...]
European Bioinformatics Institute
2006-10-27
[30]
서적
NIOSH Pocket Guide to Chemical Hazards
Department of Health and Human Services, Centers for Disease Control, National Institute for Occupational Safety & Health
2007-09
[31]
서적
The Merck Index
https://archive.org/[...]
Merck & Co.
[32]
간행물
PGCH|0161
본 사이트는 AI가 위키백과와 뉴스 기사,정부 간행물,학술 논문등을 바탕으로 정보를 가공하여 제공하는 백과사전형 서비스입니다.
모든 문서는 AI에 의해 자동 생성되며, CC BY-SA 4.0 라이선스에 따라 이용할 수 있습니다.
하지만, 위키백과나 뉴스 기사 자체에 오류, 부정확한 정보, 또는 가짜 뉴스가 포함될 수 있으며, AI는 이러한 내용을 완벽하게 걸러내지 못할 수 있습니다.
따라서 제공되는 정보에 일부 오류나 편향이 있을 수 있으므로, 중요한 정보는 반드시 다른 출처를 통해 교차 검증하시기 바랍니다.
문의하기 : help@durumis.com
