핵산 대사
"오늘의AI위키"의 AI를 통해 더욱 풍부하고 폭넓은 지식 경험을 누리세요.
1. 개요
핵산 대사는 뉴클레오타이드의 합성, 분해, 상호 전환 과정을 포괄하는 생화학적 과정이다. 뉴클레오타이드는 퓨린 또는 피리미딘 염기, 당, 인산으로 구성되며, 퓨린은 아데닌과 구아닌, 피리미딘은 시티딘, 우리딘, 티미딘을 포함한다. 뉴클레오타이드 합성은 PRPP를 사용하여 진행되며, 퓨린과 피리미딘 합성은 서로 다른 방식으로 이루어진다. DNA 합성을 위해서는 리보스를 디옥시리보스로 전환하는 과정이 필요하다. 핵산 분해는 퓨린을 요산으로, 피리미딘을 베타-알라닌 등으로 분해하며, 이 과정에서 다양한 효소가 작용한다. 뉴클레오타이드 간에는 인산 교환을 통해 상호 전환이 일어난다.
더 읽어볼만한 페이지
- 핵산 - 염기쌍
염기쌍은 DNA나 RNA에서 아데닌(A)이 티민(T) 또는 우라실(U)과, 구아닌(G)이 사이토신(C)과 수소 결합으로 연결된 뉴클레오염기 쌍을 의미하며, DNA 이중 나선 구조 안정성과 유전 정보 복제 및 전사에 필수적이고, 유전자나 DNA 조각의 크기를 나타내는 단위로 사용된다. - 핵산 - RNA
RNA는 DNA와 함께 생명체의 유전 물질을 구성하는 핵심 분자로서, DNA의 유전 정보를 바탕으로 단백질 합성, 유전자 발현 조절, 촉매 작용 등 다양한 기능을 수행하며, mRNA 백신 개발에 기여하였다. - 피리미딘 - 이마티닙
이마티닙은 Bcr-Abl 티로신 키나아제를 포함한 여러 티로신 키나아제의 활성을 선택적으로 억제하는 표적 항암제로, 만성 골수성 백혈병과 위장관기질종양 치료에 주로 사용되며, FDA 승인 후 CML 환자의 생존율을 크게 향상시켰고, 사회경제적 논란에도 불구하고 암 치료에 획기적인 발전을 가져온 약물로 평가받는다. - 피리미딘 - 티민
티민은 DNA의 네 가지 염기 중 하나로, 아데닌과 수소 결합을 통해 DNA 구조를 안정화시키며, DNA 복제, 돌연변이, 암 치료제 표적, 그리고 우주 기원 연구와 관련되어 있다. - 대사경로 - 스테로이드
스테로이드는 4개의 융합된 고리 구조를 가지는 유기 화합물로, 콜레스테롤, 스테로이드 호르몬, 담즙산 등 생물학적 활성 분자를 포함하며, 메발론산 경로를 통해 생합성되어 다양한 생리적 기능을 수행하고 의학적으로 사용되지만 오남용 시 부작용을 초래할 수 있다. - 대사경로 - 시트르산 회로
시트르산 회로는 아세틸-CoA를 이산화탄소로 산화시켜 NADH와 FADH₂를 생성, ATP 생산 및 생합성에 기여하며, 탄수화물, 지방, 단백질 대사를 연결하는 중심적인 대사 경로이다.
| 핵산 대사 | |
|---|---|
| 개요 | |
| 핵산 대사 | 세포 내에서 핵산의 합성, 분해, 및 변형을 포함하는 생화학적 과정의 총칭 |
| 주요 과정 | DNA 복제 DNA 복구 RNA 전사 RNA 번역 퓨린 및 피리미딘의 합성 및 분해 |
| 관련 물질 | 뉴클레오타이드 뉴클레오사이드 퓨린 피리미딘 DNA RNA |
| 상세 과정 | |
| 뉴클레오타이드 합성 | 데 옥시 리보 뉴클레오타이드와 리보 뉴클레오타이드는 아미노산, 이산화탄소, 포름산과 같은 작은 전구체 분자로부터 드 노보 합성된다. 회수 경로는 유리 염기 (퓨린 또는 피리미딘)가 뉴클레오사이드 포스 포릴라아제의 도움으로 리보스 1-인산에 전달되어 뉴클레오사이드가 되고, 이어서 키나아제가 작용하여 뉴클레오타이드가 되는 것을 재활용한다. |
| 뉴클레오타이드 분해 | 뉴클레오타이드는 먼저 뉴클레오사이드 형태로 전환된 다음, 질소 염기와 오탄당으로 더 분해된다. 질소 염기의 분해는 퓨린과 피리미딘에 따라 다른 경로를 따른다. |
| 아미노산 및 뉴클레오타이드 대사의 연관성 | 아미노산 대사는 퓨린 및 피리미딘 합성 모두에 필요한 단편을 제공하여 뉴클레오타이드 대사에 기여한다. |
| 관련 질병 | |
| 원인 | 핵산 대사의 결함은 다양한 유전 질환으로 이어질 수 있다. 예를 들어, 레스-니한 증후군은 퓨린 대사의 효소인 HGPRT의 결핍으로 인해 발생한다. |
| 관련 질병 | 통풍 레스-니한 증후군 ADA 결핍증 |
| 추가 정보 | |
| 관련 효소 | 리보 뉴클레오타이드 환원 효소 (RNR) 티미딜레이트 합성 효소 디 하이드로 폴레이트 환원 효소 (DHFR) HGPRT 아데노신 데 아미나아제 (ADA) |
2. 뉴클레오타이드 합성
뉴클레오타이드는 핵산으로 중합되는 단량체이다. 모든 뉴클레오타이드는 당, 인산, 질소 염기를 포함한다. 핵산에서 발견되는 염기는 퓨린 또는 피리미딘이다. 복잡한 다세포 동물에서 이들은 주로 간에서 생성되지만, 두 그룹은 서로 다른 방식으로 합성된다. 모든 뉴클레오타이드 합성은 뉴클레오타이드 생성에 필요한 리보스와 인산을 제공하는 인산리보실 피로인산(PRPP)을 사용한다.
퓨린 뉴클레오타이드 합성과 피리미딘 뉴클레오타이드 합성은 그 과정이 서로 다르다. 퓨린 합성은 인산리보실 피로인산(PRPP)으로부터 여러 단계를 거쳐 이노신 일인산(IMP)을 생성하는 과정에서 시작하고, 피리미딘 합성은 우리딘 생성을 시작으로 한다.
2. 1. 퓨린 뉴클레오타이드 합성
아데닌과 구아닌은 퓨린으로 분류되는 두 가지 뉴클레오타이드이다. 퓨린 합성은 인산리보실 피로인산(PRPP)가 이노신 일인산(IMP)으로 전환되는 과정이다. PRPP에서 IMP를 생성하려면 글루타민, 글리신, 아스파르트산 및 6개의 ATP 등이 필요하다.[1] IMP는 이후 GTP와 아스파르트산을 사용하여 AMP (아데노신 일인산)로 전환되며, 아스파르트산은 푸마르산으로 전환된다. IMP가 AMP로 직접 전환될 수 있는 반면, GMP (구아노신 일인산) 합성은 NAD+를 사용하여 중간체 잔토신 일인산, 즉 XMP를 형성하는 중간 단계를 필요로 한다. XMP는 1 ATP의 가수분해와 글루타민이 글루탐산으로의 전환을 사용하여 GMP로 전환된다.[1] AMP와 GMP는 추가적인 인산을 첨가하는 키나아제에 의해 각각 ATP와 GTP로 전환될 수 있다.ATP는 GTP 생성을 자극하고, GTP는 ATP 생성을 자극한다. 이러한 상호 조절은 ATP와 GTP의 상대적인 양을 일정하게 유지한다. 어느 뉴클레오타이드의 과도한 증가는 잘못된 퓨린 뉴클레오타이드가 삽입되는 DNA 돌연변이의 가능성을 증가시킬 수 있다.[1]
레쉬-니한 증후군은 하이포잔틴-구아닌 포스포리보실전이효소(HGPRT)의 결핍으로 인해 발생하며, 이는 GMP에서 구아닌을 생성하는 가역 반응을 촉매하는 효소이다. 이는 정신 지체, 경련, 자해 충동과 함께 요산의 과다 생성을 유발하는 성 관련 선천적 결함이다.[1][2][3]
2. 2. 피리미딘 뉴클레오타이드 합성
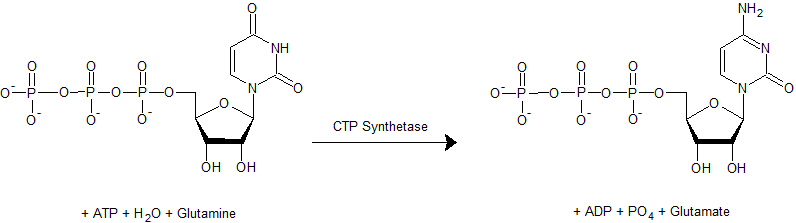
피리미딘 뉴클레오시드에는 시티딘, 우리딘, 티미딘이 포함된다.[4] 모든 피리미딘 뉴클레오타이드 합성은 우리딘 형성으로 시작된다. 이 반응에는 아스파르트산, 글루타민, 중탄산염, 2개의 ATP(에너지 제공), PRPP(리보스-모노포스페이트 제공)가 필요하다. 퓨린 합성과 달리, PRPP 유래 당/인산기는 마지막 단계에 질소 염기에 첨가된다. 우리딘-모노포스페이트 합성 후, 2개의 ATP와 반응해 UTP를 형성할 수 있다. UTP는 CTP 합성효소 촉매 반응으로 CTP로 전환될 수 있다. 티미딘 합성은 우리딘을 데옥시우리딘으로 환원 후 염기를 메틸화해야 한다.[1][8]
ATP는 피리미딘 합성을 활성화하고, CTP는 억제한다. 이는 퓨린/피리미딘 양을 유사하게 유지하여 DNA 합성에 필요한 퓨린과 피리미딘을 동일하게 공급한다.[1][5]
피리미딘 합성 효소 결핍은 오로트산뇨증을 유발하며, 이는 소변으로 오로트산이 과도하게 배설되는 유전 질환이다.[1][6]
2. 3. 뉴클레오타이드에서 디옥시뉴클레오타이드로의 전환
뉴클레오타이드는 처음에는 리보스를 당 성분으로 만들어지는데, 이는 RNA의 특징이다. 그러나 DNA는 리보스의 2'-하이드록실기(-OH기)가 없는 ''디옥시''리보스를 필요로 한다. 이 -OH기를 제거하는 반응은 리보뉴클레오타이드 환원효소에 의해 촉매된다. 이 효소는 뉴클레오사이드 이인산(NDP)을 디옥시뉴클레오사이드 이인산(dNDP)으로 전환시킨다. 뉴클레오타이드는 반응이 일어나기 위해 이인산 형태여야 한다.[1]티미딘을 합성하기 위해, 디옥시 형태만 존재하는 DNA의 구성 요소인 우리딘은 리보뉴클레오타이드 환원효소에 의해 디옥시우리딘으로 변환된 다음, 티미딜산 합성효소에 의해 메틸화되어 티미딘을 생성한다.[1]
3. 핵산 분해

DNA와 RNA는 세포 내에서 지속적으로 분해된다. 퓨린 및 피리미딘 뉴클레오시드는 분해되어 노폐물로 배설되거나 뉴클레오티드 구성 요소로 재활용될 수 있다.[8]
3. 1. 피리미딘 이화작용
사이토신과 우라실은 베타-알라닌으로 전환된 후, 지방산 합성 등에 필요한 말로닐-CoA로 전환된다. 반면에 티민은 β-아미노아이소부티르산으로 전환된 후, 이를 이용하여 메틸말로닐-CoA를 형성한다. 남은 탄소 골격인 아세틸-CoA와 석시닐-CoA는 시트르산 회로를 통해 산화될 수 있다. 피리미딘 분해는 최종적으로 암모늄, 물, 이산화 탄소의 생성을 통해 종결되며, 암모늄은 세포의 세포질과 미토콘드리아에서 일어나는 요소 회로에 들어갈 수 있다.[8]피리미딘 염기는 재활용될 수도 있다. 예를 들어 우라실 염기는 리보스-1-인산과 결합하여 우리딘 일인산(UMP)을 생성할 수 있다. 유사한 반응이 티민과 데옥시리보스-1-인산으로도 수행될 수 있다.[12]
피리미딘 이화 작용에 관여하는 효소의 결핍은 디히드로피리미딘 탈수소 효소 결핍증과 같이 부정적인 신경학적 영향을 미치는 질병을 유발할 수 있다.[7]
3. 2. 퓨린 이화작용
퓨린 분해는 주로 사람의 간에서 일어나며 퓨린을 요산으로 분해하기 위해 다양한 효소가 필요하다. 먼저, 뉴클레오타이드는 5'-뉴클레오티데이스를 통해 인산을 잃는다. 아데노신 뉴클레오사이드는 아데노신 탈아미노화 효소와 뉴클레오시다아제를 통해 탈아미노화 및 가수 분해되어 하이포잔틴을 형성한다. 하이포잔틴은 잔틴 산화 효소의 작용을 통해 산화되어 잔틴을 형성한 다음 요산으로 전환된다. 다른 퓨린 뉴클레오사이드인 구아노신은 분해되어 구아닌을 형성한다. 구아닌은 구아닌 탈아미노화 효소를 통해 탈아미노화되어 잔틴을 형성하고, 잔틴은 다시 요산으로 전환된다. 산소는 두 퓨린의 분해에서 최종 전자 수용체이다. 요산은 동물에 따라 다양한 형태로 신체에서 배설된다.[8]세포 내로 방출되는 자유 퓨린 및 피리미딘 염기는 일반적으로 막을 가로질러 세포 간 수송되어 뉴클레오타이드 재활용을 통해 더 많은 뉴클레오타이드를 생성하기 위해 재활용된다. 예를 들어, 아데닌 + PRPP → AMP + PPi 반응에는 아데닌 포스포리보실전이효소가 필요하다. 자유 구아닌은 동일한 방식으로 재활용되지만 하이포잔틴-구아닌 포스포리보실전이효소가 필요하다.
퓨린 이화 작용의 결함은 다양한 질병을 유발할 수 있으며, 여기에는 다양한 관절에 요산 결정이 축적되어 발생하는 통풍과 면역 결핍증을 유발하는 아데노신 탈아미노화 효소 결핍증이 포함된다.[9][10][11]
4. 뉴클레오타이드 상호 전환
핵산이 합성된 후에는 단인산, 이인산, 삼인산 분자 간에 인산을 교환할 수 있다. 뉴클레오사이드 이인산 키나아제는 뉴클레오사이드 이인산(NDP)을 뉴클레오사이드 삼인산(NTP)으로 전환하는 반응을 촉매하며, ATP를 인산 공여체로 사용한다.[1] 뉴클레오사이드 일인산 키나아제는 뉴클레오사이드 일인산의 인산화를 수행한다. 아데닐산 키나아제는 2ADP ⇔ ATP + AMP의 상호 변환을 통해 세포 에너지 변동을 조절하는 특정 뉴클레오티드 키나아제이다.[1][12]
참조
[1]
서적
Fundamentals of the biochemistry : life at the molecular level
Wiley
2008
[2]
논문
The Lesch-Nyhan syndrome.
1973
[3]
웹사이트
Lesch-Nyhan
http://www.lesch-nyh[...]
2014-10-31
[4]
논문
Role of pH in Regulating Cancer Pyrimidine Synthesis
2022-07-06
[5]
웹사이트
Nucleotide Metabolism II
http://oregonstate.e[...]
2014-10-20
[6]
논문
Orotic aciduria and uridine monophosphate synthase: a reappraisal.
2009
[7]
웹사이트
Dihydropyrimidine dehydrogenase deficiency
http://ghr.nlm.nih.g[...]
2014-10-31
[8]
서적
Lehninger's Principles of Biochemistry
https://archive.org/[...]
Macmillan
2008
[9]
웹사이트
Nucleotides: Their Synthesis and Degradation
http://homepages.rpi[...]
2014-10-20
[10]
논문
Disorders of purines and pyrimidines.
2014
[11]
웹사이트
Adenosine deaminase (ADA) deficiency
http://learn.genetic[...]
2014-10-31
[12]
웹사이트
Nucleotide Metabolism
http://themedicalbio[...]
2014-10-20
[13]
서적
Fundamentals of biochemistry : life at the molecular level
Wiley
2008
본 사이트는 AI가 위키백과와 뉴스 기사,정부 간행물,학술 논문등을 바탕으로 정보를 가공하여 제공하는 백과사전형 서비스입니다.
모든 문서는 AI에 의해 자동 생성되며, CC BY-SA 4.0 라이선스에 따라 이용할 수 있습니다.
하지만, 위키백과나 뉴스 기사 자체에 오류, 부정확한 정보, 또는 가짜 뉴스가 포함될 수 있으며, AI는 이러한 내용을 완벽하게 걸러내지 못할 수 있습니다.
따라서 제공되는 정보에 일부 오류나 편향이 있을 수 있으므로, 중요한 정보는 반드시 다른 출처를 통해 교차 검증하시기 바랍니다.
문의하기 : help@durumis.com