광유전학
"오늘의AI위키"의 AI를 통해 더욱 풍부하고 폭넓은 지식 경험을 누리세요.
1. 개요
광유전학은 빛을 사용하여 유전자 조작된 세포의 활동을 정밀하게 제어하는 생물학 기술이다. 1979년 프랜시스 크릭의 아이디어를 시작으로, 2000년대 초 채널로돕신과 같은 광활성 단백질의 발견과 개발을 통해 발전했다. 광유전학은 신경 회로 연구, 질병 연구 및 치료, 행동 연구, 세포 생물학 연구 등 다양한 분야에 응용되며, 뇌와 같은 복잡한 생체 조직의 기능을 이해하는 데 기여한다. 기술적 과제로는 선택적 발현, 반응 속도, 빛 흡수 스펙트럼, 공간적 반응 등이 있으며, 이 분야의 발전에 기여한 과학자들은 여러 권위 있는 상을 수상했다.
더 읽어볼만한 페이지
- 신경공학 - 사이보그
사이보그는 인공 부위를 이식받아 신체 기능이 복원되거나 향상된 개조 생명체로, 보철, 인공 장기 등의 기술을 포함하며 의료, 윤리, 군사적 측면에서 다양한 논의를 낳고 있다. - 신경공학 - 뇌자도
뇌자도(MEG)는 뇌에서 발생하는 미세한 자기장을 감지하여 뇌 활동을 측정하는 신경 영상 기술이며, 뇌파 검사보다 공간 해상도가 뛰어나 뇌전증, 뇌종양 등의 진단 및 연구에 활용된다. - 제어이론 - 칼만 필터
칼만 필터는 잡음이 있는 측정값들을 이용하여 선형 동적 시스템의 상태를 추정하는 재귀 필터로, 예측과 보정 단계를 반복하며 항법 시스템, 레이더 추적, 컴퓨터 비전 등 다양한 분야에 응용된다. - 제어이론 - 사이버네틱스
사이버네틱스는 동물과 기계의 제어 및 통신을 연구하는 학문으로, 제어 시스템, 신경과학 등 다양한 분야를 통합하여 발전해왔으며, 피드백, 자기조직화 등의 핵심 개념을 통해 여러 분야에 응용되고 있다. - 사이버네틱스 - 진화 알고리즘
진화 알고리즘은 생물학적 진화 과정을 모방하여 적합도에 따라 개체를 선택하고 교차 및 돌연변이 연산을 반복하며 최적의 해를 찾아가는 계산 기술이다. - 사이버네틱스 - AI 안전
AI 안전은 인공지능 시스템의 부정적 결과를 줄이기 위한 연구 및 정책 분야로, 시스템 강건성 확보, 가치 정렬, 사이버 보안, 제도 개선 등을 포함하며 현재와 미래의 위험을 관리하기 위한 국제 협력과 거버넌스를 강조한다.
| 광유전학 | |
|---|---|
| 개요 | |
 | |
| 정의 | 빛을 사용하여 뉴런 또는 다른 세포 유형의 활동을 제어하는 생물학적 기술 |
| 역사 | |
| 최초 보고 | 2002년 네이처 생명공학에 발표된 Shimizu-Sato 등의 논문 |
| 본격적인 발전 | 2000년대 후반, 칼 데이세로스 연구팀이 광유전학 기술을 신경과학에 적용하면서 급속히 발전 |
| 원리 | |
| 핵심 요소 | 빛에 반응하는 단백질 (광활성 단백질) 유전자 조작 기술 광 자극 시스템 |
| 광활성 단백질 | 채널로돕신 (ChR2): 청색광에 반응하여 양이온 채널을 열어 세포를 활성화 할로로돕신 (NpHR): 황색광에 반응하여 염화 이온 펌프를 작동시켜 세포를 억제 |
| 작동 방식 | 특정 세포에 광활성 단백질을 발현시킨 후, 빛을 비추어 세포의 활동을 조절 |
| 응용 분야 | |
| 신경과학 | 특정 신경 회로의 기능 연구 행동 조절 메커니즘 규명 기억, 학습, 중독 등 다양한 인지 과정 연구 |
| 질병 연구 | 파킨슨병, 알츠하이머병 등 신경 질환 모델 연구 정신 질환의 신경 생물학적 기초 연구 |
| 행동 연구 | 초파리의 먹이 섭취 행동 조절 Musso, Pierre-Yves; Junca, Pierre; Jelen, Meghan; Feldman-Kiss, Damian; Zhang, Han; Chan, Rachel CW; Gordon, Michael D. (2019-07-19). "Closed-loop optogenetic activation of peripheral or central neurons modulates feeding in freely moving Drosophila". eLife. 8: e45636. doi:10.7554/eLife.45636. ISSN 2050-084X. PMC 6668987. PMID 31322499. 초파리의 후진 보행 운동 회로 조절 Feng, Kai; Sen, Rajyashree; Minegishi, Ryo; Dübbert, Michael; Bockemühl, Till; Büschges, Ansgar; Dickson, Barry J. (2020-12-02). "Distributed control of motor circuits for backward walking in Drosophila". Nature Communications. 11 (1): 6166. doi:10.1038/s41467-020-19936-x. ISSN 2041-1723. PMC 7710706. PMID 33268800. 초파리의 다리 고유수용성 감각 회로 연구 Chen, Chenghao; Agrawal, Sweta; Mark, Brandon; Mamiya, Akira; Sustar, Anne; Phelps, Jasper S.; Lee, Wei-Chung Allen; Dickson, Barry J.; Card, Gwyneth M.; Tuthill, John C. (2021-12-06). "Functional architecture of neural circuits for leg proprioception in Drosophila". Current Biology. 31 (23): 5163–5175.e7. doi:10.1016/j.cub.2021.09.035. ISSN 0960-9822. PMC 8665017. PMID 34637749. 초파리의 중앙 복합체의 기능적 연결체 구축 Franconville, Romain; Beron, Celia; Jayaraman, Vivek (2018-08-20). "Building a functional connectome of the Drosophila central complex". eLife. 7: e37017. doi:10.7554/eLife.37017. ISSN 2050-084X. PMC 6150698. PMID 30124430. |
| 장점 | |
| 높은 시간 및 공간 해상도 | 밀리초 단위의 시간 해상도와 특정 세포 수준의 공간 해상도로 신경 활동 조절 가능 |
| 세포 유형 특이성 | 특정 유전자 발현 세포에만 작용하여 정밀한 제어 가능 |
| 가역성 | 빛 자극을 끄면 세포 활동이 원래 상태로 회복 |
| 단점 | |
| 침습성 | 유전자 조작을 위해 뇌에 직접 바이러스 주입 필요 |
| 빛의 침투 깊이 제한 | 빛이 뇌 조직 깊숙이 침투하기 어려워 적용 범위 제한적 |
| 면역 반응 | 광활성 단백질에 대한 면역 반응 가능성 |
| 기술 발전 | |
| 다양한 광활성 단백질 개발 | 다양한 파장의 빛에 반응하는 단백질, 더 강력한 활성 또는 억제 효과를 가진 단백질 개발 |
| 비침습적 광 자극 기술 개발 | 초음파, 자기장 등을 이용한 광 자극 기술 연구 |
| 광유전학 도구의 정밀성 향상 | 세포 유형 특이적 발현 시스템 개선, 빛 자극 전달 시스템 개선 |
| 참고 문헌 | |
2. 역사
1979년, 프랜시스 크릭은 뇌의 특정 유형 세포만을 제어하고 다른 세포는 거의 변경하지 않는 것이 신경과학의 과제라고 제안했다. 크릭은 빛을 사용하는 기술이 시간적, 공간적 정밀도로 신경 활동을 제어하는 데 유용할 수 있다고 추측했지만, 당시에는 뉴런을 빛에 반응하게 만드는 기술이 없었다.
1990년대 초, LC 카츠와 E. 캘러웨이는 빛이 글루탐산을 언케이지할 수 있음을 보여주었다.[17] 1994년 헤버레와 뷜트는 효모에서 박테리오로돕신을 이용해 빛으로 활성화되는 이온 흐름을 보여주었다.[18] 1995년, 게오르그 나겔 등과 에른스트 밤베르크는 미생물 로돕신(박테리오로돕신 포함)의 이종 발현으로 빛 유도 전류를 확인했다.
2002년 1월, 보리스 제멜만과 게로 미젠뵈크는 ''초파리'' 로돕신 배양 포유류 뉴런을 사용하여 빛으로 뉴런을 제어하는 최초의 유전자 표적 방식을 보고했다.[19] 2003년, 제멜만과 미젠뵈크는 단일 이온성 채널 TRPV1, TRPM8 및 P2X2가 광케이지된 리간드에 의해 게이트되는 뉴런의 빛 의존적 활성화를 위한 두 번째 방식을 개발했다.[20] 2004년부터 크라머와 이사코프 그룹은 트라우너 그룹과 협력하여 유전자 도입 이온 채널과 상호 작용하는 유기 광스위치("가역적으로 케이지된" 화합물)를 개발했다.[21][22] TRPV1 방법론은 이후 여러 연구실에서 실험 동물의 먹이 섭취, 이동 및 행동 회복력을 변경하는 데 사용되었다.[23][24][25] 그러나 뉴런 활동 변경을 위한 빛 기반 접근 방식은 채널로돕신이 더 쉽게 사용 가능해지면서 원래 연구실 밖에서는 적용되지 않았다.[26]
페터 헤게만은 레겐스부르크 대학교에서 녹조류의 광주성 연구 중, 고전적인 G 단백질 결합 로돕신으로 설명할 수 없는 빠른 광전류를 발견했다.[27] 프랑크푸르트 막스 플랑크 연구소의 게오르그 나겔과 협력하여, 조류 ''클라미도모나스 레이나르티''의 단일 유전자가 개구리 난모세포에서 발현될 때 큰 광전류를 생성함을 입증했다.[28] 발현 세포 식별을 위해 조류 단백질의 세포질 꼬리를 형광 단백질 YFP로 대체하여 최초의 일반적 광유전학 도구를 생성했다.[26] 2003년 논문에서 "난모세포 또는 포유류 세포에서 ChR2 발현은 단순 조명으로 세포질 Ca2+ 농도를 증가시키거나 세포막을 탈분극화시키는 강력한 도구"라고 말했다.
스탠포드 대학교 칼 다이서로스는 2004년 7월 초 채널로돕신 발현 뉴런의 빛 활성화를 보여주는 실험 노트를 출판했다.[29] 2005년 8월, 그의 연구실(대학원생 에드 보이든, 펑 장 포함)은 게오르그 나겔과 협력, 게오르그 나겔의 채널로돕신-2(H134R)-eYFP 돌연변이를 사용하여 신경 세포에서 단일 구성 요소 광유전학 시스템의 첫 시연을 발표했다.[30] 이 돌연변이는 게오르그 나겔과 헤게만이 기능적 특성을 처음 규명한 이후 채널로돕신-2의 첫 번째 돌연변이였다.[26]
웨인 주립 대학교 주오-화 판은 실명 시력 회복 연구 중, 뇌와 연결되는 망막 신경절 세포에서 채널로돕신을 시험했다. 판에 따르면, 채널로돕신으로 망막 뉴런의 광학적 활성화를 처음 관찰한 것은 2004년 2월이었다.[31] 이는 다이서로스가 2004년 7월에 처음 관찰하기 5개월 전이었다.[32] 2005년 주오-화 판은 쥐 망막 신경절 세포에서 채널로돕신의 생체 내 형질 전환과 망막 절편 배양에서 광자극에 대한 전기적 반응을 보고했다.[33] 이 접근법은 2021년 보톤드 로스카와 동료들에 의해 인간 환자에게 실현되었다.[88]
2005년 4월, 수사나 리마와 미젠뵈크는 유전자 표적 P2X2 광자극을 사용하여 동물의 행동을 제어하는 첫 사례를 보고했다.[34] 도파민성 뉴런 그룹의 광자극이 초파리에서 특징적인 행동 변화를 유발함을 보였다.
2005년 10월, 린 랜드메서와 스테판 헐리체는 채널로호돕신-2를 사용하여 배양된 해마 뉴런과 발달 중인 닭 척수 회로에서 신경 활동을 제어하는 연구 결과를 발표했다.[35] 또한, 해마 뉴런과 발달 중인 닭 배아에서 세포 내 신호 전달 경로를 동원, 신경 활동을 억제하는 도구로 척추 동물 로돕신(빛 활성화 G 단백질 결합 수용체)을 처음 도입했다.[35]
알렉산더 고트샬크와 게오르그 나겔 그룹은 최초의 ChR2 돌연변이(H134R)를 만들고, 유전자 선택 신경 회로의 빛 자극으로 ''꼬마선충''의 운동 패턴을 유발, 온전한 동물에서 신경 활동 제어에 채널로돕신-2를 처음 사용했다(2005년 12월 발표).[36] 쥐의 경우, 광유전학 도구의 제어된 발현은 1990년대 조 Z. 치엔이 개발한 세포 유형 특이적 Cre/loxP 방식을 사용하여 특정 뇌 영역과 세포 유형을 활성화/억제함으로써 ''생체 내''에서 달성된다.[37][38]
2007년, 보이든과 다이서로스 연구실(게오르그 나겔 그룹과 함께)은 신경 세포 활동의 광유전학적 억제를 동시에 보고했다.[39][40]
2007년, 게오르그 나겔과 헤게만 그룹은 cAMP의 광유전학적 조작을 시작했다.[41] 2014년, 아벨라 등은 곰팡이에서 최초의 로돕신-구아닐릴 사이클라제 유전자를 보고했다. 2015년, 샤이프 등과 가오 등은 로돕신-구아닐릴 사이클라제 유전자의 활성을 특징지었다. 시치앙 가오 등과 게오르그 나겔, 알렉산더 고트샬크는 이를 최초의 8 TM 로돕신으로 확인했다.[42]
광유전학이라는 용어는 2006년에 처음 사용되었다.
광활성화 이온 채널인 채널로돕신2 또는 할로로돕신을 특정 뉴런에 유전자 공학으로 발현시킨 후, 특정 파장의 빛을 조사하여 표적 뉴런을 흥분/억제시킬 수 있다.
광유전학 대상은 저분자량 G 단백질 등으로 확대되고 있다. 2009년 클라우스 한 등은 phototropin을 사용한 PA (photoactivatable)-Rac을 보고했다. Neuroscience 2009년에는 PA-RhoA, PA-Cdc42 등도 만들어지고 있음이 보고되었다.
Neuroscience 2009년, 스탠퍼드 대학교 칼 다이서로스는 채널로돕신2에 GPCR을 융합시킨 광유전학 도구를 발표했다. 빛 자극으로 cAMP, IP3, DAG 등 세컨드 메신저 생성을 국소 제어할 수 있다.
광유전학 연구 방법은 네이처 메서드에 의해 "올해의 방법 2010"으로 선정되었다.[168]
신경과학 분야에서, 빛으로 막 전위를 측정하는 막 전위 이미징과 조합, 기존 전기 생리학적 방법에 대신하는 "빛으로 신경의 전기적 특성을 해명하는 도구"인 광학적 전기 생리학으로도 사용된다.
2. 1. 초기 아이디어 및 실험
1979년, 프랜시스 크릭은 신경과학의 주요 과제 중 하나로 특정 유형의 뇌 세포만을 제어하는 기술의 필요성을 제안했다. 그는 빛을 이용하는 기술이 이러한 목표를 달성하는 데 유용할 수 있다고 추측했지만, 당시에는 뉴런을 빛에 반응하게 만드는 기술이 없었다.1990년대 초, LC 카츠와 E. 캘러웨이는 빛으로 글루탐산을 언케이지할 수 있음을 보여주었다.[17] 1994년, 헤버레와 뷜트는 효모에서 박테리오로돕신을 이용해 빛으로 활성화되는 이온 흐름을 보여주었다.[18] 1995년, 게오르그 나겔 등과 에른스트 밤베르크는 미생물 로돕신(박테리오로돕신 포함)의 이종 발현을 통해 빛으로 유도된 전류를 확인했다.[19]
2. 2. 채널로돕신 발견과 광유전학 발전
채널로돕신은 미생물인 해조류에서 추출된 단백질이다. 클라미도모나스라는 해조류가 유명한데, 이 해조류는 주광성을 가지고 있어 빛이 있는 곳으로 모이는 특징이 있다. 주광성을 띠게하는 원인이 바로 채널로돕신인데, 이 단백질은 푸른 빛을 전기로 바꾸는 역할을 하여 빛이 있을 때 조류가 지속적으로 에너지를 공급받을 수 있도록 해준다.채널로돕신은 광유전학에서 핵심적인 역할을 한다. 예를 들어 특정 뉴런을 활성화시키고자 할 때, 바이러스 벡터를 이용하여 활성화를 원하는 뉴런에 채널로돕신을 넣으면 채널로돕신이 있는 특정 뉴런만 빛에 의해 활성화된다. 이처럼 채널로돕신은 광유전학에서 빛을 인지하는 센서로 작용하며, 자극을 원하는 세포만을 자극할 수 있도록 해준다는 장점이 있다.
2. 3. 한국의 광유전학 연구
광유전학의 주요 문제점 중 하나는 모든 세포가 동일한 수준으로 미생물 옵신 유전자를 발현하지 않을 수 있다는 점이다. 따라서 정의된 빛의 강도로 조사하더라도 개별 세포에 다양한 영향을 미칠 수 있다. 뇌의 뉴런에 대한 광유전학적 자극은 광원(예: 삽입된 광섬유)으로부터 빛의 강도가 기하급수적으로 감소하기 때문에 통제가 더욱 어렵다.[49]옵신을 세포막, 시냅스 소포 또는 미토콘드리아와 같은 정의된 세포내 구획에 표적화하는 것은 여전히 어렵다.[49][74] 옵신을 수상돌기, 세포체 또는 축삭 종말과 같은 세포막의 특정 영역으로 제한하면 뉴런 회로에 대한 보다 강력한 이해를 제공한다.[74]
수학적 모델링에 따르면 특정 세포 유형에서 옵신의 선택적 발현은 신경 회로의 동적 동작을 극적으로 변경할 수 있다. 특히, 억제성 세포를 우선적으로 표적으로 하는 광유전학적 자극은 신경 조직의 흥분성을 변화시켜 비 형질전환 뉴런에도 영향을 미칠 수 있다.[75]
3. 광유전학의 구성 요소 및 기술
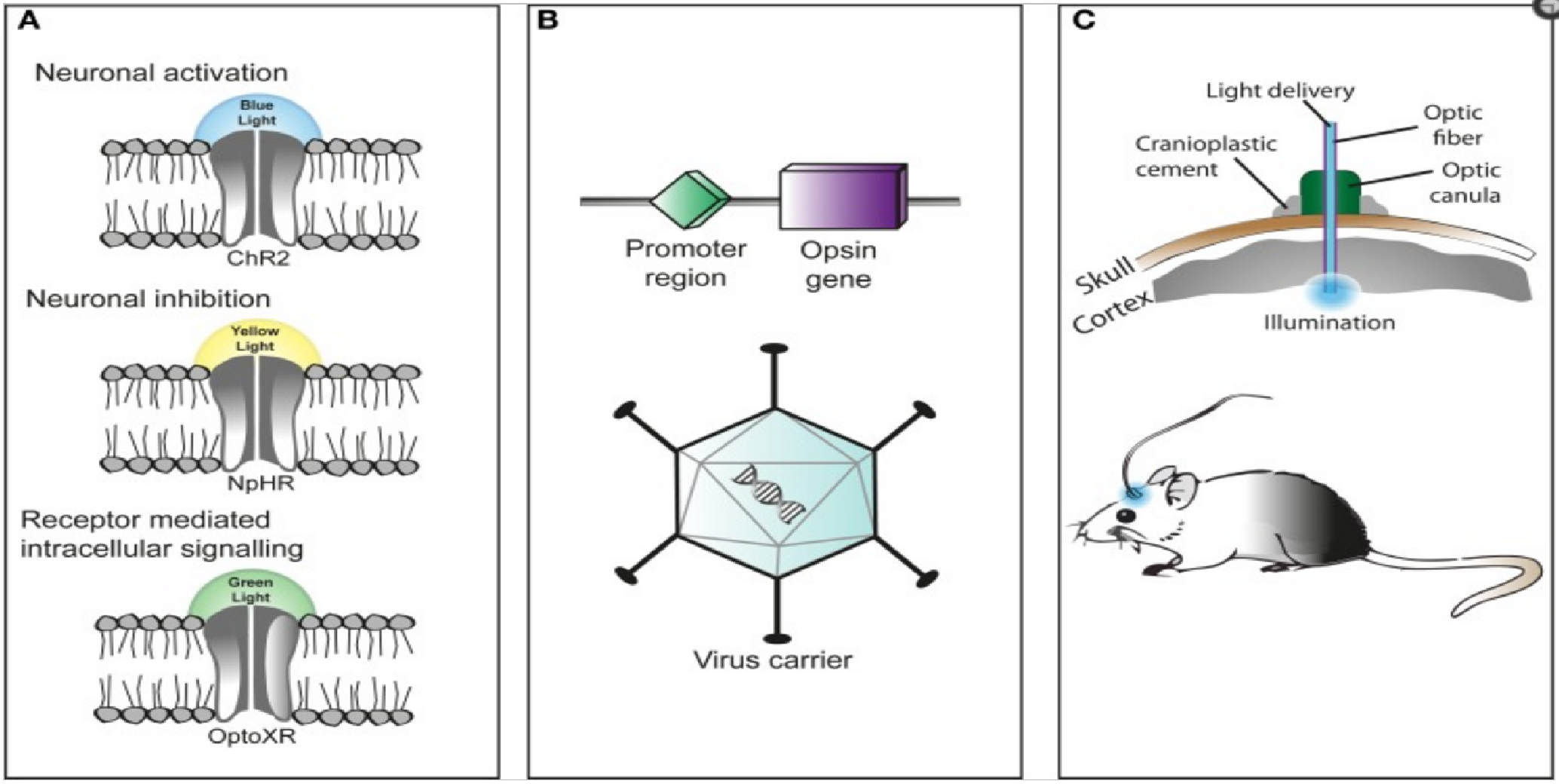
광유전학은 빛에 반응하는 단백질인 옵신, 유전자 전달 기술, 광학 자극 기술, 이 세 가지 주요 요소로 구성된다.
옵신: 광유전학의 핵심 요소로, 빛을 감지하여 세포 내 신호 전달을 유도하는 단백질이다. 채널로돕신은 해조류에서 추출된 단백질로, 빛을 받아 세포를 활성화시키는 역할을 한다. 예를 들어, 채널로돕신을 특정 뉴런에 발현시키면, 빛을 통해 해당 뉴런만 선택적으로 활성화시킬 수 있다.[45]
광유전학적 액추에이터 발현: 광유전학은 특정 뉴런 집단에 광 감응성 프로브를 전달하기 위해 세포 특이적 프로모터나 맞춤형 조건부 활성 바이러스와 같은 유전자 표적화 전략을 사용한다. 무척추동물의 경우, all-trans-retinal (ATR)을 식품에 보충하기도 한다. 미생물 옵신의 주요 장점은 척추 동물에서 외인성 보조 인자를 추가하지 않고도 완전히 기능한다는 것이다.[61]
광 응용 하드웨어: 뇌 깊숙한 곳에서도 특정 세포를 제어할 수 있도록 하는 하드웨어(통합된 광섬유 및 고체 광원 등)가 필요하다. 광섬유 결합 다이오드 기술이 가장 일반적으로 사용되지만,[59][60][61] 쥐 두개골에 이식된 투명하게 수정된 지르코니아로 만들어진 "창"을 새기는 방법도 고안되었다.[62] 대뇌 피질과 같은 뇌 표면 부위를 자극하기 위해 광섬유 또는 LED를 동물의 두개골에 직접 장착할 수 있다.[63] 더 깊은 뇌 부위에 빛을 전달하기 위해 이식된 광섬유가 사용된다.[63] 자유롭게 행동하는 유기체에서 복잡한 행동을 방해받지 않고 연구하기 위해 머리에 장착된 LED에 무선으로 전력을 공급하는 무선 기술도 개발되었다.[64]
광유전학 기술은 실험자의 필요에 따라 유연하게 적용할 수 있다. 양이온 선택 채널로돕신(예: ChR2)은 뉴런을 흥분시키는 데 사용되며, 음이온 전달 채널로돕신(예: GtACR2)은 뉴런 활동을 억제한다. 이러한 도구를 단일 구조체(예: BiPOLES)로 결합하면 조명의 파장에 따라 억제와 흥분을 모두 할 수 있다.[66]
광유전학은 밀리초 단위의 시간적 정밀도를 제공하여, 특정 활동 전위 패턴의 인과적 역할을 정의된 뉴런에서 조사할 수 있도록 한다.[45]
3. 1. 광 활성화 단백질: 채널, 펌프 및 효소
광유전학의 특징은 특정 표적화 메커니즘을 사용하여 세포 유형의 해상도를 유지하면서 전기적 및 생화학적 이벤트를 시간적으로 정확하게 조작할 수 있는 빠르고 광 활성화된 채널, 펌프 및 효소를 도입하는 것이다. 신경계의 기능을 조사하는 데 사용할 수 있는 미생물 옵신 중에는 뉴런을 흥분시키는 채널로돕신(ChR2, ChR1, VChR1, SFO)과 빛으로 유도된 억제를 위한 음이온 전도 채널로돕신이 있다.[46][47] 간접적으로 빛으로 제어되는 칼륨 채널은 최근 청색광 조명 동안 뉴런에서 활동 전위 생성을 방지하도록 설계되었다.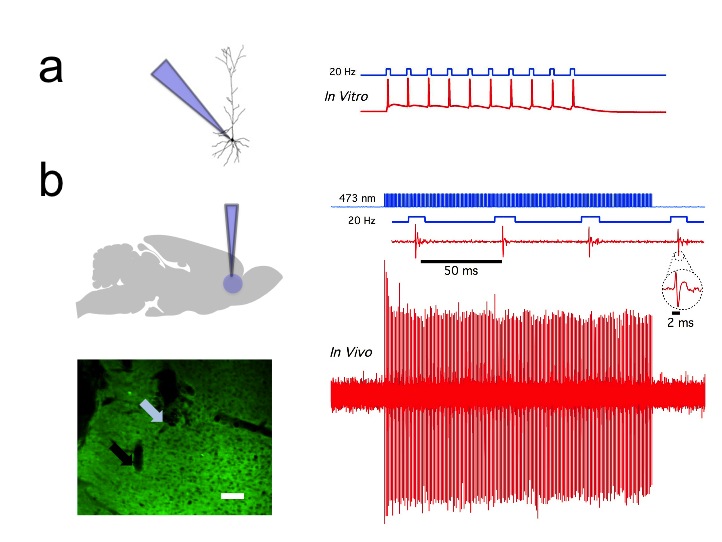
빛 구동 이온 펌프는 또한 뉴런 활성을 억제하는 데 사용된다. 예를 들어, 할로로돕신(NpHR),[48] 향상된 할로로돕신(eNpHR2.0 및 eNpHR3.0, 그림 2 참조),[49] 아르카에로돕신(Arch), 곰팡이 옵신(Mac) 및 향상된 박테리오로돕신(eBR)이 있다.[50]


행동하는 포유류 내에서 잘 정의된 생화학적 사건에 대한 광유전학적 제어도 가능하다. 척추동물 옵신을 특정 G 단백질 결합 수용체에 융합시키는 이전 작업에 기반하여,[51] 연구자들이 행동하는 포유류 내에서 표적 세포에서 cAMP 및 IP3와 같은 정의된 세포 내 메신저의 농도를 조작할 수 있도록 하는 일련의 키메라 단일 구성 요소 광유전학 도구가 생성되었다.[52] 다른 생화학적 광유전학 접근 방식(결정적으로 어둠 속에서 낮은 활성을 나타내는 도구를 사용하여)은 작은 GTPase 및 아데닐릴 시클라제를 광학적으로 제어하는 것이 여러 다른 실험실의 새로운 전략을 사용하여 배양된 세포에서 달성되었을 때 곧 이어졌다.[53][54][55] 광 활성화 아데닐릴 시클라제는 곰팡이에서 발견되었으며 포유류 뉴런에서 cAMP 수준을 제어하는 데 성공적으로 사용되었다.[56][57] 이 새로운 광유전학적 액추에이터의 레퍼토리는 이제 온전한 동물 내에서 세포 유형별로 시간적으로 정확한 여러 축의 세포 기능 제어를 허용한다.[58]
3. 2. 유전자 전달 기술
광유전학에서는 특정 세포에 옵신 유전자를 도입하는 것이 중요하다. 이를 위해 다양한 유전자 전달 기술이 사용된다.- 바이러스 벡터: 아데노 연관 바이러스(AAV)와 같은 바이러스 벡터를 이용하여 옵신 유전자를 특정 세포에 전달할 수 있다.[67]
- Cre-loxP 시스템: 크레 재조합효소(Cre recombinase)를 이용하는 방법이다. 특정 세포에서 크레 재조합효소를 발현하는 형질전환 동물 ("드라이버" 생쥐)을 이용하여, 두 개의 록스-P 부위 사이에 옵신 유전자를 삽입한 바이러스 벡터를 주입하면, 크레 재조합효소를 생성하는 세포에서만 옵신이 발현되도록 할 수 있다.[68] 이 방법을 사용하면 새로운 옵신을 사용할 때마다 형질전환 동물을 만들 필요가 없어 여러 종류의 변형된 광유전학적 도구를 사용할 수 있다.[68]
- 세포 특이적 프로모터: CAMKIIα와 같이 특정 유형의 세포에서만 활성화되는 프로모터를 이용하여, 해당 프로모터에 옵신 유전자를 연결하면 특정 세포 유형에서만 옵신을 발현시킬 수 있다. 예를 들어, CAMKIIα 프로모터는 흥분성 뉴런에서 활성화되므로, 이 프로모터를 사용하면 교세포가 아닌 흥분성 뉴런에서만 옵신이 발현되도록 할 수 있다.[67]
3. 3. 광학 자극 기술
광유전학에서는 빛을 이용하여 옵신을 활성화시켜 세포 활성을 조절한다. 이를 위해 광섬유, 발광 다이오드(LED), 다이오드 펌핑 고체 레이저(DPSS) 등 다양한 광원이 사용된다. 2007년에 도입된 광섬유 결합 다이오드 기술이 가장 일반적으로 사용되지만,[59][60][61] 쥐 두개골에 투명하게 수정된 지르코니아로 만들어진 "창"을 새겨 넣어 광파가 뇌 깊숙이 침투하여 개별 뉴런을 자극하거나 억제할 수 있도록 하는 방법도 개발되었다.[62]뇌 표면 부위를 자극하기 위해서는 광섬유나 LED를 동물의 두개골에 직접 장착할 수 있으며,[63] 더 깊은 뇌 부위에 빛을 전달하기 위해서는 광섬유를 이식한다.[63] 광섬유 외에도, 자유롭게 행동하는 유기체의 행동을 방해하지 않고 연구하기 위해 머리에 장착된 LED에 무선으로 전력을 공급하는 무선 기술도 개발되었다.[64]
광섬유를 기반으로 광 자극과 칼슘 영상을 결합하여,[63] 깨어있는 행동하는 동물에서 단일 뉴런의 활동을 시각화하고 조작할 수 있다.[71] 또한 외부에 위치한 광 검출기 및 광 자극기에 광섬유를 통해 연결된 굴절률 구배 렌즈(GRIN) 렌즈를 사용하여 여러 뇌 심부 영역에서 같은 방식으로 기록하는 것도 가능하다.[72][73]
최근에는 유기 LED(OLED)를 광유전학 자극에 활용하는 연구도 진행되고 있다.[171] 미생물 옵신을 발현하는 뉴런을 밀리초 단위로 정확하게 자극 제어하는 것이 In vitro에서 실증되었으며, 펄스 모드로 조작하여 적합한 저온 영역에서 신경을 자극할 수 있다. 유기 EL은 두께가 1μm 이하로 매우 얇아 뇌에 삽입하기에 적합하다.
4. 기술적 과제
광유전학 기술은 아직 해결해야 할 과제들을 안고 있다. 자유롭게 행동하는 동물의 뇌 심부 특정 유형의 세포를 제어하기 위한 하드웨어(통합된 광섬유나 고체 광원 등)가 필요하다. 2007년에 도입된[169] 광섬유 결합 다이오드 기술이 일반적으로 사용되지만, 매립 전극 없이 광파가 더 깊이 침투하여 개별 뉴런을 자극 또는 억제할 수 있도록 마우스 두개골에 투명한 지르코니아 "창"을 새기는 방법이 개발되었다.[170]
4. 1. 선택적 발현
최근에는 광유전학 자극으로 유기 LED(OLED)를 사용하는 연구가 진행되고 있다.[171] 미생물 옵신을 발현하는 뉴런을 밀리초(millisecond) 단위의 시간 척도로 정확하게 자극 제어하는 것이 In vitro에서 실증되었다. 또한, 펄스 모드에서의 조작을 통해 적합한 저온 영역에서의 신경 자극도 가능해졌다. 유기 EL은 두께가 1μm 이하로 극히 얇기 때문에 뇌에 매립하기에 적합하다.4. 2. 반응 속도 및 동기화
원래의 채널로돕신-2(channelrhodopsin-2)는 피질 뉴런의 전형적인 양이온 채널보다 닫히는 속도가 느려, 장기간의 탈분극 및 칼슘 유입을 유발했다.[76] 이후 더 유리한 운동성을 가진 많은 채널로돕신 변종들이 개발되었다.광유전학적 활성화는 펄스 조명 자극이 발현 뉴런의 동기적 활성화를 유발하여, 자극된 집단 내에서 순차적 활동의 가능성을 제거한다는 점에서 자연적인 스파이크 패턴과 차이가 있다. 따라서 영향을 받은 집단의 세포들이 서로 어떻게 소통하는지 또는 활성화의 위상적 특성이 회로 기능과 어떻게 관련되는지 이해하기 어렵다.
4. 3. 빛 흡수 스펙트럼
이 섹션은 주어진 원본 소스에 빛 흡수 스펙트럼에 대한 내용이 직접적으로 언급되지 않았기 때문에 요약문의 내용 또한 직접적인 연관성을 찾기 어렵습니다. 따라서 원본 소스에서 해당 섹션 제목과 관련된 내용을 찾을 수 없어, 섹션 내용을 작성할 수 없습니다.4. 4. 공간적 반응
광유전학적 활성화는 뇌의 신경 연결에 대한 철저한 지도인 커넥톰을 밝히기 위해 기능적 자기 공명 영상(fMRI)과 결합되었다.[74][77] 정확하게 시간을 맞춘 광유전학적 활성화는 fMRI의 기반이 되는 지연된 혈역학적 신호(BOLD)를 보정하는 데 사용된다.대뇌 피질 등 뇌의 표층부를 자극하기 위해 광섬유 또는 LED를 동물의 두개골에 직접 부착하는 경우가 있다. 또한, 광섬유를 더 깊이 매립함으로써 뇌의 더 깊은 영역에 빛을 전달하는 것도 가능하다. 광섬유를 통한 접근 방식 외에도 자유롭게 행동하는 생물의 복잡한 행동을 방해하지 않고 연구를 수행하기 위해 휴대용 LED에 무선으로 전력을 공급하는 무선 기술도 개발되고 있다.
최근에는 광유전학 자극으로 유기 LED(OLED)를 사용하는 연구가 진행되고 있다.[171] In vitro에서 미생물 옵신을 발현하는 뉴런을 밀리초(millisecond) 단위의 시간 척도로 정확하게 자극 제어하는 것이 실증되었다. 또한, 펄스 모드에서의 조작을 통해 적합한 저온 영역에서의 신경 자극도 가능해졌다. 더욱이, 유기 EL은 두께가 1μm 이하로 극히 얇기 때문에 뇌에 매립하기에 적합하다.
5. 응용 분야
광유전학은 신경과학, 심장학, 세포생물학 등 다양한 분야에서 활용될 가능성이 높은 기술이다.
광유전학은 특정 세포 유형이 생체 조직, 특히 신경 회로의 기능에 어떻게 기여하는지 밝히는 데 중요한 역할을 한다. 예를 들어, 파킨슨병[82][83], 자폐증, 조현병, 약물 남용, 불안, 우울증[50][84][85][86]과 같은 신경 및 정신 질환 연구에 새로운 통찰력을 제공하며, 빛을 이용한 회복 치료법 개발에도 기여하고 있다. 맹인을 위한 실험적 치료법으로는 특수 고글의 빛 패턴으로 자극받는 신경절 세포에 채널 로돕신을 발현시키는 방법이 연구되고 있다.[87][88]
광유전학은 현재 신경 회로, 질병, 행동, 세포 생물학 연구 등에서 활용되고 있다.
5. 1. 신경 회로 연구
광유전학은 특정 세포 유형이 생체 조직, 예를 들어 신경 회로의 기능에 어떻게 기여하는지 밝혀냈다.광유전학적 접근은 공포 조건화에 기여하는 편도체의 신경 회로를 매핑하는 데 사용되었다.[89][90][91][92] 쥐의 기저외측 편도체에서 등쪽-내측 전전두피질로 이어지는 연결에서 4Hz의 신경 진동이 관찰되었고, 파르발부민-Cre 프로모터가 부착된 채널로돕신-2를 도입하여 광학적으로 자극했을 때 동결 행동이 유발되었다.[93]
광유전학적 활성화를 통해 후각 감각 뉴런의 타이밍이 냄새 처리[94] 및 신경조절 매개 후각 유도 행동(예: 공격성, 짝짓기)에 중요함을 보였다.[95] 또한, 냄새의 "잔상"이 후각 수용체 뉴런이 위치하는 주변부보다는 후각망울을 중심으로 더 집중된다는 증거가 재현되었다.[96]
절편 생리학과 ''생체 내'' 전기 생리학을 광유전학과 통합하여 측좌핵의 콜린성 사이신경세포를 탐구했다. 이 세포는 도파민성 종말의 활동을 제어하며, 코카인 의존성 치료의 표적이 될 수 있다.[50][97]

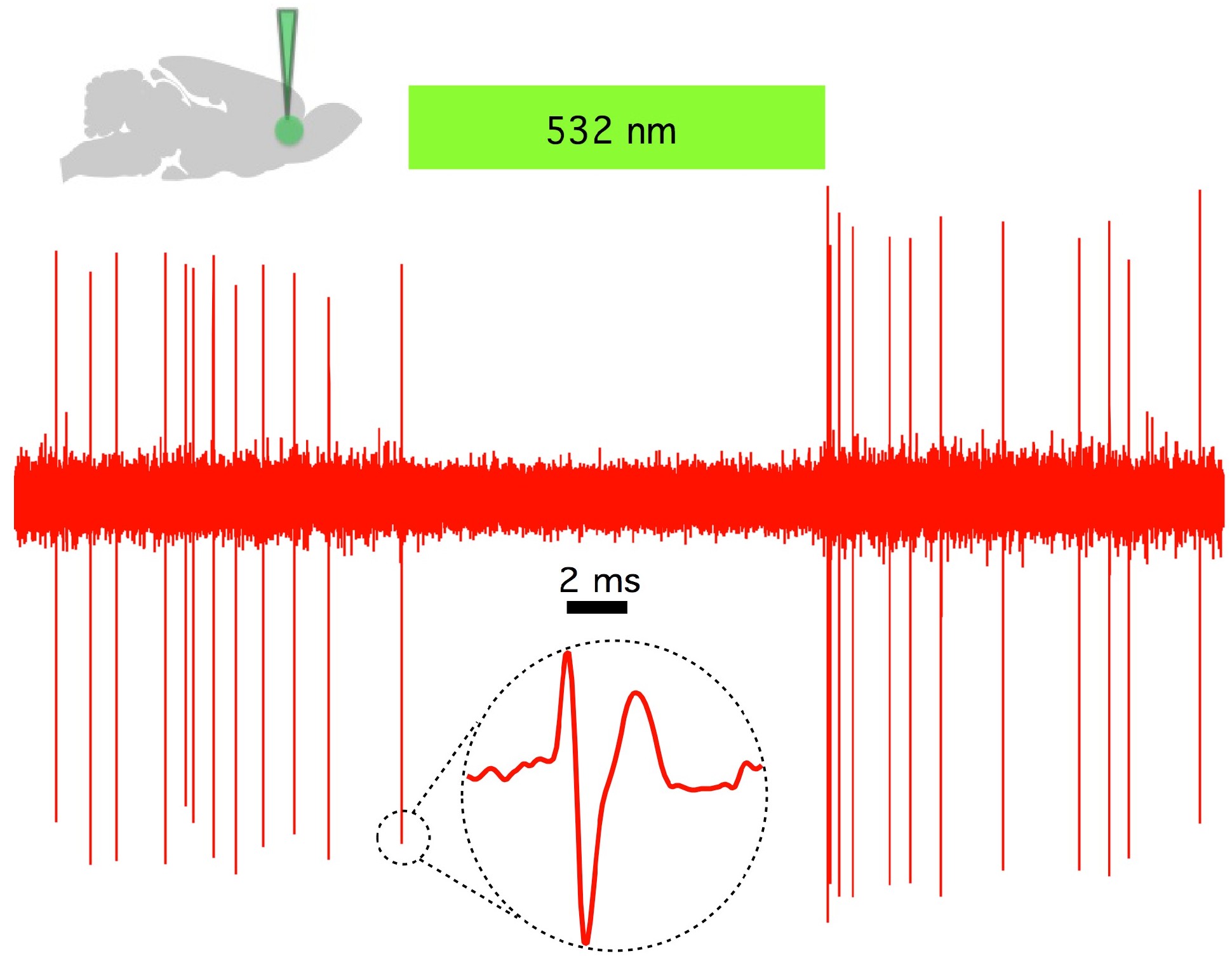
콜로라도 대학교 볼더 옵토생리학 연구소의 ''생체 내'' 및 ''생체 외'' 기록에 따르면, 전전두피질 내 CAMKII AAV-ChR2 발현 피라미드 신경세포는 20 Hz의 짧은 청색광 펄스로 높은 충실도의 활동 전위 출력을 보였다.[98]
'''운동 피질'''에서 건강한 동물의 ''생체 내'' 반복적인 광유전학적 자극은 결국 발작을 유발할 수 있었다.[99]
'''이상 피질'''에서 건강한 동물의 피라미드 세포에 대한 ''생체 내'' 반복적인 광유전학적 자극은 결국 발작을 유발할 수 있었으며, ''생체 외'' 연구에 따르면 GABA 합성이 손상되어 피드백 억제가 손실된 것으로 나타났다.[100]
현재 사용 가능한 광유전학적 작동기는 밀리초 수준의 정밀도로 표적 뉴런의 억제 또는 흥분을 제어할 수 있다.[122] 빛을 특정 행동 요소, 무조건 자극, 또는 뇌의 특정 진동 사건에 의해 트리거되도록 설계할 수 있다.[124][125]
5. 2. 질병 연구 및 치료
광유전학 기반 연구는 빛을 이용한 회복, 파킨슨병[82][83], 자폐증, 조현병, 약물 남용, 불안, 우울증과 같은 기타 신경 및 정신 질환에 대한 통찰력을 제공한다.[50][84][85][86] 맹목에 대한 실험적 치료법에는 엔지니어링된 고글의 빛 패턴으로 자극되는 신경절 세포에서 발현되는 채널 로돕신이 포함된다.[87][88]광유전학은 심방 심근 세포에 적용되어 심방 세동에서 발생하는 나선파 부정맥을 빛으로 종결시켰다.[101] 최근 연구에서는 부정맥을 교정하고 심장 박동을 재동기화하는 방법으로서 광유전학의 가능성을 탐구했다. 이 연구에서는 형질전환 마우스의 심실 부위에 있는 심근 세포에 채널로돕신-2를 도입하고, 개방강 및 폐쇄강 마우스에 대한 광자극의 ''시험관 내'' 연구를 수행했다. 광자극은 세포의 활성화를 증가시켜 심실 수축을 증가시켰고, 그 결과 심박수가 증가했다. 또한, 이 접근 방식은 전극 기반 CRT의 대체물로서 새로운 생물학적 심장 박동기인 심장 재동기화 치료(CRT)에 적용되었다.[102]
난청 생쥐의 나선 신경절에 대한 광유전학적 자극은 청각 활동을 회복시켰다.[106] 달팽이관 부위에 광유전학을 적용하면 나선 신경절 세포(SGN)를 자극하거나 억제할 수 있다. SGN의 휴지 전위 특성으로 인해 Chronos,[107] CatCh 및 f-Chrimson과 같은 단백질 채널로돕신-2의 다양한 변형이 사용되었다.[108]
얼굴신경운동핵에 발현된 변형된 적색광 여기성 채널로돕신(ReaChR)의 광유전학적 자극은 운동신경세포의 최소 침습적 활성화를 가능하게 하여 쥐의 수염 움직임을 유도하는 데 효과적이었다.[111]
5. 3. 행동 연구
광유전학으로 뉴런을 억제하거나 활성화하면 행동을 생성하는데 있어서 뉴런의 필요성과 충분성을 검증할 수 있다.[117] 연구자들은 이러한 접근 방식을 사용하여 운동 출력을 제어하는 신경 회로를 분석한다. 감각 운동 시스템의 다양한 지점에서 뉴런을 교란함으로써, 정형화된 행동을 유발하는 하행 뉴런의 역할,[118] 국소적인 촉각 감각 입력[119] 및 연접 뉴런의 활동[120]이 보행을 어떻게 변화시키는지, 그리고 푸르키니에 세포의 움직임 생성 및 조절 역할을 밝혀냈다.[121] 이는 동물 운동과 더 넓은 의미의 움직임에 대한 신경학적 기초를 이해하는 강력한 기술이다.현재 사용 가능한 광유전학적 작동기는 필요한 개입(표적 뉴런의 억제 또는 흥분)의 정확한 시간적 제어를 제공하며, 정밀도는 일반적으로 밀리초 수준까지 내려간다.[122] 그러나 시간적 정밀도는 광유전학적 작동기에 따라 다르며,[123] 자극의 주파수와 강도에 따라 달라진다.[78]
이제 개입에 사용되는 빛이 특정 행동 요소(행동 억제), 특정 무조건 자극(해당 자극에 무언가를 연관시키기 위해) 또는 뇌의 특정 진동 사건(사건 억제)에 의해 트리거되는 실험을 설계할 수 있다.[124][125] 이러한 종류의 접근 방식은 이미 여러 뇌 영역에서 사용되었다.
SWR는 기억 형성 및 공고화에 역할을 하는 것으로 여겨지는 해마에서 나타나는 뚜렷한 고주파 진동 현상이다. 이러한 현상은 온라인으로 기록된 국소 전위의 진동 주기를 추적하여 쉽게 감지할 수 있다. 이러한 방식으로 현상의 시작을 해마로 다시 유도되는 빛 섬광의 트리거 신호로 사용하여 SWR 동안 특정 뉴런을 억제하고, 또한 광유전학적으로 진동 자체를 억제할 수 있다.[126] 이러한 종류의 "폐쇄 루프" 실험은 SWR 복합체와 기억에서의 역할을 연구하는 데 유용하다.
5. 4. 세포 생물학 연구
채널로돕신-2와 같은 자연적인 빛 감지 이온 채널이 이온 흐름을 광학적으로 제어할 수 있게 하여 신경과학 분야에서 특히 유용하게 사용되는 것처럼, 자연적인 빛 제어 신호 전달 단백질은 생화학 경로, 특히 이차 전달자 생성과 단백질-단백질 상호 작용을 모두 광학적으로 제어할 수 있게 하여 세포 및 발생 생물학 연구에 특히 유용하다.[128] 2002년, 생화학 경로를 제어하기 위해 다른 유기체의 광단백질을 사용한 첫 번째 사례가 효모에서 식물 피토크롬과 피토크롬 상호 작용 인자(PIF) 간의 빛 유도 상호 작용을 사용하여 유전자 전사를 제어하는 방식으로 입증되었다.[1] 피토크롬을 DNA 결합 도메인에 융합하고 PIF를 전사 활성화 도메인에 융합함으로써 DNA 결합 도메인에 의해 인식되는 유전자의 전사 활성화를 빛에 의해 유도할 수 있었다.[1]
식물과 시아노박테리아에서 발견되는 피토크롬 외에도, 식물과 효모의 LOV 도메인(빛-산소-전압 감지 도메인)과 식물의 크립토크롬 도메인이 세포 내 생화학적 경로를 광학적으로 제어하는 데 사용된 또 다른 자연 광감지 도메인이다.[132][128] 또한, 형광 단백질 Dronpa로부터 생화학적 경로의 광학적 제어를 위해 합성 광감지 도메인이 설계되었다.[128] 광감지 도메인에서 빛 흡수는 단백질-단백질 상호 작용의 변화(피토크롬, 일부 LOV 도메인, 크립토크롬 및 Dronpa 돌연변이의 경우) 또는 연결된 단백질 세그먼트를 노출시키거나 연결된 단백질 도메인의 활성을 변경하는 구조 변화(피토크롬 및 일부 LOV 도메인의 경우)에 연결된다.[128] 빛에 의해 조절되는 단백질-단백질 상호 작용은 유전자 전사 또는 DNA 변형을 유도하거나, 예를 들어, 상주하는 신호 단백질을 활성화하기 위해, 예를 들어, 단백질을 DNA로, 또는 세포막으로 모집하는 데 사용될 수 있다.[127][133][134][135][136][137] CRY2 또한 활성화될 때 클러스터를 형성하므로 신호 도메인과 융합되어 광활성화되어 클러스터 기반 활성화를 허용한다.[138] ''Avena sativa''(귀리)의 LOV2 도메인은 빛 의존적 방식으로 짧은 펩타이드 또는 활성 단백질 도메인을 노출하는 데 사용되었다.[139][140][141] 이 LOV 도메인을 다른 단백질에 도입하면 빛 유도 펩타이드 장애를 통해 기능을 조절할 수 있다.[142] 펩타이드를 광유전학적으로 노출하는 asLOV2 단백질은 또한 여러 합성 빛 유도 이량체화 및 빛 유도 해리 시스템(각각 iLID 및 LOVTRAP)의 스캐폴드로 사용되었다.[143][144] 이 시스템은 단백질 분할 전략을 통해 단백질을 제어하는 데 사용될 수 있다.[145] 광분리성 Dronpa 도메인은 어둠 속에서 단백질 활성 부위를 가두고, 청록색 빛을 조사한 후 해제하고, 보라색 빛을 조사한 후 다시 가두는 데에도 사용되었다.[146]
신호 전달을 다양한 시간 동안 광학적으로 제어하는 능력은 세포 신호 전달 경로가 신호 지속 시간과 반응을 어떻게 다른 출력으로 변환하는지 규명하기 위해 연구되고 있다.[147] 자연 신호 전달 캐스케이드(cascade)는 자극 타이밍, 지속 시간 및 역학의 차이에 대해 서로 다른 출력으로 반응할 수 있다.[148] 예를 들어, PC12 세포를 상피 성장 인자(EGF, 일시적인 ERK 활성 프로파일 유도)로 처리하면 세포 증식이 일어나지만, 신경 성장 인자(NGF, 지속적인 ERK 활성 프로파일 유도)를 도입하면 신경 세포 유사 세포로 분화가 일어난다.[149] 이러한 현상은 처음에는 EGF와 NGF 적용을 사용하여 특징지어졌지만, 광학적 입력을 사용하여 부분적으로 복제되었다.[150] 또한, 광분리 가능한 Dronpa 도메인으로 조작된 광전환성 RAF의 맥동 활성을 사용하여 RAF-MEK-ERK 경로에서 빠른 음성 피드백 루프가 발견되었다.[146]
5. 5. 한국의 광유전학 응용 현황
광유전학 분야는 특정 세포 유형이 생체 조직, 예를 들어 ''생체 내'' 신경 회로의 기능에 어떻게 기여하는지에 대한 근본적인 과학적 이해를 증진시켰다. 임상 측면에서 광유전학 기반 연구는 빛을 이용한 회복, 파킨슨병[82][83], 자폐증, 조현병, 약물 남용, 불안, 우울증과 같은 기타 신경 및 정신 질환에 대한 통찰력으로 이어졌다.[50][84][85][86] 맹목에 대한 실험적 치료법에는 엔지니어링된 고글의 빛 패턴으로 자극되는 신경절 세포에서 발현되는 채널 로돕신이 포함된다.[87][88]6. 수상
광유전학 기술이 뇌 연구에 미치는 강력한 영향은 이 분야의 핵심 인물들에게 수많은 상을 수여함으로써 인정받았다.
2010년, 게오르크 나겔, 페터 헤게만, 에른스트 밤베르크는 와일리 생명 의학상(Wiley Prize in Biomedical Sciences)과 칼 하인츠 베크루츠 상(Karl Heinz Beckurts Prize)을 수상했다.[154][155] 같은 해, 칼 다이서로스는 "행동의 근본이 되는 신경 네트워크의 기능을 연구하기 위한 광유전학적 방법 개발에 대한 선구적인 연구"로 제1회 HFSP 나카소네상(HFSP Nakasone Award)을 수상했다.[156]
2012년, 밤베르크, 다이서로스, 헤게만, 게오르크 나겔은 막스 플랑크 협회(Max Planck Society)로부터 췰히 상(Zülch Prize)을 수상했으며,[157] 미젠뵈크는 "신경 활동을 조작하고 동물의 행동을 제어하는 광유전학적 접근법을 개척한 것"으로 Baillet Latour 건강 상(Baillet Latour Health Prize)을 수상했다.[158]
2013년, 게오르크 나겔과 헤게만은 루이-장테 의학상(Louis-Jeantet Prize for Medicine)을 수상했다.[159] 같은 해, 밤베르크, 보이든, 다이서로스, 헤게만, 미젠뵈크, 게오르크 나겔은 "광유전학의 발명 및 개선"으로 뇌상(The Brain Prize)을 공동 수상했다.[160][161]
2017년, 다이서로스는 "광유전학과 하이드로젤 조직 화학에서의 발견, 그리고 우울증의 신경 회로 기반에 대한 연구"로 엘제 크뢰너-프레제니우스 재단(Else Kröner-Fresenius Foundation) 연구상을 수상했다.[162]
2018년, 이나모리 재단(Inamori Foundation)은 다이서로스에게 "광유전학을 선도"하고 "시스템 신경과학 연구에 혁명을 일으킨" 공로로 교토상(Kyoto Prize)을 수여했다.[163]
2019년, 밤베르크, 보이든, 다이서로스, 헤게만, 미젠뵈크, 게오르크 나겔은 "광유전학의 발명과 개선에 관련된 특별한 공헌"을 인정받아 미국 예술 과학 아카데미(American Academy of Arts and Sciences)로부터 럼포드상(Rumford Prize)을 수상했다.[164]
2020년, 다이서로스는 광유전학과 하이드로젤 조직 화학을 개발한 공로로 네덜란드 왕립 예술 과학 아카데미(Royal Netherlands Academy of Arts and Sciences)로부터 하이네켄상(Heineken Prizes) 의학상을 수상했다.[165] 같은 해, 미젠뵈크, 헤게만, 게오르크 나겔은 쇼상(Shaw Prize) 생명 과학 및 의학 부문을 공동 수상했다.[166]
2021년, 헤게만, 다이서로스, 디터 오스터헬트는 앨버트 래스커 기초 의학 연구상(Albert Lasker Award for Basic Medical Research)을 수상했다.
참조
[1]
논문
A light-switchable gene promoter system
2002-10-01
[2]
논문
Flow of cortical activity underlying a tactile decision in mice
2014-01-01
[3]
논문
Dopaminergic and Prefrontal Basis of Learning from Sensory Confidence and Reward Value
2020-02-01
[4]
논문
Optogenetic stimulation of a hippocampal engram activates fear memory recall
2012-03-01
[5]
논문
Optogenetic Activation of the fruitless-Labeled Circuitry in Drosophila subobscura Males Induces Mating Motor Acts
2017-11-01
[6]
논문
Optogenetic strategies to dissect the neural circuits that underlie reward and addiction
2012-11-01
[7]
논문
Closed-loop optogenetic activation of peripheral or central neurons modulates feeding in freely moving Drosophila
2019-07-19
[8]
논문
Distributed control of motor circuits for backward walking in Drosophila
2020-12-02
[9]
논문
Optogenetic approaches for functional mouse brain mapping
2013
[10]
논문
Light Up the Brain: The Application of Optogenetics in Cell-Type Specific Dissection of Mouse Brain Circuits
2020
[11]
논문
Building a functional connectome of the Drosophila central complex
2018-08-20
[12]
논문
Functional architecture of neural circuits for leg proprioception in Drosophila
2021-12-06
[13]
논문
Optogenetics
2011-01-01
[14]
논문
Insights of the decade. Stepping away from the trees for a look at the forest. Introduction
2010-12-01
[15]
웹사이트
Method of the Year 2010: Optogenetics
https://www.youtube.[...]
2010-12-17
[16]
웹사이트
Optogenetics: Controlling the Brain with Light
http://www.scientifi[...]
Springer Nature America, Inc.
2010-10-20
[17]
논문
The impact of molecular biology on neuroscience
1999-12-01
[18]
논문
Photoactive mitochondria: in vivo transfer of a light-driven proton pump into the inner mitochondrial membrane of Schizosaccharomyces pombe
1994-09-01
[19]
논문
Selective photostimulation of genetically chARGed neurons
2002-01-01
[20]
논문
Photochemical gating of heterologous ion channels: remote control over genetically designated populations of neurons
2003-02-01
[21]
논문
Light-activated ion channels for remote control of neuronal firing
2004-12-01
[22]
논문
Allosteric control of an ionotropic glutamate receptor with an optical switch
2006-01-01
[23]
논문
Genetic control of neuronal activity in mice conditionally expressing TRPV1
2008-04-01
[24]
논문
Transient activation of specific neurons in mice by selective expression of the capsaicin receptor
2012-03-01
[25]
논문
Synaptic modifications in the medial prefrontal cortex in susceptibility and resilience to stress
2014-05-01
[26]
논문
Channelrhodopsin-2, a directly light-gated cation-selective membrane channel
2003-11-01
[27]
논문
Rhodopsin-regulated calcium currents in Chlamydomonas
1991-06-06
[28]
논문
Channelrhodopsin-1: a light-gated proton channel in green algae
2002-06-01
[29]
논문
Optogenetics: 10 years of microbial opsins in neuroscience
2015-09-01
[30]
논문
Millisecond-timescale, genetically targeted optical control of neural activity
2005-09-01
[31]
웹사이트
He may be the rightful inventor of neuroscience's biggest breakthrough in decades. But you've never heard of him
https://www.statnews[...]
2016-09-01
[32]
논문
Optogenetics: 10 years of microbial opsins in neuroscience
2015-08-26
[33]
논문
Ectopic expression of a microbial-type rhodopsin restores visual responses in mice with photoreceptor degeneration
2006-04-01
[34]
논문
Remote control of behavior through genetically targeted photostimulation of neurons
2005-04-01
[35]
논문
Fast noninvasive activation and inhibition of neural and network activity by vertebrate rhodopsin and green algae channelrhodopsin
2005-12-01
[36]
논문
Light activation of channelrhodopsin-2 in excitable cells of Caenorhabditis elegans triggers rapid behavioral responses
2005-12-00
[37]
논문
Subregion- and cell type-restricted gene knockout in mouse brain
1996-12-00
[38]
논문
Cre-Lox Neurogenetics: 20 Years of Versatile Applications in Brain Research and Counting...
[39]
논문
Multiple-color optical activation, silencing, and desynchronization of neural activity, with single-spike temporal resolution
Public Library of Science
2007-03-00
[40]
논문
Multimodal fast optical interrogation of neural circuitry
2007-04-00
[41]
논문
Fast manipulation of cellular cAMP level by light in vivo
http://edoc.hu-berli[...]
2007-01-00
[42]
논문
Optogenetic manipulation of cGMP in cells and animals by the tightly light-regulated guanylyl-cyclase opsin CyclOp
2015-09-00
[43]
논문
Microbial light-activatable proton pumps as neuronal inhibitors to functionally dissect neuronal networks in C. elegans
[44]
논문
A cholinergic-regulated circuit coordinates the maintenance and bi-stable states of a sensory-motor behavior during Caenorhabditis elegans male copulation
2011-03-00
[45]
뉴스
Optogenetics: Controlling the Brain with Light [Extended Version]
https://www.scientif[...]
2016-11-28
[46]
논문
Synthetic Light-Activated Ion Channels for Optogenetic Activation and Inhibition
2018-00-00
[47]
논문
Potassium channel-based two component optogenetic tool for silencing of excitable cells
2018-11-00
[48]
논문
Improved expression of halorhodopsin for light-induced silencing of neuronal activity
2008-08-00
[49]
논문
eNpHR: a Natronomonas halorhodopsin enhanced for optogenetic applications
2008-08-00
[50]
논문
Cholinergic interneurons control local circuit activity and cocaine conditioning
2010-12-00
[51]
논문
Light-driven activation of beta 2-adrenergic receptor signaling by a chimeric rhodopsin containing the beta 2-adrenergic receptor cytoplasmic loops
2005-02-00
[52]
논문
Temporally precise in vivo control of intracellular signalling
2009-04-00
[53]
논문
Spatiotemporal control of cell signalling using a light-switchable protein interaction
2009-10-00
[54]
논문
A genetically encoded photoactivatable Rac controls the motility of living cells
2009-09-00
[55]
논문
Induction of protein-protein interactions in live cells using light
2009-10-00
[56]
논문
Light modulation of cellular cAMP by a small bacterial photoactivated adenylyl cyclase, bPAC, of the soil bacterium Beggiatoa
2011-01-00
[57]
논문
Natural and engineered photoactivated nucleotidyl cyclases for optogenetic applications
2010-12-00
[58]
논문
Communication in Neural Circuits: Tools, Opportunities, and Challenges
2016-03-00
[59]
논문
An optical neural interface: in vivo control of rodent motor cortex with integrated fiberoptic and optogenetic technology
2007-09-00
[60]
논문
Neural substrates of awakening probed with optogenetic control of hypocretin neurons
2007-11-00
[61]
논문
Targeting and readout strategies for fast optical neural control in vitro and in vivo
2007-12-00
[62]
논문
Transparent nanocrystalline yttria-stabilized-zirconia calvarium prosthesis
https://escholarship[...]
2013-11-00
[63]
논문
Fiber photometry in striatum reflects primarily nonsomatic changes in calcium
2022-08-30
[64]
논문
A wirelessly powered and controlled device for optical neural control of freely-behaving animals
2011-08-00
[65]
논문
Optogenetics as a neuromodulation tool in cognitive neuroscience
2013-01-01
[66]
논문
BiPOLES is an optogenetic tool developed for bidirectional dual-color control of neurons
2021-07-26
[67]
논문
Optogenetic interrogation of neural circuits: technology for probing mammalian brain structures
2010-03-00
[68]
서적
Optogenetics: Tools for Controlling and Monitoring Neuronal Activity
2012-09-05
[69]
논문
Optical neural interfaces
2014-07-00
[70]
논문
Making Sense of Optogenetics
2015-07-00
[71]
웹사이트
The Evolution in Freely-Behaving Imaging and Optogenetics Technology
https://www.mightexb[...]
Mightex
2021-06-03
[72]
논문
Deep brain optical measurements of cell type-specific neural activity in behaving mice
2016-04-00
[73]
논문
Deep brain optical measurements of cell type-specific neural activity in behaving mice
2014-06-00
[74]
웹사이트
Current Challenges in Optogenetics
https://www.sfn.org/[...]
2013-00-00
[75]
논문
Optogenetic Stimulation Shifts the Excitability of Cerebral Cortex from Type I to Type II: Oscillation Onset and Wave Propagation
2017-01-00
[76]
논문
Optical induction of synaptic plasticity using a light-sensitive channel
http://www.nature.co[...]
2007-00-00
[77]
논문
Mapping the connectome: multi-level analysis of brain connectivity
2012-05-01
[78]
논문
Nonlinear response characteristics of neural networks and single neurons undergoing optogenetic excitation
2020-09-00
[79]
웹사이트
PyRhO: a virtual optogenetics laboratory
https://github.com/P[...]
[80]
웹사이트
Simulation tool for neural networks and single neurons with light-sensitive channels
https://github.com/j[...]
[81]
논문
Spread of activation and interaction between channels with multi-channel optogenetic stimulation in the mouse cochlea
2023-12-00
[82]
논문
Regulation of parkinsonian motor behaviours by optogenetic control of basal ganglia circuitry
2010-07-00
[83]
논문
Optical deconstruction of parkinsonian neural circuitry
2009-04-00
[84]
논문
Driving fast-spiking cells induces gamma rhythm and controls sensory responses
2009-06-00
[85]
논문
Parvalbumin neurons and gamma rhythms enhance cortical circuit performance
2009-06-00
[86]
논문
Phasic firing in dopaminergic neurons is sufficient for behavioral conditioning
2009-05-00
[87]
뉴스
Scientists Partially Restored a Blind Man's Sight With New Gene Therapy
https://www.nytimes.[...]
2021-05-24
[88]
논문
Partial recovery of visual function in a blind patient after optogenetic therapy
2021-07-00
[89]
논문
Genetic dissection of an amygdala microcircuit that gates conditioned fear
2010-11-00
[90]
논문
Optical activation of lateral amygdala pyramidal cells instructs associative fear learning
2010-07-00
[91]
논문
Thy1-expressing neurons in the basolateral amygdala may mediate fear inhibition
2013-06-00
[92]
논문
Towards new approaches to disorders of fear and anxiety
2013-06-00
[93]
논문
4-Hz oscillations synchronize prefrontal-amygdala circuits during fear behavior
2016-04-00
[94]
논문
Precise olfactory responses tile the sniff cycle
2011-07-00
[95]
논문
Differential Muscarinic Modulation in the Olfactory Bulb
2015-07-00
[96]
논문
Odor representations in the olfactory bulb evolve after the first breath and persist as an odor afterimage
2013-08-00
[97]
논문
Glutamatergic signaling by mesolimbic dopamine neurons in the nucleus accumbens
2010-05-00
[98]
논문
Optogenetic control of genetically-targeted pyramidal neuron activity in prefrontal cortex
http://precedings.na[...]
2012-04-02
[99]
논문
An Optogenetic Kindling Model of Neocortical Epilepsy
2019-03-00
[100]
논문
Chronic loss of inhibition in piriform cortex following brief, daily optogenetic stimulation
2021-04-00
[101]
논문
Light-induced termination of spiral wave arrhythmias by optogenetic engineering of atrial cardiomyocytes
2014-10-00
[102]
논문
Optogenetics for in vivo cardiac pacing and resynchronization therapies
2015-07-00
[103]
논문
Optogenetic termination of ventricular arrhythmias in the whole heart: towards biological cardiac rhythm management
2017-07-00
[104]
논문
Optogenetic defibrillation terminates ventricular arrhythmia in mouse hearts and human simulations
2016-10-00
[105]
논문
Optogenetics design of mechanistically-based stimulation patterns for cardiac defibrillation
2016-10-00
[106]
논문
Optogenetic stimulation of the auditory pathway
2014-03-01
[107]
논문
Ultrafast optogenetic stimulation of the auditory pathway by targeting-optimized Chronos
2018-12-01
[108]
논문
High frequency neural spiking and auditory signaling by ultrafast red-shifted optogenetics
2018-05-01
[109]
웹사이트
Engineering long-wavelength light-driven ion channels to hear the light. Atlas of Science
https://atlasofscien[...]
2019-11-07
[110]
논문
Optogenetic stimulation of the auditory pathway for research and future prosthetics
2015-10-01
[111]
논문
ReaChR: a red-shifted variant of channelrhodopsin enables deep transcranial optogenetic excitation
2013-10-01
[112]
논문
Dorsal Raphe Dopamine Neurons Represent the Experience of Social Isolation
2016-02-01
[113]
논문
Independent optical excitation of distinct neural populations
2014-03-01
[114]
논문
Bi-stable neural state switches
2009-02-01
[115]
논문
NEUROSCIENCE. Natural light-gated anion channels: A family of microbial rhodopsins for advanced optogenetics
2015-08-01
[116]
논문
Optogenetic Neuronal Silencing in Drosophila during Visual Processing
2017-10-01
[117]
논문
Optogenetics in a transparent animal: circuit function in the larval zebrafish
2013-02-01
[118]
논문
Optogenetic dissection of descending behavioral control in Drosophila
2018-06-26
[119]
논문
Spatiotemporally precise optogenetic activation of sensory neurons in freely walking Drosophila
2020-04-22
[120]
논문
Two Brain Pathways Initiate Distinct Forward Walking Programs in Drosophila
2020-11-11
[121]
논문
Precise Control of Movement Kinematics by Optogenetic Inhibition of Purkinje Cell Activity
https://www.jneurosc[...]
2014-02-05
[122]
논문
Open Source Tools for Temporally Controlled Rodent Behavior Suitable for Electrophysiology and Optogenetic Manipulations
2018-05-01
[123]
논문
A user's guide to channelrhodopsin variants: features, limitations and future developments
2011-01-01
[124]
논문
Closed-Loop and Activity-Guided Optogenetic Control
2015-04-08
[125]
논문
Closed-loop optogenetic intervention in mice
2013-01-01
[126]
논문
Optogenetically Blocking Sharp Wave Ripple Events in Sleep Does Not Interfere with the Formation of Stable Spatial Representation in the CA1 Area of the Hippocampus
2016-11-19
[127]
논문
Optogenetic control of cellular forces and mechanotransduction
2017-02-01
[128]
논문
Applications of Optobiology in Intact Cells and Multicellular Organisms
2017-10-01
[129]
논문
The development and application of optogenetics
2011-01-01
[130]
Youtube
Method of the Year 2010: Optogenetics
https://www.youtube.[...]
2010-12-17
[131]
웹사이트
optogenetics - Search Results
https://pubmed.ncbi.[...]
2020-02-29
[132]
논문
Lights, cytoskeleton, action: Optogenetic control of cell dynamics
Elsevier Ltd.
2020-10-01
[133]
논문
Optical control of mammalian endogenous transcription and epigenetic states
2013-08-01
[134]
논문
Genetically encoded photoswitching of actin assembly through the Cdc42-WASP-Arp2/3 complex pathway
2008-09-01
[135]
논문
Light-based feedback for controlling intracellular signaling dynamics
2011-09-01
[136]
논문
TULIPs: tunable, light-controlled interacting protein tags for cell biology
2012-03-01
[137]
논문
Optogenetic control of phosphoinositide metabolism
2012-08-01
[138]
논문
Optogenetic protein clustering and signaling activation in mammalian cells
2013-03-01
[139]
논문
Designing photoswitchable peptides using the AsLOV2 domain
2012-04-01
[140]
논문
A genetically encoded photoactivatable Rac controls the motility of living cells
2009-09-01
[141]
저널
Engineering a light-activated caspase-3 for precise ablation of neurons in vivo
2017-09-00
[142]
저널
Engineering extrinsic disorder to control protein activity in living cells
2016-12-00
[143]
저널
Engineering an improved light-induced dimer (iLID) for controlling the localization and activity of signaling proteins
2015-01-00
[144]
저널
LOVTRAP: an optogenetic system for photoinduced protein dissociation
2016-09-00
[145]
저널
Local control of intracellular microtubule dynamics by EB1 photodissociation
Nature Research.
2018-03-00
[146]
저널
Optical control of protein activity by fluorescent protein domains
2012-11-00
[147]
저널
Illuminating cell signalling with optogenetic tools
2014-08-00
[148]
저널
Encoding and decoding cellular information through signaling dynamics
2013-02-00
[149]
저널
Growth factor-induced MAPK network topology shapes Erk response determining PC-12 cell fate
2007-03-00
[150]
저널
Using optogenetics to interrogate the dynamic control of signal transmission by the Ras/Erk module
2013-12-00
[151]
저널
Brownian Optogenetic-Noise-Photostimulation on the Brain Amplifies Somatosensory-Evoked Field Potentials
2017-00-00
[152]
저널
Optogenetic noise-photostimulation on the brain increases somatosensory spike firing responses
2018-01-00
[153]
저널
Noisy Light Augments the Na+ Current in Somatosensory Pyramidal Neurons of Optogenetic Transgenic Mice
2020-00-00
[154]
웹사이트
Ninth Annual Wiley Prize in Biomedical Sciences Awarded to Dr. Peter Hegemann, Dr. Georg Nagel, and Dr. Ernst Bamberg
http://eu.wiley.com/[...]
[155]
웹사이트
Karl Heinz Beckurts-Preis 2010
https://www.beckurts[...]
[156]
웹사이트
HFSP Nakasone Award 2010
https://www.hfsp.org[...]
[157]
웹사이트
International Prize for Translational Neuroscience of the Gertrud Reemtsma Foundation (K.J. Zülch Prize until 2019)
https://www.mpg.de/p[...]
[158]
웹사이트
InBev-Baillet Latour International Health Prize
https://www.frs-fnrs[...]
[159]
웹사이트
Louis-Jeantet Prize
https://www.jeantet.[...]
[160]
웹사이트
The Brain Prize 2013
http://www.thebrainp[...]
2013-10-03
[161]
저널
The Brain Prize 2013: the optogenetics revolution
2013-10-00
[162]
웹사이트
Else Kröner Fresenius Prize for Medical Research 2017
http://ekfs.de/en/sc[...]
[163]
웹사이트
2018 Kyoto Prize Laureate Karl Deisseroth
https://kyotoprize.o[...]
[164]
웹사이트
Rumford Prize Awarded for the Invention and Refinement of Optogenetics
https://www.amacad.o[...]
2019-01-30
[165]
웹사이트
2020 Heineken Prize Laureate Karl Deisseroth
https://www.heineken[...]
[166]
웹사이트
2020 Shaw Prize Laureates Miesenböck, Hegemann and Georg Nagel
https://www.shawpriz[...]
[167]
서적
依存症の科学 いちばん身近なこころの病
化学同人
[168]
웹사이트
Method of the Year 2010
http://www.nature.co[...]
[169]
저널
An optical neural interface: in vivo control of rodent motor cortex with integrated fiberoptic and optogenetic technology
https://iopscience.i[...]
2007-09-01
[170]
저널
Transparent nanocrystalline yttria-stabilized-zirconia calvarium prosthesis
https://linkinghub.e[...]
2013-11-00
[171]
저널
Sub-millisecond Control of Neuronal Firing by Organic Light-Emitting Diodes
https://www.frontier[...]
2019-10-22
[172]
저널
Next-Generation Optical Technologies for Illuminating Genetically Targeted Brain Circuits
[173]
저널
2010-00-00
[174]
저널
Single-molecule fluorimetry and gating currents inspire an improved optical voltage indicator
2015-00-00
관련 사건 타임라인
( 최근 20개의 뉴스만 표기 됩니다. )
"치매에도 날 기억한 할머니"…알츠하이머 단초 찾는 연구됐다
본 사이트는 AI가 위키백과와 뉴스 기사,정부 간행물,학술 논문등을 바탕으로 정보를 가공하여 제공하는 백과사전형 서비스입니다.
모든 문서는 AI에 의해 자동 생성되며, CC BY-SA 4.0 라이선스에 따라 이용할 수 있습니다.
하지만, 위키백과나 뉴스 기사 자체에 오류, 부정확한 정보, 또는 가짜 뉴스가 포함될 수 있으며, AI는 이러한 내용을 완벽하게 걸러내지 못할 수 있습니다.
따라서 제공되는 정보에 일부 오류나 편향이 있을 수 있으므로, 중요한 정보는 반드시 다른 출처를 통해 교차 검증하시기 바랍니다.
문의하기 : help@durumis.com