근염
"오늘의AI위키"의 AI를 통해 더욱 풍부하고 폭넓은 지식 경험을 누리세요.
- 1. 개요
- 2. 종류
- 3. 역사
- 4. 역학
- 5. 원인
- 6. 병태
- 7. 증상
- 8. 진단
- 9. 감별 진단
- 10. 치료
- 11. 각론
- 참조
1. 개요
근염은 근육에 염증이 생기는 질환을 통칭하며, 다양한 종류가 존재한다. 원인으로는 부상, 약물, 감염, 유전 질환, 자가면역 질환 등이 있으며, 특발성인 경우도 있다. 근염은 다발근염, 피부근염, 봉입체 근염 등 하위 유형으로 분류되며, 각각의 특징적인 증상, 진단 방법, 치료법을 가진다. 자가면역성 근염은 전신 쇠약감, 근력 저하, 특징적인 피부 발진 등을 동반할 수 있으며, 혈액 검사, 근전도 검사, 근육 생검 등을 통해 진단한다. 치료는 근본 원인에 따라 다르며, 자가면역성 근염의 경우 글루코코르티코이드, 면역억제제, 생물학적 제제 등이 사용된다. 한국에서는 후생노동성 진단 기준이 자주 사용되며, 피부근염, 항합성효소 증후군 등 각 유형별로 특이적인 자가항체가 존재한다.
더 읽어볼만한 페이지
- 근육 질환 - 근위축증
근위축증은 골격근의 양이 감소하는 상태로, 부동, 악액질 등 다양한 원인에 의해 발생하며, 근육량 감소와 쇠약을 특징으로 하고, 운동, 영양, 약물 치료를 통해 관리한다. - 근육 질환 - 쥐 (의학)
쥐(의학)은 다양한 원인으로 발생하는 근육의 비자발적 수축 현상으로, 스트레칭, 마사지 등으로 치료하고 컨디셔닝, 수분 및 전해질 균형 유지로 예방할 수 있다. - 염증 - 신장염
신장염은 콩팥에 발생한 염증으로, 자가면역질환, 요로감염, 루푸스, 격렬한 운동 등이 원인이 되어 혈뇨, 핍뇨, 요독증, 고혈압 등의 증상을 유발하며, 혈액 검사, X레이, 초음파 등으로 진단하고 원인에 따라 치료한다. - 염증 - 신우신염
신우신염은 신장의 신우와 신실질에 발생하는 감염으로, 급성(고열, 배뇨통, 옆구리 통증)과 만성(지속적인 옆구리 통증, 체중 감소)으로 나뉘며, 대장균과 장구균이 주요 원인균이고, 항생제로 치료하며, 요로의 구조적 이상, 당뇨병, 면역 저하 등이 위험 요인이다.
| 근염 | |
|---|---|
| 질병 개요 | |
| 분야 | 류머티스학 |
| 증상 | 미정 |
| 합병증 | 확대된 근골격계 통증 증후군 |
| 발병 시기 | 미정 |
| 지속 기간 | 미정 |
| 유형 | 미정 |
| 원인 | 자가면역 특발성 약물 부작용 |
| 위험 요인 | 미정 |
| 진단 | 미정 |
| 감별 진단 | 미정 |
| 예방 | 미정 |
| 치료 | 미정 |
| 약물 | 미정 |
| 예후 | 미정 |
| 빈도 | 미정 |
| 사망률 | 미정 |
| 식별 | |
| 질병 데이터베이스 | 29473 |
| 국제질병분류 (ICD-10) | M60 |
| 국제질병분류 (ICD-9) | 729.1 |
| 온라인 멘델 유전형질 데이터베이스 (OMIM) | 160750 |
| 엠디라인플러스 | 001245 |
| 메시 ID | D009220 |
| 추가 정보 | |
| 관련 문서 | 근육염 관련 메들라인플러스 |
2. 종류
- 화골성근염
- (특발성) 염증성 근육병증
- * 피부근염
- ** 연소성 피부근육염
- * 다발성 근염
- * 포함체 근육염
- * BACM (benign acute childhood myositis|소아 급성 양성 근염영어)
- * Statin-associated autoimmune myopathy|스타틴 연관 자가면역 근병증영어
- 고름근육염
3. 역사
1975년에 발표된 보한과 피터(Bohan and Peter)의 진단 기준에 따라 오랫동안 발진이 있는 피부근염과 발진이 없는 다발근염(polymyositis)으로 분류되었다.[12][13] 교원병 내과나 피부과학 영역에서는 다발(poly)과 다발성(multi)의 구별이 이루어지지 않아 다발근염을 다발성근염으로 기재하는 경우도 있다.
이후, 근염 특이 자가항체(MSA)와 다른 교원병에서도 발견되는 근염 관련 자가항체(MAA)에 관한 지견 및 근병리 소견의 특징이 밝혀졌다. 2003년에 Dalalas와 Hohfeld가 염증성 근 질환에서 봉입체근염을 제외한 다음, 발진 유무와 근병리를 중시한 다발근염과 피부근염의 진단 기준을 작성했다.[14] 2004년 유럽 신경근 센터(ENMC) 워크숍에서는 피부근염, 다발근염, 봉입체근염, 면역매개성 괴사성 미오파티, 비특이성 근염의 5가지로 분류하는 ENMC 분류 기준을 작성했다.[15] 2014년 유럽 신경근 센터 워크숍에서는 항합성효소 증후군(ASS)이 독립적인 하위 유형으로 추가되었다.[16]
2018년에는 피부근염의 진단 기준도 개정되었다.[17] 믹소바이러스 저항성 단백질 A(MxA)는 Ⅰ형 인터페론으로 유도되는 대표적인 단백질이다. 골격근의 근섬유에서 MxA의 발현은 근속 변연부 위축보다 피부근염의 진단에서 감도·특이도가 모두 뛰어나 2018년 개정으로 진단 기준에도 포함되게 되었다. 피부근염은 전신성 홍반성 루푸스나 류마티스 관절염과 함께 Ⅰ형 인터페로노파티로 인식되게 되었다.
임상적으로 다발근염으로 진단되는 예의 대부분이 근병리학적으로는 면역매개성 괴사성 미오파티이며, 다발근염의 조직학적 정의는 "CD8 양성 T세포의 근내막 및 비괴사성 섬유 내부로의 침윤을 동반"이라는 것이지만, 이를 엄밀하게 채택하면 다발근염으로 병리 진단되는 예는 거의 없어졌다. 종래 다발근염으로 병리 진단되어 온 예의 대부분은 봉입체근염이었다.[18] 그 때문에, 자가면역성 근염은 피부근염, 항합성효소 증후군, 봉입체근염, 면역매개성 괴사성 미오파티의 4가지 하위 유형으로 분류되게 되었다.
자가면역성 근염은 교원병 내과, 피부과, 소아과, 뇌신경내과 등 다양한 진료과에서 진료된다. 2004년 위 4개과의 역학자, 생물 통계학자들이 모여 국제 근염 분류 기준 프로젝트(IMCCP)를 결성하고, 새로운 국제 근염 분류 기준을 책정하게 되었다. 그 결과는 유럽 류마티스 학회, 미국 류마티스 학회에 의해 2017년에 승인되었다.[19] 국제 진단 기준에서는 무근증성 피부근염(ADM)의 정의가 변경된 점에 주의해야 한다. 국제 진단 기준에서는 근력 저하를 인정하지 않고, 피부근염에 전형적인 발진을 가진 증례는 모두 ADM이라고 부른다.
4. 역학
일본에서 다발근염 및 피부근염 환자는 약 17,000명이며, 매년 1,500명씩 증가하고 있다. 남녀 비율은 1:2.7로 여성에게 더 많이 발생하며, 중년기에 발병하는 경우가 많다. 초기부터 간질성 폐렴 합병증이 과반수에서 나타난다.[1]
5. 원인
근염은 부상, 특정 약물, 감염, 유전 근육 질환 또는 자가면역 질환을 포함한 다양한 원인으로 발생할 수 있다. 어떤 경우에는 뚜렷한 원인 없이 특발성 질환으로 남기도 한다.
- 부상: 심한 운동으로 경미한 형태의 근염이 발생할 수 있다.[4] 횡문근융해증이라고 하는 더 심각한 형태의 근육 부상 또한 근염과 관련이 있는데,[4] 이는 환자의 근육 부상으로 인해 근육이 빠르게 파괴되는 상태이다.[4]
- 약물: 다양한 약물이 근염을 유발할 수 있다. 가장 흔한 유형 중 하나는 콜레스테롤 수치를 낮추는 데 사용되는 스타틴이다. 스타틴 치료의 가장 흔한 부작용 중 하나는 근육통[5]이며, 드물게 근염으로 이어질 수 있다.[5]
- 감염: 근염의 가장 흔한 감염성 원인은 바이러스 감염이며, 일반적인 감기를 예로 들 수 있다.[4] 코로나19와 같은 다른 바이러스도 근염의 드문 원인이 된다.[6] 양성 급성 소아 근염은 다른 바이러스성 병원체로 전구 바이러스 감염 후 소아에서 기술되었다. 세균 감염, 기생충 감염, 진균 감염은 근염의 다른 감염성 원인이다.[7]
- 유전 근육 질환: 많은 유전성 근병증은 칼파이노병증, 디스페린병증, 얼굴어깨상완 근이영양증, 디스트로피노병증 및 ''LMNA'' 관련 근병증을 포함하여 이차적인 근염을 가질 수 있다.[8]
- 자가면역: 자가면역 질환은 특정 신체 단백질 또는 근육 중 하나와 같은 다른 생체 분자 표적에 대한 비정상적인 면역 반응이다. 일반적으로 자가항체에 대해 양성 반응을 보이는 세 가지 주요 유형의 특발성 근염 (염증성 근병증으로 알려짐)은 피부근염, 다발성 근염 및 봉입체 근염이다.[4] 전신성 홍반성 루푸스와 같은 다른 자가면역 질환도 근염 유사 증상을 유발할 수 있다.[4]
6. 병태
자가면역 근염은 다양한 정도의 근염, 특징적인 피부 증상, 간질성 폐렴을 동반하는 스펙트럼이다. 암의 전이를 설명하는 "씨앗과 토양 이론(Seed and Soil model)"은 여러 장기에 증상을 나타내는 염증성 근질환에도 적용할 수 있다. 세포 독성 T 세포 등 면역 세포를 씨앗으로 간주하고, 토양으로서의 조건이 갖춰진 특정 장기로 집중적으로 이동하여 염증을 일으켜, 그 전체상이 자가면역 질환을 이룬다는 관점이다.
근원성 변화는 염증성 근육 질환 외에 근육병증 등에서도 나타나는 소견이다. 근섬유 직경의 크기는 크고 작음이 일정하지 않으며, 근섬유의 형태는 원형화된다. 만성 경과 사례에서는 100μm 이상의 비대 섬유가 관찰되며, 근내막이 확장되고 간질의 확장 및 섬유화를 보이기도 한다. 섬유의 중심부에 핵이 있는, 이른바 중심핵을 보이는 경우도 많다. 괴사·재생 근육이 관찰된다. NADH-TR 염색에서는 근원 섬유간 망의 혼란이 관찰되며 AcidP 염색에서는 재생 섬유에서 활성의 상승이 관찰된다.
7. 증상
자가면역 근염은 전신 쇠약감, 발열, 체중 감소와 같은 전신 증상을 동반할 수 있다. 체중 감소는 근육량 감소나 음식 섭취의 어려움(연하 장애)으로 인해 나타날 수 있다.[20]
근력 저하 증상은 점진적으로 나타나며, 주로 몸통과 가까운 팔다리 근육(사지 근위 근육), 목 근육(경부 굴근), 인두 근육이 영향을 받는다. 이로 인해 침대에서 일어나거나, 앉았다 일어서기, 계단 오르내리기, 머리 빗기(상지 거상) 등의 일상생활 동작이 어려워질 수 있다. 인두 근육이 손상되면 삼킴 장애(연하 장애)나 발성 장애가 발생하여 흡인성 폐렴을 유발할 수도 있다. 항합성 효소 증후군에서는 관절통이 동반되기도 한다.[20]
피부근염에서는 쾨브너 현상이 나타날 수 있는데, 이는 정상 피부에 긁힘, 외상, 염증 등의 자극이 가해진 후 해당 부위에 원래 질병과 같은 피부 증상이 나타나는 것을 말한다. 고트론 구진·고트론 징후, 헬리오트로프 발진, 메카닉스 핸드 등이 쾨브너 현상의 예시이다.[20]
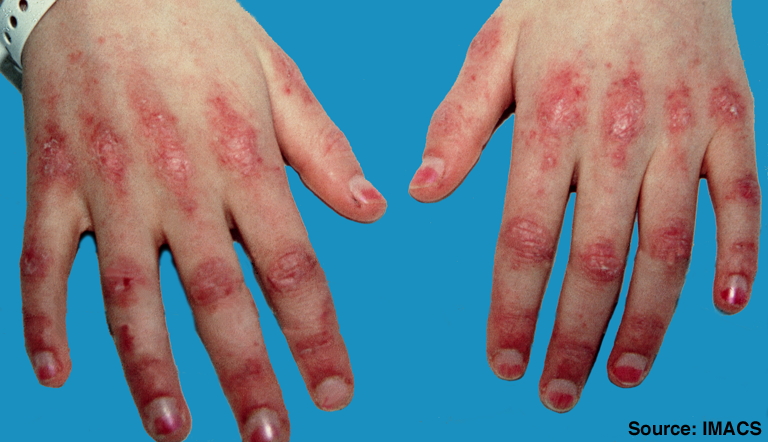
- 손의 피부 증상:
- 고트론 구진, 고트론 징후: 손가락 관절 뒷면(배면)에 나타나는 발진으로, 구진성 변화는 고트론 구진, 홍반은 고트론 징후라고 한다. 주로 시지, 중지의 MP 관절이나 PIP 관절에 잘 생긴다.
- 조갑 주위 홍반 및 조상피 출혈점: 손톱 주위의 변화는 고트론 구진이나 징후보다 먼저 나타나는 경우가 많아 진단에 중요하다.
- 역고트론 징후: 손바닥 쪽 손가락 관절 주변에 나타나는 자홍색 발진으로, 항 MDA5 항체 양성 환자에게 특징적이다.
- 메카닉스 핸드: 손가락 측면, 특히 엄지 척측이나 시지 요측에 나타나는 손 습진과 유사한 발진으로, 항합성 효소 증후군에 특징적이다.
- 얼굴·머리의 피부 증상:
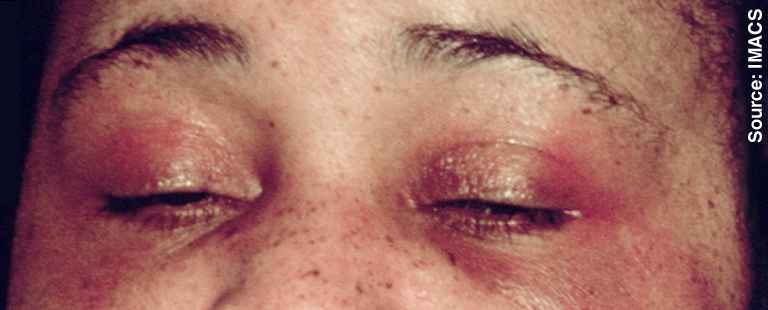
- 헬리오트로프 발진: 윗눈꺼풀(상안검)에 나타나는 부종성 홍반으로, 자홍색에서 암적색을 띠는 경우가 많다. 뺨, 이마, 귓바퀴 등에도 홍반이 나타날 수 있다.
- 몸통의 피부 증상:
- V 징후: 앞가슴 부위에 나타나는 발진
- 숄 징후: 어깨에서 등 윗부분에 나타나는 발진
- 팔다리의 피부 증상:
- 팔꿈치, 무릎 등 관절 뒷면(배면)에 홍반이 나타나며, 고트론 징후라고 불린다.
- 기타 피부 증상:
- 수포, 지방직염, 피부 궤양, 다형성 피부 위축(포이킬로더마), 피하 석회화 침착 등이 나타날 수 있으며, 특히 피하 석회화 침착은 항 NXP2 항체 양성 환자에게 많다.
피부근염 피부 병변의 조직학적 변화는 표피 기저층의 액상 변성, 진피의 혈관 주위를 중심으로 한 염증 세포 침윤, 진피의 뮤신 침착 등이 나타날 수 있다. 이러한 소견은 전신성 홍반 루푸스와 감별이 어려울 수 있다.
- 표피 기저층의 액상 변성: 피부근염 조직 소견의 특징 중 하나로, 기저층의 각질 세포가 공포성으로 변성된 상태를 말한다. 아폽토시스에 빠진 표피 세포가 호산성의 콜로이드 소체로 관찰될 수도 있다. 전신성 홍반 루푸스나 편평 태선에서도 관찰될 수 있다.
- 진피 염증 세포 침윤: 염증 세포가 진피 얕은 층의 혈관 주위를 중심으로 띠 모양으로 분포한다. 침윤 세포는 대부분 CD4 양성 T 세포이지만, CD8 양성 T 세포, 대식세포, 형질 세포양 수지상 세포 등도 섞여 있다. 항합성 효소 증후군 환자에서는 표피 내에 CD8 양성 T 세포가 많이 침윤한다.
- 진피의 뮤신 침착: 진피에 뮤신이 침착되어 HE 염색에서 진피 간질이 약간 호염기성의 자주빛을 띤다.
노동 시 호흡 곤란이 있는 경우에는 간질성 폐렴이나 심근염의 합병을 의심해야 한다. 간질성 폐렴은 항 ARS 항체나 항 MDA5 항체 양성 환자에게서 흔하게 나타나며, 항합성 효소 증후군 환자의 80%에서 관찰된다는 보고도 있다.[20]
심근염은 심부전이나 부정맥을 유발할 수 있으며, 중증의 경우 치명적일 수 있다.[21] 심전도, 심근 이탈 효소 측정, 심장 초음파 검사 등이 필요하다.
소화기 장애는 인두근 장애가 가장 중요하며, 염증성 장 질환, 특발성 담즙성 간경변, 특발성 경화성 담관염 등이 합병될 수 있다.
자가면역 근염 환자는 일반인보다 내장 악성 종양 발생 위험이 5~7배 높으므로, 유방과 하부 소화관을 포함한 검진이 필요하다.[22]
8. 진단
혈액 내 크레아틴 키나아제 수치 상승은 근염의 표징이다.[2] 근염 진단에는 신체 검사, 근전도 검사(EMG), 자기 공명 영상(MRI), 근육 생검, 혈액 검사 등이 사용된다.[2] 의사는 우선 신체 검사를 통해 근력 약화나 발진을 평가한다.[2]
근전도 검사는 작은 바늘을 근육에 삽입하여 전기적 신경 자극에 대한 근육 반응을 확인하는 검사이다.[4] 자기 공명 영상은 근육 위축을 시각화하는 데 유용하며, 고통 없고 비침습적이다.[9][4] 반면, 근육 생검은 근염 진단에 가장 신뢰할 수 있는 검사이다.[4]
혈액 검사에서는 근육 염증을 나타내는 크레아틴 키나아제 수치 증가를 확인할 수 있다.[4] 특정 자가항체(근육 세포를 표적으로 하는 항체)가 혈액에서 발견될 수도 있는데, 이는 근염이 자가면역 질환으로 발생했음을 나타낸다.[3] 이러한 자가항체의 예로는 항-Jo-1, 항-HMGCR, 항-TIF1 등이 있다.[3]
말초 혈액 소견에서는 경미한 백혈구 증가나 빈혈이 나타날 수 있다. 적혈구 침강 속도(ESR)나 C 반응 단백(CRP) 등의 염증 반응은 경미하게 상승하는 경우가 많아 질병 활성 지표로서 의미는 적다. 오히려 염증 반응 상승은 감염 합병을 의심해야 한다. 혈청 근원성 효소(CK, LDH, AST, ALT, 알돌라제) 상승은 근육 질환을 시사하며, 특히 CK는 민감도가 높고 질병 활성도와 가장 잘 상관관계를 보인다. CK 아이소자임에는 골격근 유래의 CM-MM과 심근 유래의 CK-MB가 있으며, CK-MB/CK가 10%를 초과하면 심근 장애 합병을 의심해야 한다. 종양성 질환이나 만성 간 질환에서 고CK 혈증을 보이는 경우도 있는데, 이는 IgG 성분이 CK에 결합하여 CK 클리어런스가 저하되어 나타나는 매크로 CK로, 임상적 의미는 불명확하다. 혈청 페리틴이나 KL-6은 근염 마커는 아니지만, 합병되는 간질성 폐렴의 마커이다.
근염 특이 자가항체(MSA)와 근염 중복 증후군에서 발견되는 근염 관련 자가항체(MAA)가 알려져 있다.
| 근염 특이 자가항체 | 근염 관련 자가항체 | |
|---|---|---|
| 피부근염 | TIF1-γ, MDA5, Mi-2, NXP-2, SAE | |
| 항합성효소 증후군 | Jo-1, OJ, PL-7, EJ, KS, Ha, Zo, SC, JS | |
| 면역 매개성 괴사성 근병증 | SRP, HMGCR | 미토콘드리아 M2 |
| 봉입체 근염 | cN1A | |
| 오버랩 증후군 | Ku |
근염 관련 항체에는 항핵항체, 항U1RNP 항체, 항SS-A/Ro 항체, 항Ku 항체, 항PM-Scl 항체, 항미토콘드리아 M2 항체, 항cN1A 항체 등이 있다. 이 중 항Ku 항체는 중복 증후군, 항미토콘드리아 M2 항체는 면역 매개 괴사성 근병증, 항cN1A 항체는 봉입체 근염과 관련이 있다.
- 피부근염: 피부근염의 근염 특이적 자기항체로는 항TIF1-γ항체, 항MDA5항체, 항Mi-2항체, 항NXP-2항체, 항SAE항체가 있다.
- 항합성효소증후군: 항합성효소증후군의 근염 특이적 자기항체로는 아미노아실 tRNA 합성효소(ARS)에 대한 자기항체인 항ARS항체가 있다. 항ARS항체는 총칭이며 이론상의 것도 포함하여 10종류(항Jo-1항체, 항OJ항체, 항PL-7항체, 항PL-12항체, 항EJ항체, 항KS항체, 항Ha항체, 항Zo항체, 항SC항체, 항JS항체)가 알려져 있다. 항합성효소증후군에서는 항ARS항체는 1종류만 검출되며 중복되지 않는다.
- 면역 매개성 괴사성 근병증: 면역 매개성 괴사성 근병증의 근염 특이적 자기항체로는 항SRP항체나 항HMGCR항체가 있다.
- CT(컴퓨터 단층 촬영): 전신의 근위축 및 간질성 폐렴 유무를 평가한다.
- MRI(자기 공명 영상): MRI는 간질의 섬유화나 염증성 변화에 따른 부종성 변화 등 CT로는 평가할 수 없는 근속 내 구조를 평가할 수 있어 근염에 필수적인 검사이다. T1WI, T2WI, STIR로 촬영하며, 근속 내 염증이 생긴 섬유 분포와 부종을 STIR로 평가한다. STIR에서 고신호여도 병리학적으로 염증 세포 침윤이 있다고 단정할 수는 없다. Gd 조영은 STIR나 T2WI에 비해 부종성 변화 검출률이 높지 않아 사르코이드증이나 근막염을 상정하지 않는 경우 불필요하다. 피부근염에서는 종종 근막에 강조된 부종성 변화나 피하 부종이 관찰될 수 있다.
- 신티그래피(섬광 조영술): 99mTc-MDP신티그래피(골 신티그래피)는 전신의 골격근 염증을 한 번에 평가할 수 있다.
- 침 근전도: 침 근전도에서는 안정 시에 섬유 자발 전위, 양성 예파, 가성 미오토니 방전이 관찰된다. 이는 분절성 괴사나 재생 섬유가 관여하는 소견으로 여겨진다. 수의적 수축 시에는 급속 동원이나 BSAP 패턴의 MUP가 관찰된다.
근육 생검은 MRI에서 부종성 변화가 있는 부위에서 채취한다.[23] 스테로이드 요법 전후의 근육 생검 병리 소견을 비교하면, 스테로이드 요법 후에 근육에 침윤된 림프구 수가 감소하고 근육 내 염증성 사이토카인 및 혈관 내피 세포에서 세포 부착 인자의 발현과 근육의 HLA-ABC 발현이 저하된다.[24] 따라서 근육 생검은 치료 전에 시행하는 것이 바람직하다.
한국에서는 후생노동성의 진단 기준이 자주 사용된다. Bohen and Peter의 진단 기준[12]이나 Tanimoto의 진단 기준[36]도 알려져 있다. 2019년에는 소아·성인 통일 진단 기준이 작성되었다.[37] 국제 진단 기준은 기존 분류 기준에 비해 우수한 민감도와 특이도를 가지고 있지만,[19] 각 항목 점수를 기억하기 어렵고, 점수 총합에서 자가면역성 근염 가능성을 판단하기 위해 그래프를 참조해야 하는 단점이 있다. 이 때문에 웹 계산기가 제작되었고, 일본어판도 공개되었다. 뇌신경내과에서는 유럽 신경근 센터(ENMC)의 진단 기준이 중요하게 여겨진다.[15]
9. 감별 진단
근이영양증에서도 반응성 세포 침윤이 종종 관찰된다. 특히 안면견갑상완형 근이영양증(FSHD), LMNA 유전자 변이에 의한 근이영양증 및 디스페린 유전자 변이에 의한 근이영양증이 유명하다. LMNA 유전자 변이에 의한 근이영양증은 에머리-드레이퍼스형 근이영양증이나 LGMD1B를 나타낸다. 또한 디스페린 유전자 변이는 LGMD2B를 나타낸다. 원칙적으로는 염증성 근 질환에서는 HLA-ABC가 근 섬유에 발현되지만 근이영양증에서는 발현되지 않는 경우가 많다.
글리코겐 축적병, 지질 대사 이상, 미토콘드리아 질환에 의한 근육병증도 감별해야 한다.
10. 치료
여러근육염과 피부근염은 우선 많은 양의 코르티코스테로이드로 치료한다. 근염 치료는 근본 원인에 따라 달라진다.[4] 바이러스 감염으로 인한 근염은 일반적으로 치료가 필요하지 않다.[4] 세균 감염으로 인한 근염은 항생제를 사용할 수 있다.[4] 약물로 인한 근염은 해당 약물 사용을 중단하는 것이 중요하다.[4]
자가면역 질환으로 인한 근염의 경우 다양한 치료 방법이 있다. 글루코코르티코이드가 종종 치료의 첫 번째 선택이다.[10] 이 약물은 면역 체계를 약화시켜 근육을 공격하지 못하도록 한다. 이는 일종의 스테로이드이며 기분 변화, 식욕 증가, 수면 장애 등 다양한 부작용을 일으킬 수 있다. 스테로이드 절약형 면역억제제는 또 다른 치료 선택지이다.[10] 이는 면역 체계를 약화시키지만 스테로이드가 유발하는 부작용은 일으키지 않는다. 생물학적 제제라는 종류의 약물 또한 치료 방법 중 하나이다.[10] 정맥 내 면역 글로불린 (IVIg)은 자가면역 질환으로 인한 근염 치료에 효과적인 것으로 나타났다.[11]
자가면역성 근염 치료에는 PSL을 첫 번째로 선택하는 것에 대해 세계적으로 의견이 일치한다. Dalakas가 2010년에 리뷰에서 제창한 치료 지침이 잘 알려져 있다.[60] 이 치료 지침에서는 PSL을 1mg/kg의 고용량으로 시작하고, 중증의 경우 스테로이드 펄스 요법으로 시작한다. 초기 용량을 3~4주간 지속하고, 2~3주 간격으로 5~10mg의 속도로 감량한다고 기술되어 있다. 스테로이드 저항 사례나 PSL 감량 중 악화가 있는 경우에는 면역 글로불린 대량 요법이나 면역 억제제의 병용 또는 리툭시맙을 검토한다. 메이요 클리닉의 치료 프로토콜 또한 잘 알려진 치료 지침이다.[61] 면역 억제제를 처음부터 병용하는 것과 PSL의 감량 속도가 비교적 빠른 것이 특징이다. 면역 매개성 괴사성 근병증에 관해서는 2016년 ENMC 워크숍에서 치료 알고리즘이 제창되었다.[62] 항 SRP 항체 양성 면역 매개성 괴사성 근병증의 리툭시맙 투여 효과는 편차가 있으며, 수 회의 투여로 관해를 얻는 경우도 있지만 리툭시맙 정기 투여가 필요했던 사례까지 있다.[63] 항 SRP 항체 양성 면역 매개성 괴사성 근병증에는 77.8%에서 유효했지만 항 HMGCR 항체 양성 면역 매개성 괴사성 근병증에서는 43.8%에서만 유효했다.[64] 면역 매개성 괴사성 근병증 중 23.5%에서 리툭시맙 투여 후 감염증이 확인되었고 5.9%가 사망했다. 면역 질환을 대상으로 한 대규모 검토[65]에서는 리툭시맙 투여 후 17.3%에서 감염증이 확인되었고, 4.1%가 사망했다. 면역 매개성 괴사성 근병증에 대한 리툭시맙의 안전성은 기타 면역 질환과 거의 동등하다고 생각된다. 항 HMGCR 항체 양성 면역 매개성 괴사성 근병증에서는 면역 글로불린 요법의 장기적인 반복 투여가 종종 이루어지고 있다.[62] 2년간의 치료를 받아도 반수 이상의 면역 매개성 괴사성 근병증 사례에서는 불충분한 신경학적 개선에 그치고 있다는 보고가 있다.[49]
11. 각론
자가면역성 근염은 피부근염, 항합성효소 증후군, 봉입체근염, 면역매개성 괴사성 미오파티의 4가지 하위 유형으로 분류된다.[18] 1975년 보한과 피터(Bohan and Peter)의 진단 기준에 따라 오랫동안 발진 유무에 따라 피부근염과 다발근염으로 분류되었으나,[12][13] 이후 근염 특이 자가항체(MSA)와 근염 관련 자가항체(MAA)에 대한 지식, 근병리 소견의 특징이 밝혀지면서 분류 기준이 변화했다.
2003년 Dalalas와 Hohfeld는 봉입체근염을 제외하고 발진 유무와 근병리를 중시한 다발근염과 피부근염의 진단 기준을 제시했다.[14] 2004년 유럽 신경근 센터(ENMC) 워크숍에서는 피부근염, 다발근염, 봉입체근염, 면역매개성 미오파티, 비특이성 근염의 5가지로 분류하는 ENMC 분류 기준을 만들었다.[15] 2014년에는 항합성효소 증후군(anti-synthetase syndrome, ASS)이 독립적인 하위 유형으로 추가되었다.[16]
2018년에는 피부근염 진단 기준이 개정되었는데,[17] 믹소바이러스 저항성 단백질 A(MxA) 발현이 피부근염 진단에 유용하다는 점이 반영되었다. 피부근염은 전신성 홍반성 루푸스, 류마티스 관절염과 함께 Ⅰ형 인터페로노파티로 인식된다.
임상적으로 다발근염으로 진단되는 경우 대부분 근병리학적으로는 면역매개성 미오파티이며, 엄밀한 병리 진단 기준을 적용하면 다발근염으로 진단되는 예는 거의 없다. 과거 다발근염으로 병리 진단되었던 사례의 대부분은 봉입체근염이었다.[18]
2017년 유럽 류마티스 학회, 미국 류마티스 학회는 국제 근염 분류 기준 프로젝트(IMCCP)의 새로운 국제 근염 분류 기준을 승인했다.[19] 이 기준에서는 무근증성 피부근염(ADM)의 정의가 변경되어, 근력 저하 없이 피부근염에 전형적인 발진을 가진 경우는 모두 ADM으로 부른다.
- 오버랩 증후군 (Overlap syndrome): 교원병에 근염이 함께 나타나는 경우로, 둘 이상의 교원병 진단 기준을 충족한다.
- 육아종성 미오파티 (Granulomatous myopathy): 육아종 병변은 다양한 근육 질환에서 나타날 수 있다.[55][56]
- GVHD 근염: 조혈모세포 이식 후 합병증으로 나타난다.[57][58]
11. 1. 피부근염 (Dermatomyositis)
피부근염은 아급성으로 진행되며, 고트론 징후나 헬리오트로프 발진과 같은 특징적인 피부 발진과 함께 몸통 쪽에 가까운 근육(근위근)의 힘이 약해지는 증상을 보인다. 다섯 종류의 피부근염 특이 자가항체가 발견되었으며, 어떤 항체가 양성으로 나오는지에 따라 특징이 조금씩 다르다. 성인의 경우 항TIF1-γ 항체가 가장 많이 발견되며, 악성 종양을 동반하는 경우가 많다. 어린이는 항NXP-2 항체 양성이 많은 편이다. 근육 증상으로는 팔다리 근위근과 목 근육의 힘이 약해지는 것이 일반적이다. 근육 증상이 뚜렷하지 않은 무근증성 피부근염의 경우, 항MDA5 항체 양성인 경우가 많다. 혈액 검사에서 CK 값은 다양하게 나타나는데, 항MDA5 항체 양성인 경우에는 정상치이거나 약간만 상승하는 경우가 많다. 항Mi 항체 양성인 경우에는 대부분 1000 이상으로 나타난다. 골격근 MRI에서는 근막에 부종이 두드러지게 나타나는 경우가 많고, 피하 부종이 나타나기도 한다. 피부와 근육 외 증상으로는 간질성 폐렴이 중요하며, 특히 항MDA5 항체 양성의 무근증성 피부근염에서는 빠르게 진행되는 간질성 폐렴이 동반되는 경우가 많아 주의해야 한다.쾨브너 현상은 피부근염의 발진을 설명하는 중요한 개념이다. 쾨브너 현상은 정상적인 피부에 긁힘, 상처, 염증 등이 생기면 그 부위에 원래 있던 피부 질환과 같은 증상이 나타나는 것을 말한다. 피부근염 외에도 건선, 편평 태선 등에서 나타난다. 고트론 구진·고트론 징후는 관절이 펴지는 부분에, 헬리오트로프 발진은 눈꺼풀에 잘 생기는데, 이는 쾨브너 현상과 관련이 있다.
피부근염은 여러 가지 특징적인 피부 소견을 보인다.
; 손의 피부 소견
손의 피부 소견은 진단에 매우 중요하다. 고트론 구진, 고트론 징후는 관절 뒷면에 생기는 발진으로, 구진(볼록한 발진)이 있으면 고트론 구진, 붉은 반점만 있으면 고트론 징후라고 한다. 특히 둘째, 셋째 손가락의 중간 관절에 잘 생긴다. 손톱 주위의 붉은 반점이나 출혈점도 중요한데, 고트론 구진이나 징후보다 먼저 나타나는 경우가 많다. 손바닥 쪽 손가락 관절 주변에 자홍색의 발진이 생기기도 하는데, 이를 역고트론 징후라고 하며 항MDA5 항체 양성에서 특징적이다. 메카닉스 핸드는 손가락 측면, 특히 엄지손가락 척측이나 둘째 손가락 요측에 생기는 손 습진과 비슷한 발진으로, 항합성 효소 증후군에서 특징적으로 나타난다.
; 얼굴·머리의 피부 소견
헬리오트로프 발진은 윗눈꺼풀에 나타나는 부종성 홍반으로, 자홍색이나 암적색을 띠는 경우가 많지만 부종만 나타나기도 한다. 뺨, 이마, 귓바퀴 등에도 홍반이 자주 나타난다.
; 체간의 피부 소견
가슴 앞쪽에는 V 징후, 어깨에서 등 윗부분에는 숄 징후라고 불리는 발진이 잘 나타난다.
; 사지의 피부 소견
팔꿈치, 무릎 등 관절 뒷면에도 홍반이 생기는데, 이 역시 고트론 징후라고 불린다.
; 부위에 관계없는 발진
수포, 지방직염, 피부 궤양, 다형성 피부 위축(포이킬로더마), 피하 석회화 침착 등이 나타날 수 있다. 특히 피하 석회화 침착은 항 NXP2 항체 양성에서 많이 나타난다.
피부근염의 피부 병변을 조직학적으로 검사하면 표피 기저층의 액상 변성, 진피 혈관 주위 염증 세포 침윤, 진피의 뮤신 침착 등이 공통적으로 나타난다. 이러한 소견은 전신성 홍반 루푸스와 감별하기 어렵다.
thumb
근육 조직 검사에서는 근섬유 다발 주변 위축(perifascicular atrophy)이 가장 특징적인 소견이다. 하지만 항MDA5 항체 양성 사례에서는 잘 나타나지 않는다.
면역 염색에서는 근세포막에 HLA-ABC가 발현되고, 내피 모세혈관에 막 침습 복합체(MAC) 침착이 관찰된다. HLA-DR이 일부 근섬유에서 발현되기도 하지만 드물다. 믹소바이러스 저항성 단백질 A(MxA)는 Ⅰ형 인터페론(IFN-Ⅰ)에 의해 유도되는 단백질로, 골격근 근섬유에서 MxA 발현은 피부근염 진단에 유용하다.
전자 현미경에서는 혈관 내피에서 tubuloreticular inclusions(TRIs)라고 불리는 관상 구조물의 집괴를 관찰한다[27]。
과거에는 혈류 장애로 인해 근섬유 다발 주변 위축이 생긴다고 생각했지만, 최근에는 Ⅰ형 인터페론의 영향으로 생긴다는 가설이 제시되고 있다. 피부근염에서 관찰되는 염증 세포는 주로 CD4 양성 T 세포와 B 세포이며, CD8 양성 T 세포는 적다. 자가 항체에 따라 임상 증상과 병리 소견이 다르다는 것이 밝혀졌다.
| 자가 항체 | 임상적 특징 | 병리학적 특징 |
|---|---|---|
| TIF1-γ | 성인에서 악성 종양 동반 | 근섬유 다발 주변 위축, 모세 혈관에 MAC 침착, punched-out vacuoles |
| MDA5 | 무근증성 피부근염 | 근섬유 다발 주변 위축은 드물며, 모세 혈관에 MAC 침착 |
| Mi-2 | 근력 저하, 고CK 혈증 | 근섬유 다발 주변 괴사, 주피 ALP 발현, 주피 결합 조직 단편화, 모세 혈관에 MAC 침착은 드물다 |
| NXP-2 | 젊은 나이의 피부근염 | 미세 경색 |
| SAE | 광범위한 홍반 | ? |
항MDA5 항체 양성 피부근염은 궤양, 지방직염, 관절염, 간질성 폐렴을 특징으로 하는 피부근염의 한 종류이다. 급속 진행성 간질성 폐렴을 동반하는 경우가 많아 예후가 좋지 않다[39]. 이 질환은 IL-6, IL-10, IL-18, IFN-γ, TNF-α 등의 사이토카인 상승 및 영상 소견이 COVID-19와 유사하며, MDA5가 SARS-CoV-2의 인식과도 관련이 있어 주목받고 있다[42][43].
11. 1. 1. 연소성 피부근염
성인의 피부근염과 달리 소아 사례는 악성 종양을 동반하지 않고, 미세 경색 사례의 빈도가 높으며, 피하나 근막의 석회화를 동반하는 경우가 있는 등 성인 사례와 임상적 특징이 일부 다르기 때문에, 소아 피부근염은 별개의 질환으로 취급되기도 한다.[1] 소아 피부근염의 특징으로 여겨져 온 징후의 대부분은 항NXP-2 항체 양성 사례의 특징이며, 단지 항NXP-2 항체 양성 사례의 빈도가 높다는 것을 반영하고 있을 뿐일 수 있다.[1]
11. 1. 2. 무근증성 피부근염
무근육증 피부근염은 항MDA5 항체 양성 피부근염이 잘 알려져 있지만, 항ARS 항체 양성 사례나 항TIF1-γ 항체 양성 사례도 포함된다. 무근육증 피부근염과 관련된 간질성 폐렴의 예후는 좋지 않다고 보고되었지만, 항MDA5 항체 양성 사례가 많이 포함된 영향으로 생각된다[38].
11. 2. 항합성효소 증후군 (Anti-synthetase syndrome, ASS)
항아미노아실-tRNA 합성효소(aminoacyl-tRNA synthetase, ARS) 항체 양성 근염 사례를 통칭하여 항합성효소 증후군 (anti-synthetase syndrome, ASS) 또는 항ARS 항체 증후군이라고 부른다. 항ARS 항체는 이론상 10종류가 알려져 있다. 항Jo-1 항체, 항OJ 항체, 항PL-7 항체의 빈도가 높다. 임상적으로는 근염에 더하여 간질성 폐렴, 메카닉 핸드 등의 피부 증상, 다발성 관절염, 발열, 레이노 현상 등을 합병한다. 항합성 효소 증후군의 간질성 폐렴은 항MDA5 항체 양성 사례에서 전형적으로 나타나는 급속 진행성 간질성 폐렴과는 달리 만성으로 경과하는 경우가 많다. 피부근염에서는 다발 관절염이나 레이노 현상을 보이는 경우는 드물어 감별에 유용하다. 근육 증상은 항Jo-1 항체, 항OJ 항체, 항PL-7 항체에서 두드러지는 경향이 있으며, CK도 높은 수치를 나타낸다. 항EJ 항체나 항PL-12 항체 양성 사례에서는 간질성 폐렴이 주를 이루며 근염 증상은 경미한 경우가 많다. CK도 정상 또는 상승하더라도 경미하다. 골격근 MRI에서는 피부 근염과 마찬가지로 부종성 변화는 근막이 주를 이루는 경우가 많다. 피하에도 부종을 보이는 경우가 있다.
11. 3. 면역 매개성 괴사성 근병증 (Immune-mediated necrotizing myopathy, IMNM)
근원성 변화, 괴사 및 재생 근육에 대식세포 침윤이 확인된다. 림프구 침윤은 확인되지 않거나, 있어도 반응성 변화로 설명 가능하다. 만성 경과를 보이는 사례에서는 간질의 섬유화나 지방 침윤이 확인된다. 면역 염색에서는 근섬유막에서 HLA-ABC 발현 증가가 확인되지만, 피부근염이나 포함체 근육염에 비해 매우 경미하다. 일반적으로 HLA-DR 발현은 확인되지 않는다. 일부 근섬유막에서 막 침습 복합체 (MAC) 침착을 확인한다. 또한 p62가 근세포질 내에서 과립상으로 염색되며, 자가 탐식과 관련된 샤페론 단백질과 공존한다.[45]
면역 매개 괴사성 미오파티에 특이적인 자가항체로는 항-SRP 항체와 항-HMGCR 항체가 알려져 있다. 항-HMGCR 항체는 스타틴 유발성 면역 매개 괴사성 미오파티에 특이적인 항체로 보고되었지만, 이후 검토에서는 항-HMGCR 항체 양성 면역 매개 괴사성 미오파티 중 스타틴 복용 이력이 있었던 것은 18%에 불과했다. 스타틴 복용은 면역 매개 괴사성 미오파티의 위험 인자이지만 원인이라고는 할 수 없다. SRP와 HMGCR 모두 근 섬유막에 발현하며, 자가항체가 이 항원에 결합하여 C1q가 유도되고, 고전 경로를 통해 순차적으로 보체가 활성화된다. 최종적으로 C5b-9로 구성된 막 공격 복합체 (MAC)가 근 섬유막에 형성되어, 근 섬유막에 구멍이 생기므로 근 섬유가 괴사한다.[46]
항-SRP 항체 양성 괴사성 미오파티, 항-HMGCR 항체 양성 괴사성 미오파티 모두 30대 이상인 경우가 약 90%를 차지한다. 소아의 경우 근육 디스트로피와의 감별이 매우 어려워 근 생검을 포함한 검사가 필요하다.
전형적으로 아급성으로 근위 근육 우위로 근력 저하를 나타낸다. 근육 증상으로는 근력 저하 외에 근위축을 보이는 것이 특징적이며, 비교적 근육통도 동반되는 경우가 많다.[47][48] 척추 기립근, 연하에 관련된 근육 및 안면 장애도 동반될 수 있다. 또한 목 처짐이나 연하 장애도 흔히 나타난다.[49][50] 만성적으로 경과한 일부 항-SRP 항체 양성 사례는 안면견갑상완형 근육 디스트로피가 감별될 수 있다. 발진, 관절염, 간질성 폐렴, 심근염을 동반하는 경우도 있지만 근외 증상은 비교적 적다. CK는 대부분의 사례에서 1000 이상의 고치를 나타낸다. 골격근에서는 미만성의 옅은 부종성 변화를 근육 내에서 보이는 경우가 많다.
11. 3. 1. 항미토콘드리아 M2 항체 양성 근염
항미토콘드리아 M2 항체는 원발성 담즙성 간경변에 특징적인 자가항체이다. 만성적인 경과로 심근 장애, 호흡근 장애, 골격근 위축이 두드러지는 등 특징적인 근염으로 알려져 있다.[51] 경부·체간의 근력 저하가 두드러지며, 종종 목떨굼이나 호흡 부전을 나타내기 때문에 운동 신경 질환이나 네마린근병증이 감별 대상이 된다. 병리학적으로는 면역 매개성 괴사성 근병증과 유사하지만 육아종을 고율로 인정했다는 보고도 있다.[52]
11. 3. 2. 면역 관문 억제제 관련 근염
면역 관문 억제제의 면역 관련 부작용(immune-related adverse events, irAE)으로 면역 관문 억제제 관련 근염이 알려져 있다. 안검하수나 복시가 흔하며, 초기 증상이 중증 근무력증과 유사한 것이 특징이다. 병리학적으로는 면역 매개 괴사성 근병증과 유사하지만 괴사·재생 섬유가 수 개 단위로 뭉쳐서 존재하는 경향을 보인다[53].
11. 4. 봉입체 근염 (Inclusion body myositis, IBM)
봉입체 근염(Inclusion body myositis, IBM)은 50세 이후에 발병하며, 남성에게 약간 더 많이 나타나는 질환이다. 손가락 굴곡근, 특히 심지굴근이 손상되기 쉬워 단추를 채우지 못하거나, 페트병 뚜껑을 열지 못하는 등의 증상을 호소하는 경우가 많다. 대퇴사두근도 자주 손상되며, 진행성 근력 저하와 근위축을 보이고, 종종 증상은 좌우 비대칭적이다. 발병 5년 만에 일상생활에 지장을 초래한다.[35]
연하 장애는 60% 이상에서 나타나지만, 호흡근이나 심근은 손상되기 어렵다. 혈청 CK 값은 정상에서 정상 상한의 10배 정도로 증가한다. 근육 MRI에서는 대퇴사두근 및 비복근 내측두에 지방 치환과 부종성 변화를 보인다. 대퇴사두근 중 대퇴직근은 상대적으로 약간 보존되는 경향이 있다. 세포질 5'-뉴클레오티다제(cN1A)에 대한 자가항체가 일부에서 검출된다.[35]
병태 기전은 불분명하지만 변성, 단백질 분해 경로의 이상, 면역계의 이상이 시사되고 있다.[35]
11. 5. 오버랩 증후군 (Overlap syndrome)
교원병에 근염이 함께 나타나는 경우가 있다. 둘 이상의 교원병 진단 기준을 충족하는 경우를 오버랩 증후군이라고 한다. 함께 나타나는 근염은 면역 매개성 괴사성 근병증, 피부근염, 비특이성 근염 등 다양하지만, 면역 매개성 괴사성 근병증이 자주 발생한다. 이러한 사례 중에는 항Ku항체 양성 사례가 일정 수 존재한다.
11. 6. 육아종성 미오파티 (Granulomatous myopathy)
육아종 병변은 다양한 근육 질환에서 나타난다.[55][56] 특발성, 사르코이드증, 감염, 악성 종양, 교원병, 염증성 장 질환, 원발성 담즙성 담관염, 크리오피브리노겐혈증, 이물질 등으로 발생할 수 있다. 또한 봉입체 근염, 항 미토콘드리아 M2 항체 양성 근염 등 염증성 근육 질환에서도 관찰된다. 육아종성 근육 미오파티를 일으키는 악성 종양으로는 악성 림프종, 교원병으로는 다발혈관염 육아종증, 경피증, 류마티스 관절염, 염증성 장 질환으로는 크론병이 있다. 육아종성 미오파티를 일으키는 감염증으로는 좁쌀 결핵, 제3기 매독, 톡소플라스마증, 뉴모시스티스 이로베치이, 브루셀라증, HTLV-1, 크립토코쿠스증 등이 있다. 건락성 육아종을 확인한 경우에는 결핵 등 항산균에 의한 육아종을 고려하지만, 일본에서는 근육 내에서 확인되는 육아종은 거의 비건락성 육아종이다. 근육 내에서 비건락성 육아종을 확인한 경우에는 우선 사르코이드증을 의심한다. 근육 내 비건락성 육아종은 사르코이드증뿐만 아니라, 봉입체 근염, 항 미토콘드리아 M2 항체 양성 근염 등에서도 나타난다. 근육에서만 비건락성 육아종이 확인되는 경우에는 사르코이드증으로 진단하기 어렵다.
11. 7. GVHD 근염
조혈모세포 이식 후 합병증으로 GVHD 근염이 알려져 있다.[57][58] 다른 염증성 근육 질환과는 다른 병리 소견을 보인다.[59]
참조
[1]
웹사이트
Amplified Musculoskeletal Pain Syndrome (AMPS)
https://www.children[...]
Children's Health
[2]
논문
Diagnosis, pathogenesis and treatment of myositis: recent advances
2014-03
[3]
논문
Myositis-specific autoantibodies: an important tool to support diagnosis of myositis
2016-07
[4]
웹사이트
Myositis: Symptoms and Causes
https://www.webmd.co[...]
2022-06-12
[5]
논문
Statin induced myopathy
2008-11
[6]
논문
COVID-19 and Myositis: What We Know So Far
2021-07
[7]
논문
Differential diagnosis of idiopathic inflammatory myopathies in adults - the first step when approaching a patient with muscle weakness
2018
[8]
논문
Genetic Myopathies Initially Diagnosed and Treated as Inflammatory Myopathy
2016-05
[9]
논문
Value of MRI in diagnostics and evaluation of myositis
2016-11
[10]
논문
Current diagnosis and treatment of polymyositis and dermatomyositis
2018-11
[11]
논문
Indications for IVIG in rheumatic diseases
2015-03
[12]
논문
1975-02-13
[13]
논문
1975-02-20
[14]
논문
2003-09-20
[15]
논문
2004-05
[16]
논문
2015-03
[17]
논문
2020-01
[18]
논문
2003-08-12
[19]
논문
2017-12
[20]
논문
2001-10-01
[21]
논문
2011-05-05
[22]
논문
1992-02-06
[23]
논문
2019-10
[24]
논문
2000-02
[25]
논문
1985-02-16
[26]
논문
2012-01
[27]
논문
1974-11
[28]
논문
2010
[29]
논문
2018-12-01
[30]
논문
2019-10
[31]
논문
2020-10
[32]
논문
2006-10
[33]
논문
2008-12
[34]
논문
2010-02
[35]
논문
2013-07-01
[36]
논문
J Rheumatol. 1995 Apr;22(4):668-74.
[37]
웹사이트
多発性筋炎・皮膚筋炎診療ガイドライン(2020 年暫定版)
http://www.aid.umin.[...]
[38]
논문
Curr Rheumatol Rep. 2014 Dec;16(12):465.
[39]
논문
J Am Acad Dermatol. 2018 Apr;78(4):776-785.
[40]
논문
Neurology. 2020 Jul 7;95(1):e70-e78.
[41]
논문
Eur Respir J. 2020 Sep 24;56(3):2001618.
[42]
논문
Trends Microbiol. 2019 Jan;27(1):75-85.
[43]
논문
Front Immunol. 2020 May 8;11:939.
[44]
논문
J Virol. 2020 Jun 16;94(13):e00099-20.
[45]
논문
Neurology. 2018 Feb 6;90(6):e507-e517.
[46]
논문
Ann Rheum Dis. 2019 Jan;78(1):131-139.
[47]
논문
Ann Rheum Dis. 2006 Dec;65(12):1635-8.
[48]
논문
Arthritis Rheum. 2004 Jan;50(1):209-15.
[49]
논문
Semin Arthritis Rheum. 2019 Dec;49(3):420-429.
[50]
논문
Mayo Clin Proc. 2017 May;92(5):826-837.
[51]
논문
Brain. 2012 Jun;135(Pt 6):1767-77.
[52]
논문
Ann Neurol. 2017 Apr;81(4):538-548.
[53]
논문
J Autoimmun. 2019 Jun;100:105-113.
[54]
웹사이트
封入体筋炎 診療の手引き
https://www.neurolog[...]
[55]
논문
Am J Clin Pathol. 1999 Jul;112(1):63-8.
[56]
논문
Autoimmun Rev. Apr-May 2014;13(4-5):372-4.
[57]
논문
Biol Blood Marrow Transplant. 2015 Mar;21(3):389-401.e1.
[58]
논문
Bone Marrow Transplant. 2009 Jan;43(2):159-67.
[59]
논문
Muscle Nerve. 2021 Jun;63(6):852-860.
[60]
논문
Nat Rev Rheumatol. 2010 Mar;6(3):129-37.
[61]
논문
Mayo Clin Proc. 2013 Jan;88(1):83-105.
[62]
논문
Neuromuscul Disord. 2018 Jan;28(1):87-99.
[63]
논문
Arthritis Care Res (Hoboken). 2010 Sep;62(9):1328-34.
[64]
논문
Ther Adv Neurol Disord. 2021 Mar 12;14:1756286421998918.
[65]
논문
Clin Infect Dis. 2021 Mar 1;72(5):727-737.
[66]
웹사이트
Myositis
https://medlineplus.[...]
본 사이트는 AI가 위키백과와 뉴스 기사,정부 간행물,학술 논문등을 바탕으로 정보를 가공하여 제공하는 백과사전형 서비스입니다.
모든 문서는 AI에 의해 자동 생성되며, CC BY-SA 4.0 라이선스에 따라 이용할 수 있습니다.
하지만, 위키백과나 뉴스 기사 자체에 오류, 부정확한 정보, 또는 가짜 뉴스가 포함될 수 있으며, AI는 이러한 내용을 완벽하게 걸러내지 못할 수 있습니다.
따라서 제공되는 정보에 일부 오류나 편향이 있을 수 있으므로, 중요한 정보는 반드시 다른 출처를 통해 교차 검증하시기 바랍니다.
문의하기 : help@durumis.com