리보뉴클레오타이드
"오늘의AI위키"의 AI를 통해 더욱 풍부하고 폭넓은 지식 경험을 누리세요.
1. 개요
리보뉴클레오타이드는 인산기, 리보스, 핵염기로 구성된 분자이며, RNA의 구성 단위이다. 핵염기 종류에 따라 아데닐산, 구아닐산, 우리딜산, 시티딜산으로 나뉘며, DNA의 데옥시리보뉴클레오타이드와 비교하여 리보스를 당 성분으로 갖는다는 차이점이 있다. 리보뉴클레오타이드는 포스포다이에스터 결합을 통해 RNA 가닥을 형성하며, 데옥시리보뉴클레오타이드의 전구체로 작용하거나, 퓨린 및 피리미딘 뉴클레오타이드의 합성 경로를 통해 생합성된다. 1869년 프리드리히 미셰르에 의해 핵산이 처음 발견되었고, 포에버스 레벤이 뉴클레오타이드의 개념을 정립했다.
더 읽어볼만한 페이지
- 리보사이드 - 아데노신
아데노신은 다양한 생리적 과정을 조절하는 내인성 퓨린 뉴클레오사이드로, 심실상 빈맥 치료, 심장 스트레스 검사 보조제, 혈관 확장, 항염증, 항바이러스 효과 연구 등에 사용되며, 뇌에서 수면을 유도하고 주름 개선 화장품 성분으로도 활용된다. - 리보사이드 - 리보뉴클레오사이드
- RNA - RNA 간섭
RNA 간섭은 이중가닥 RNA에 의해 유전자 발현이 억제되는 과정으로, 다이서 효소에 의해 생성된 작은 간섭 RNA가 RNA 유도 침묵 복합체와 결합하여 표적 mRNA를 분해하거나 번역을 억제하며, 바이러스 방어, 발생 조절, 유전체 안정성 유지 등 다양한 기능과 응용 분야를 가진다. - RNA - 방향성 (분자생물학)
DNA 또는 RNA 가닥의 방향성은 5' 말단(5번 탄소에 인산기)과 3' 말단(3번 탄소에 수산기)로 구별되며, 이는 유전자 발현 조절, 폴리아데닐화, DNA 염기서열 분석 등 DNA와 RNA의 합성, 안정성, 번역 과정에 필수적이다. - 뉴클레오타이드 - 아데노신 삼인산
아데노신 삼인산(ATP)은 아데닌, 리보스, 세 개의 인산기로 구성된 뉴클레오티드로서, 고에너지 인산 결합의 가수분해를 통해 에너지를 방출하여 세포 과정에 사용되는 생명체의 주요 에너지 저장 및 전달 분자이며, 다양한 대사 경로를 통해 생성 및 재생될 뿐만 아니라 세포 신호 전달과 DNA 및 RNA 합성에도 필수적인 역할을 한다. - 뉴클레오타이드 - 폴리뉴클레오타이드
폴리뉴클레오타이드는 DNA와 RNA를 구성하는 뉴클레오타이드가 연결된 고분자이며, 생물체의 게놈을 구성하고 생화학 실험, 의학 및 미용 분야에서 활용된다.
| 리보뉴클레오타이드 | |
|---|---|
| 개요 | |
| 유형 | 뉴클레오타이드 |
| 하위 단위 | 인산 오탄당 (리보스) 질소 염기 |
| 관련 화합물 | 디옥시리보뉴클레오타이드 |
| 구조 | |
| 오탄당 | 리보스 |
| 질소 염기 | 아데닌 구아닌 사이토신 유라실 |
| 역할 | |
| 주요 역할 | RNA 구성 단위 세포 신호 전달 효소 보조 인자 |
| 기타 | |
| 관련 용어 | 뉴클레오사이드 DNA |
2. 구조
리보뉴클레오타이드는 인산기, 리보스(5탄당), 핵염기로 구성된다. 핵염기에는 아데닌(A), 구아닌(G), 시토신(C), 우라실(U) 중 하나가 포함된다. 핵염기와 리보스가 결합한 형태는 뉴클레오사이드라고 하며, 여기에 인산기가 하나 결합하면 리보뉴클레오타이드가 된다. 핵염기는 퓨린과 피리미딘에서 파생된 복소환식 화합물이다.
RNA와 DNA는 모두 퓨린 염기인 아데닌(A)과 구아닌(G)을 포함하며, 피리미딘 염기 중 하나로 시토신(C)을 가진다. 그러나 DNA는 티민(T)을, RNA는 우라실(U)을 가진다는 차이점이 있다. 드물게 RNA에서 티민이, DNA에서 우라실이 발견되기도 한다.[1]
리보뉴클레오타이드와 데옥시리보뉴클레오타이드의 주요 차이점은 5탄당의 종류이다. 리보뉴클레오타이드는 리보스를, 데옥시리보뉴클레오타이드는 데옥시리보스를 가진다. 데옥시리보스는 리보스의 2번 탄소의 수산기(-OH)가 수소 원자(-H)로 치환된 형태이다.[26] DNA는 2'-데옥시리보스를 포함하는 핵산으로, RNA는 리보스를 포함하는 핵산으로 정의된다.[1]
리보뉴클레오타이드는 포스포다이에스터 결합을 통해 서로 연결되어 RNA 가닥을 형성한다. 한 뉴클레오타이드의 5'-인산기는 다음 뉴클레오타이드의 3'-수산기와 연결되어 인산기와 5탄당 잔기가 번갈아 나타나는 골격(backbone)을 생성한다. RNA 가닥은 5' 말단에서 3' 말단 방향으로 합성된다.[5][6] RNA의 골격은 친수성이며 극성을 띤다. 중성 pH에서 핵산은 각 인산기가 음전하를 띠므로 전하를 많이 띤다.[7]
핵산은 자발적으로 단량체인 뉴클레오타이드로 가수분해되는 경향이 있다. RNA의 전구체는 GTP, CTP, UTP, ATP이며, ATP는 주요 에너지원이다.[8]
2. 1. 일반적인 구조

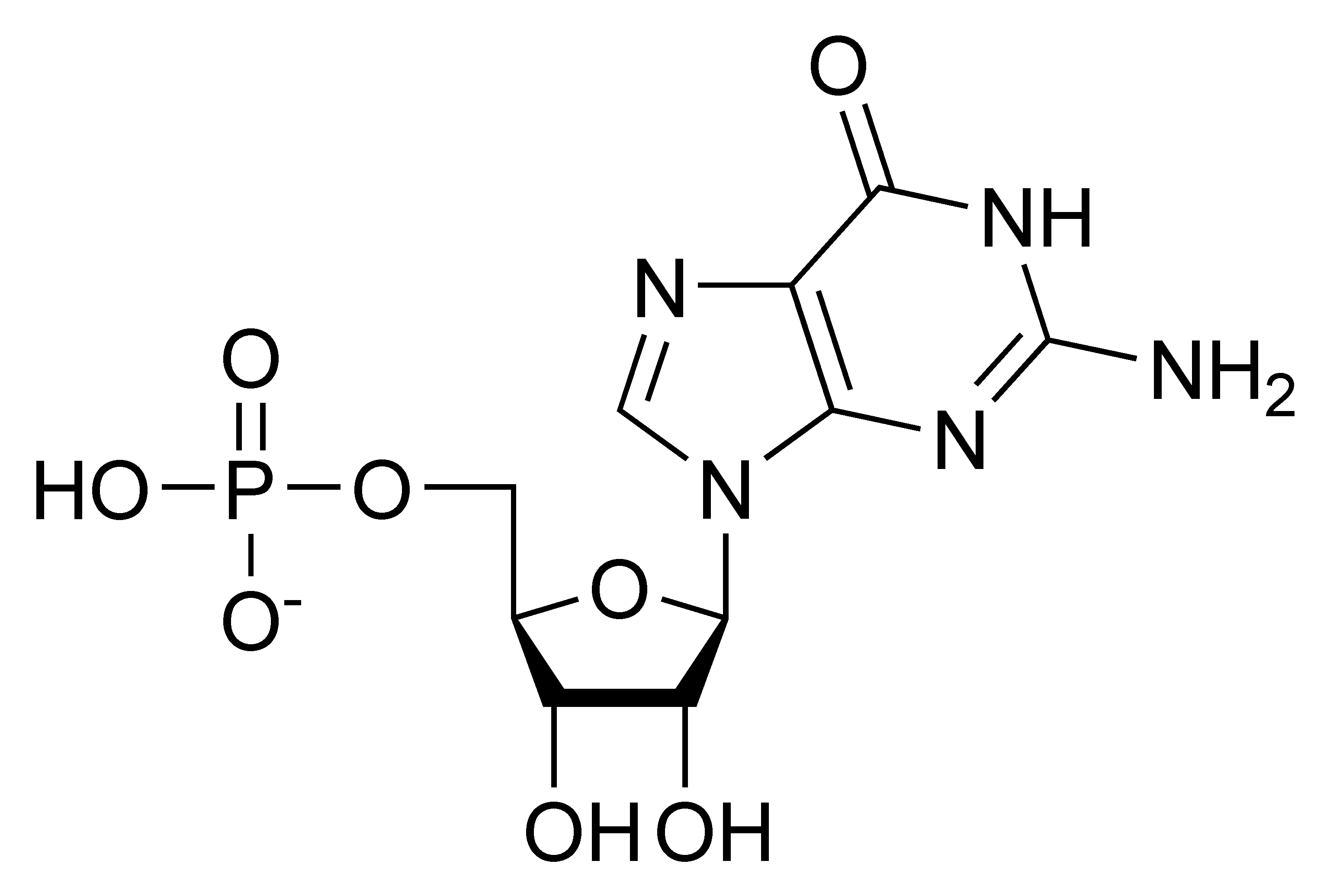

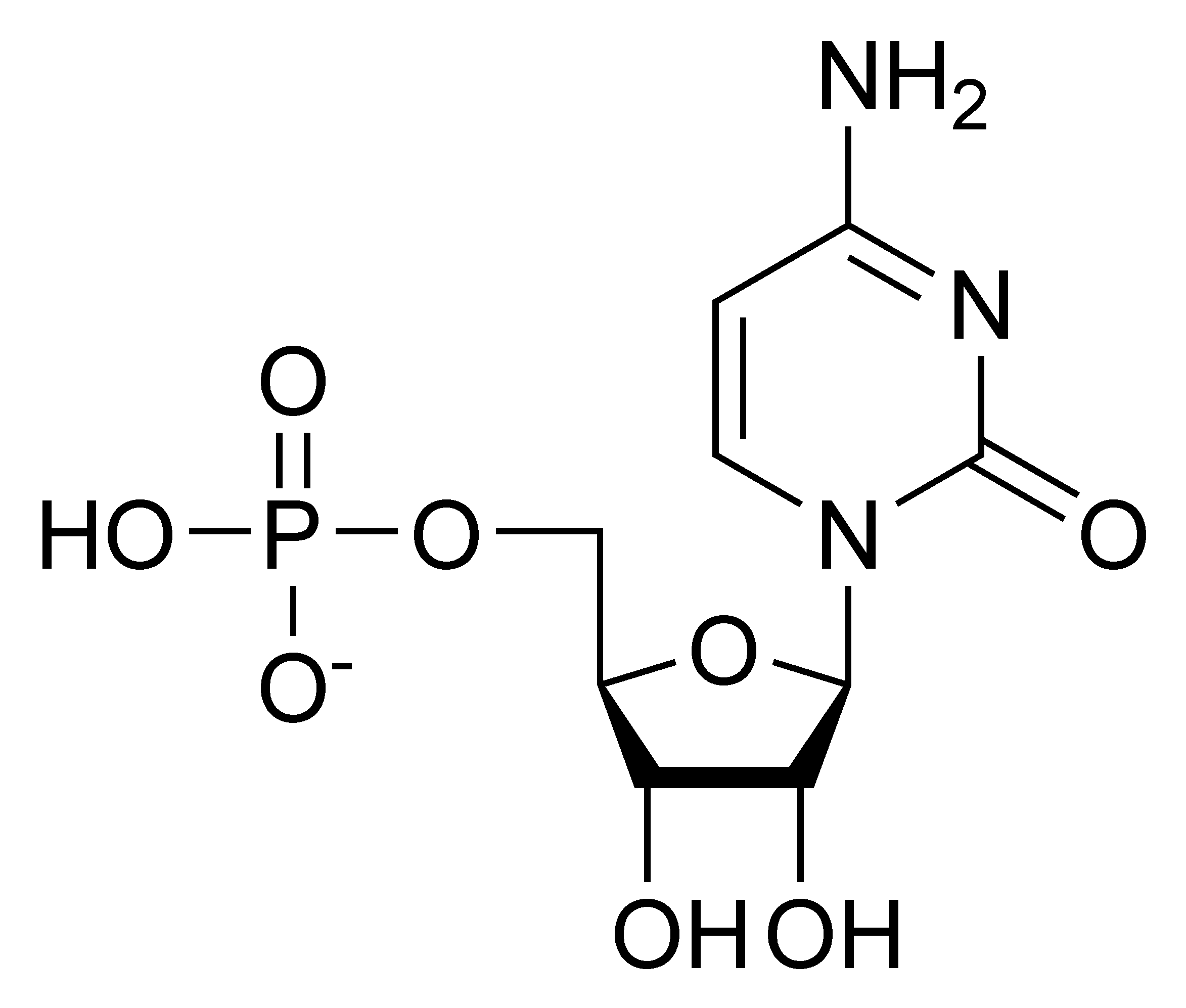
리보뉴클레오타이드의 일반적인 구조는 인산기, 5탄당인 리보스, 핵염기로 구성되며, 핵염기에는 아데닌(A), 구아닌(G), 시토신(C), 우라실(U) 중 하나가 포함된다. 핵염기와 리보스가 결합한 형태를 뉴클레오사이드라고 하며, 여기에 인산기가 하나 결합하면 리보뉴클레오타이드가 된다. 서로 교환 가능한 질소 함유 염기는 퓨린과 피리미딘이라는 두 가지 모체 화합물에서 파생된다. 뉴클레오타이드는 복소환식 화합물인데, 이는 고리 구성원으로 적어도 두 가지 이상의 다른 화학 원소를 포함한다는 것을 의미한다.
RNA와 DNA 모두 두 개의 주요 퓨린 염기인 아데닌(A)과 구아닌(G), 그리고 두 개의 주요 피리미딘을 포함한다. DNA와 RNA 모두에서 피리미딘 중 하나는 시토신(C)이다. 그러나 DNA와 RNA는 두 번째 주요 피리미딘에서 차이를 보인다. DNA는 티민(T)을 포함하는 반면 RNA는 우라실(U)을 포함한다. 티민이 RNA에서, 우라실이 DNA에서 발생하는 드문 경우도 있다.[1]
다음은 RNA의 구조적 단위인 4가지 주요 리보뉴클레오타이드(리보뉴클레오사이드 5'-일인산)이다.
| 뉴클레오타이드 | 기호 | 뉴클레오사이드 |
|---|---|---|
| 아데닐산 (아데노신 5'-일인산) | A, AMP | 아데노신 |
| 구아닐산 (구아노신 5'-일인산) | G, GMP | 구아노신 |
| 우리딜산 (우리딘 5'-일인산) | U, UMP | 우리딘 |
| 시티딜산 (시티딘 5'-일인산) | C, CMP | 시티딘 |
2. 2. DNA 데옥시리보뉴클레오타이드와의 비교
리보뉴클레오타이드와 데옥시리보뉴클레오타이드의 주요 차이점은 5탄당의 종류이다. 리보뉴클레오타이드는 리보스를, 데옥시리보뉴클레오타이드는 데옥시리보스를 가진다. 데옥시리보스는 리보스의 2번 탄소에 있는 수산기(-OH)가 수소 원자(-H)로 치환된 형태이다.[26] DNA와 RNA의 두 종류의 5탄당은 모두 β-푸라노스(닫힌 5원 고리) 형태이며, 이는 핵산의 정체성을 정의한다. DNA는 2'-데옥시리보스 핵산을 포함하는 것으로 정의되는 반면, RNA는 리보스 핵산을 포함하는 것으로 정의된다.[1]DNA는 티민(T)을 염기로 가지지만, RNA는 티민 대신 우라실(U)을 가진다. RNA가 티민을 포함하고 DNA가 우라실을 포함하는 드문 경우도 있다.[25]
RNA의 구성 단위가 되는 4가지 주요 리보뉴클레오타이드는 다음과 같다.
2. 3. 뉴클레오타이드의 연결
리보뉴클레오타이드는 포스포다이에스터 결합을 통해 서로 연결되어 RNA 가닥을 형성한다. 한 뉴클레오타이드의 5'-인산기는 다음 뉴클레오타이드의 3'-수산기와 연결되어 인산기와 펜토스 잔기가 번갈아 나타나는 백본을 생성한다. 다핵산체 각 말단에는 포스포디에스터 결합이 없다.[5] 포스포디에스터 결합은 RNA 중합 효소에 의해 리보뉴클레오타이드 사이에서 형성된다. RNA 가닥은 사슬의 마지막 리보뉴클레오타이드의 3'-수산기가 친핵체로 작용하여 들어오는 리보뉴클레오타이드의 5'-삼인산기에 친수성 공격을 가하고 피로인산을 부산물로 방출하면서 5' 말단에서 3' 말단 방향으로 합성된다.[6] 뉴클레오타이드의 물리적 특성으로 인해 RNA의 백본은 매우 친수성이며 극성을 띤다. 중성 pH에서 핵산은 각 인산기가 음전하를 띠므로 전하를 많이 띤다.[7]DNA와 RNA는 모두 아미노산보다 결합할 가능성이 열역학적으로 낮은 뉴클레오사이드 인산염, 즉 모노뉴클레오타이드 단량체로 구성된다. 포스포디에스터 결합이 가수분해될 때 상당한 양의 자유 에너지가 방출되므로, 핵산은 자발적으로 모노뉴클레오타이드로 가수분해되는 경향이 있다. RNA의 전구체는 GTP, CTP, UTP, ATP이며, ATP는 그룹 전달 반응에서 주요 에너지원이다.[8]
3. 기능
리보뉴클레오타이드는 데옥시리보뉴클레오타이드의 전구체로, DNA 복제 및 복구에 필수적인 데옥시리보뉴클레오타이드(dNTP) 합성에 관여한다. DNA 중합 효소는 DNA 합성 과정에서 리보뉴클레오타이드보다 데옥시리보뉴클레오타이드를 선택적으로 사용하지만, 일부는 DNA에 리보뉴클레오타이드를 통합시키기도 한다.
3. 1. 데옥시리보뉴클레오타이드의 전구체
리보뉴클레오타이드 환원효소는 리보뉴클레오타이드를 데옥시리보뉴클레오타이드로 환원시키는 반응을 촉매한다. 리보뉴클레오타이드 환원효소(RNR)는 DNA 복제 및 복구에 필요한 네 가지 데옥시리보뉴클레오타이드(dNTP)의 합성에 관여하는 마지막 단계를 담당하므로 모든 생물체에게 필수적인 효소이다.[10] 이 반응에는 티오레독신과 티오레독신 환원효소의 두 가지 다른 단백질이 필요하다. 리보뉴클레오사이드 이인산(NDP)은 티오레독신에 의해 환원되어 데옥시리보뉴클레오사이드 이인산(dNTP)이 된다.일반적인 반응은 다음과 같다.[11]
:리보뉴클레오사이드 이인산 + NADPH + H+ -> 데옥시리보뉴클레오사이드 이인산 + NADP+ + H2O
이 방정식을 예시로 들면, dATP와 dGTP는 각각 ADP와 GDP로부터 합성된다. 그들은 먼저 RNR에 의해 환원된 다음 뉴클레오시드 디포스포키나아제에 의해 인산화되어 dATP와 dGTP가 된다. 리보뉴클레오타이드 환원효소는 알로스테릭 효과에 의해 조절된다. 일단 dATP가 리보뉴클레오타이드 환원효소에 결합하면 데옥시리보뉴클레오타이드의 과잉을 나타내므로 효소의 전체 촉매 활성이 감소한다. 이러한 피드백 억제는 ATP가 결합하면 역전된다.[17]
3. 2. 리보뉴클레오타이드의 구분
DNA 합성 과정에서 DNA 중합 효소는 데옥시리보뉴클레오타이드보다 훨씬 더 높은 수준으로 존재하는 리보뉴클레오타이드를 선택적으로 배제해야 한다. DNA 복제는 유기체의 게놈을 유지하기 위해 정확해야 하므로 선택성은 매우 중요하다. Y-계열 DNA 중합효소의 활성 부위가 리보뉴클레오타이드에 대한 높은 선택성을 유지하는 데 책임이 있음이 밝혀졌다.[12] 대부분의 DNA 중합효소는 또한 리보스 고리의 2'-수산기를 입체적으로 차단할 수 있는 부피가 큰 측쇄 잔기를 통해 활성 부위에서 리보뉴클레오타이드를 배제하도록 갖춰져 있다. 그러나 많은 핵 복제 및 복구 DNA 중합효소가 리보뉴클레오타이드를 DNA에 통합시키는데,[13][14] 이는 배제 메커니즘이 완벽하지 않음을 시사한다.[15]4. 합성
리보뉴클레오타이드는 작은 분자들로부터 새로 합성되거나(de novo 합성), 재활용 경로를 통해 합성될 수 있다. 퓨린 뉴클레오타이드(아데닌, 구아닌)와 피리미딘 뉴클레오타이드(시토신, 우라실)는 각각 다른 경로를 통해 합성된다.
RNA 세계 가설에 따르면, 초기 지구 환경에는 자유롭게 떠다니는 리보뉴클레오타이드가 존재했을 것으로 추정된다. 이것들은 일련으로 결합하여 RNA를 형성하는 기본적인 분자였다. RNA는 신뢰할 수 있는 정보 전달에 필요한 퓨린 및 피리미딘 뉴클레오타이드로 구성되어 있으며, 따라서 다윈의 자연 선택과 진화에 필요하다. 최근 연구에 따르면, 활성화된 피리미딘 리보뉴클레오타이드가 원시 지구 환경과 유사한 조건에서 합성될 수 있음이 밝혀졌다.[18] 합성의 출발 물질(시아나미드, 시아노아세틸렌, 글리콜알데히드, 글리세르알데히드 및 무기 인산염)은 생명 기원 원료 분자로 여겨진다.[2] Nam 등은 수성 마이크로 액적에서 리보스와 뉴클레오베이스의 직접적인 축합을 입증하여 RNA 형성을 이끄는 핵심 단계를 제시했다.[19] 또한, 젖고 건조한 주기를 사용하여 피리미딘 및 퓨린 리보뉴클레오타이드를 합성하는 생명 기원 과정이 Becker 등에 의해 제시되었다.[20]
4. 1. 리보뉴클레오타이드 합성
리보뉴클레오타이드는 작은 분자들로부터 새로 합성되거나(de novo 합성), 재활용 경로를 통해 합성될 수 있다. 퓨린 뉴클레오타이드(아데닌, 구아닌)와 피리미딘 뉴클레오타이드(시토신, 우라실)는 각각 다른 경로를 통해 합성된다.퓨린 뉴클레오타이드의 생합성은 복잡하며, 여러 효소 반응을 거쳐 이노신산(IMP)을 형성하고, IMP로부터 아데닐산(AMP)과 구아닐산(GMP)이 합성된다. 이 경로는 리보스 5-인산(R5P)이 효소 리보스-인산 디포스포키나제(PRPS1)에 의해 포스포리보실 피로인산(PRPP)으로 전환되는 것으로 시작된다. 퓨린 고리는 11단계를 거쳐 한 번에 몇 개의 원자씩 만들어진다.

퓨린 고리 원자의 기원은 다음과 같다.
| 원자 | 기원 |
|---|---|
| N1 | 아스파르트산의 아민기 |
| C2, C8 | 포름산 |
| N3, N9 | 글루타민의 아미드기 |
| C4, C5, N7 | 글리신 |
| C6 | HCO3-(CO2) |
피리미딘 뉴클레오타이드의 합성은 퓨린 뉴클레오타이드의 합성에 비해 비교적 간단하며, 아스파르트산과 카바모일 인산으로부터 시작하여 우리딜산(UMP)을 거쳐 시티딜산(CTP)이 합성된다.[1]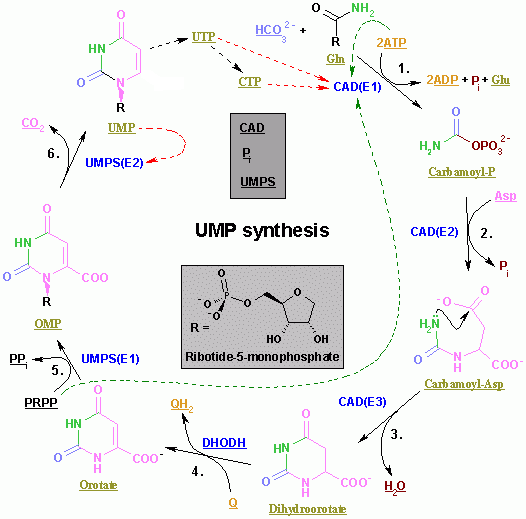
4. 2. 리보뉴클레오타이드의 생명 기원 합성
RNA 세계 가설에 따르면, 초기 지구 환경에는 자유롭게 떠다니는 리보뉴클레오타이드가 존재했을 것으로 추정된다. 이것들은 일련으로 결합하여 RNA를 형성하는 기본적인 분자였다. RNA는 신뢰할 수 있는 정보 전달에 필요한 퓨린 및 피리미딘 뉴클레오타이드로 구성되어 있으며, 따라서 다윈의 자연 선택과 진화에 필요하다. 최근 연구에 따르면, 활성화된 피리미딘 리보뉴클레오타이드가 원시 지구 환경과 유사한 조건에서 합성될 수 있음이 밝혀졌다.[18] 합성의 출발 물질(시아나미드, 시아노아세틸렌, 글리콜알데히드, 글리세르알데히드 및 무기 인산염)은 생명 기원 원료 분자로 여겨진다.[2] Nam 등은 수성 마이크로 액적에서 리보스와 뉴클레오베이스의 직접적인 축합을 입증하여 RNA 형성을 이끄는 핵심 단계를 제시했다.[19] 또한, 젖고 건조한 주기를 사용하여 피리미딘 및 퓨린 리보뉴클레오타이드를 합성하는 생명 기원 과정이 Becker 등에 의해 제시되었다.[20]5. 역사

제임스 왓슨과 프랜시스 크릭이 로잘린드 프랭클린의 X선 결정학 사진을 바탕으로 DNA의 구조를 상세히 설명한 획기적인 논문을 발표하기 전, DNA 발견에 기여한 여러 과학자들이 있었다.[21] 1869년, 스위스 의사 프리드리히 미셰르는 백혈구 핵에서 핵산을 처음으로 분리하고 확인했으며, 이를 "뉴클레인"이라고 명명하여 DNA 발견의 길을 열었다.[22] 미셰르의 연구에 이어 독일 생화학자 알브레히트 코셀은 1878년 "뉴클레인"의 비단백질 성분을 분리하여 핵산에 존재하는 5개의 뉴클레오베이스, 즉 아데닌, 시토신, 구아닌, 티민 및 우라실을 발견했다.[23] 이러한 초기의 발견으로 핵산에 대한 몇 가지 기본적인 사실이 알려졌지만, 그 구조와 기능은 여전히 밝혀지지 않은 상태였다.
1919년 러시아-리투아니아 생화학자 포에버스 레벤은 뉴클레오타이드를 발견하면서 DNA 발견의 문을 다시 열었다. 레벤은 효모 RNA에 존재하는 탄수화물 성분이 리보스임을 처음으로 확인했다. 그러나 가슴샘 핵산의 탄수화물 성분 역시 당이지만 산소 원자가 하나 부족하여 데옥시리보스라고 명명했다는 사실을 발견한 이후에야 그의 발견은 과학계에서 널리 인정받게 되었다. 결국, 레벤은 RNA와 DNA의 구성 성분이 인산-당-염기 단위로 결합한다는 정확한 순서를 파악했고, 이를 뉴클레오타이드라고 명명했다. 레벤에 의해 뉴클레오타이드 구성 성분의 순서가 밝혀졌지만, 뉴클레오타이드 배열의 공간적 구조와 유전 암호는 그의 초기 경력 동안 여전히 밝혀지지 않은 상태였다.[24]
참조
[1]
서적
Lehninger Principles of Biochemistry
W H Freeman
[2]
서적
Functional biochemistry in health & disease: metabolic regulation in health and disease
Wiley
[3]
서적
Biochemistry
Bimal Kumar Dhur of Academic Publishers
[4]
서적
Principles of Biochemistry
W H Freeman
[5]
서적
General, organic, and biological chemistry: an integrated approach
Wiley
[6]
서적
The Desk Encyclopedia of Microbiology
Elsevier
[7]
서적
Molecular Biology
CRC, Taylor & Francis
[8]
서적
Lehninger Principles of Biochemistry
W H Freeman and Co
[9]
서적
A textbook of molecular biotechnology
I.K. International Pub. House
[10]
논문
Biofilm modifies expression of ribonucleotide reductase genes in Escherichia coli.
[11]
서적
Biochemistry
Brooks/Cole Cengage Learning
[12]
논문
Structural Mechanism of Ribonucleotide Discrimination by a Y-Family DNA Polymerase
2011-04-01
[13]
논문
Genome instability due to ribonucleotide incorporation into DNA.
2010-10
[14]
논문
Abundant ribonucleotide incorporation into DNA by yeast replicative polymerases.
2010-03-16
[15]
논문
Ribonucleotide discrimination and reverse transcription by the human mitochondrial DNA polymerase.
2011-09-09
[16]
문서
[17]
서적
Biochemistry
W.H. Freeman
[18]
논문
Synthesis of activated pyrimidine ribonucleotides in prebiotically plausible conditions
2009-05
[19]
논문
Abiotic synthesis of purine and pyrimidine ribonucleosides in aqueous microdroplets
2018-01
[20]
논문
Unified prebiotically plausible synthesis of pyrimidine and purine RNA ribonucleotides
2019-10
[21]
논문
Molecular structure of nucleic acids; a structure for deoxyribose nucleic acid.
1953-04-25
[22]
논문
Discovering DNA: Friedrich Miescher and the early years of nucleic acid research.
2008-01
[23]
논문
Albrecht Kossel, a biographical sketch.
1953-09
[24]
논문
The structure of yeast nucleic acid IV. Ammonia Hydrolysis
[25]
서적
Lehninger Principles of Biochemistry
W H Freeman and Co.
[26]
서적
Functional biochemistry in health & disease : metabolic regulation in health and disease
Wiley
[27]
서적
Biochemistry
Bimal Kumar Dhur of Academic Publishers
[28]
서적
Principles of Biochemistry
W H Freeman & Co
[29]
서적
General, organic, and biological chemistry : an integrated approach
Wiley
[30]
서적
The desk encyclopedia of microbiology
Elsevier Acad. Press
[31]
서적
"*Instant notes in molecular biology.
CRC, Taylor & Francis
[32]
서적
Lehninger Principles of Biochemistry
W H Freeman and Co
[33]
서적
A textbook of molecular biotechnology
I.K. International Pub. House
[34]
논문
Biofilm modifies expression of ribonucleotide reductase genes in Escherichia coli.
[35]
서적
Biochemistry
Brooks/Cole Cengage Learning
[36]
서적
Essentials of biochemistry
Springer
[37]
서적
Biochemistry
Freeman
[38]
논문
Structural Mechanism of Ribonucleotide Discrimination by a Y-Family DNA Polymerase
2011-04-01
[39]
논문
Ribonucleotide discrimination and reverse transcription by the human mitochondrial DNA polymerase.
2011-09-09
[40]
서적
Lehninger Principles of Biochemistry
W H Freeman and Co.
[41]
서적
Biochemistry. Purine Bases can be Synthesized by de Novo or Recycled by Salvage Pathways
http://www.ncbi.nlm.[...]
W H Freeman
[42]
논문
Molecular structure of nucleic acids; a structure for deoxyribose nucleic acid.
1953-04-25
[43]
논문
Discovering DNA: Friedrich Miescher and the early years of nucleic acid research.
2008-01
[44]
논문
Albrecht Kossel, a biographical sketch.
1953-09
[45]
서적
The structure of yeast nucleic acid
Journal of Biological Chemistry 40(2)
[46]
서적
Lehninger Principles of Biochemistry
W H Freeman and Co.
본 사이트는 AI가 위키백과와 뉴스 기사,정부 간행물,학술 논문등을 바탕으로 정보를 가공하여 제공하는 백과사전형 서비스입니다.
모든 문서는 AI에 의해 자동 생성되며, CC BY-SA 4.0 라이선스에 따라 이용할 수 있습니다.
하지만, 위키백과나 뉴스 기사 자체에 오류, 부정확한 정보, 또는 가짜 뉴스가 포함될 수 있으며, AI는 이러한 내용을 완벽하게 걸러내지 못할 수 있습니다.
따라서 제공되는 정보에 일부 오류나 편향이 있을 수 있으므로, 중요한 정보는 반드시 다른 출처를 통해 교차 검증하시기 바랍니다.
문의하기 : help@durumis.com