버크민스터풀러렌
"오늘의AI위키"의 AI를 통해 더욱 풍부하고 폭넓은 지식 경험을 누리세요.
1. 개요
버크민스터풀러렌(C60)은 1985년 해럴드 크로토, 로버트 컬, 리처드 스몰리 등에 의해 처음 발견된 탄소 동소체이다. 이 분자는 20개의 육각형과 12개의 오각형으로 이루어진 절단된 정이십면체 구조를 가지며, 축구공과 유사한 형태를 띤다. C60은 벤젠 등 유기 용매에 약간 용해되며, 순수한 용액은 짙은 보라색을 띤다. 전기적 특성, 화학적 반응성, 광학적 성질을 가지고 있으며, 태양광 발전, 광전자 재료 등 다양한 분야에 응용된다. C60은 빛에 민감하며, 빛에 노출되면 분해되어 독성을 띨 수 있어 취급에 주의가 필요하다.
더 읽어볼만한 페이지
| 버크민스터풀러렌 - [화학 물질]에 관한 문서 | |
|---|---|
| 일반 정보 | |
 | |
 | |
| IUPAC 명칭 | (C60-Ih)[5,6]풀러렌 |
| 다른 이름 | 버키볼 풀러렌-C60 [60]풀러렌 |
| 식별 정보 | |
| InChI | 1/C60/c1-2-5-6-3(1)8-12-10-4(1)9-11-7(2)17-21-13(5)23-24-14(6)22-18(8)28-20(12)30-26-16(10)15(9)25-29-19(11)27(17)37-41-31(21)33(23)43-44-34(24)32(22)42-38(28)48-40(30)46-36(26)35(25)45-39(29)47(37)55-49(41)51(43)57-52(44)50(42)56(48)59-54(46)53(45)58(55)60(57)59 |
| InChIKey | XMWRBQBLMFGWIX-UHFFFAOYAU |
| InChIKey1 | XMWRBQBLMFGWIX-UHFFFAOYSA-N |
| 베일슈타인 등록 번호 | 5901022 |
| CAS 등록 번호 | 99685-96-8 |
| 펍켐 CID | 123591 |
| 켐스파이더 ID | 110185 |
| ChEBI | 33128 |
| UNII | NP9U26B839 |
| 표준 InChIKey | XMWRBQBLMFGWIX-UHFFFAOYSA-N |
| SMILES | c12c3c4c5c2c2c6c7c1c1c8c3c3c9c4c4c%10c5c5c2c2c6c6c%11c7c1c1c7c8c3c3c8c9c4c4c9c%10c5c5c2c2c6c6c%11c1c1c7c3c3c8c4c4c9c5c2c2c6c1c3c42 |
| 표준 InChI | 1S/C60/c1-2-5-6-3(1)8-12-10-4(1)9-11-7(2)17-21-13(5)23-24-14(6)22-18(8)28-20(12)30-26-16(10)15(9)25-29-19(11)27(17)37-41-31(21)33(23)43-44-34(24)32(22)42-38(28)48-40(30)46-36(26)35(25)45-39(29)47(37)55-49(41)51(43)57-52(44)50(42)56(48)59-54(46)53(45)58(55)60(57)59 |
| 물리적 성질 | |
| 분자식 | C60 |
| 외관 | 검은색 바늘 모양 결정 |
| 밀도 | 1.65 g/cm³ |
| 증기압 | 0.4–0.5 Pa (T ≈ 800 K); 14 Pa (T ≈ 900 K) |
| 용해도 | 물에 불용성 |
| 결정 구조 | |
| 결정계 | 면심 입방 구조, Pearson symbol cF1924 |
| 공간군 | Fmm, No. 225 |
| 격자 상수 a | 1.4154 nm |
| 위험성 | |
| 신호어 | 경고 |
2. 역사
버크민스터풀러렌 분자에 대한 이론적 예측은 1960년대 후반과 1970년대 초에 나타났다.[11][12][13][14] 1984년 에릭 롤핑, 도널드 콕스, 앤드루 캘더는 초음속 헬륨 빔에서 레이저를 사용하여 탄소를 증발시키는 실험을 통해 최초로 C60을 생성했지만, 이것이 버크민스터풀러렌이라는 것을 인지하지는 못했다.[14][15]
해럴드 크로토와 리처드 스몰리 팀은 1985년의 C60 구조를 버크민스터풀러렌으로 인식한 연구 이전에, 천체 물리학자들은 적색 거성에서 나오는 적외선 방출을 연구하기 위해 분광학자들과 함께 작업하고 있었다.[16][17][18] 리처드 스몰리 팀은 레이저 증발 기술을 사용하여 적색 탄소별에서 방출된 것과 동일한 파장에서 적외선을 방출할 수 있는 탄소 클러스터를 만들 수 있었다.[16][19]
2. 1. 발견과 명명
해럴드 크로토, 리처드 스몰리 등은 레이저 증발을 사용하여 흑연에서 C''n'' 클러스터(''n'' > 20이고 짝수)를 발견했는데, 이 중 가장 흔한 것은 C60과 C70이었다. 이들은 C60이 케이지형 분자, 즉 정규 잘린 이코사헤드론임을 발견했다.[16][20] 720 원자 질량 단위에서 강한 피크는 60개의 탄소 원자를 가진 탄소 분자가 형성되고 있음을 나타냈지만, 구조적 정보는 제공하지 않았다. 연구 그룹은 반응성 실험 후 가장 유력한 구조가 구형 분자라고 결론 내렸다.[11]크로토, 컬, 스몰리는 버크민스터풀러렌 및 관련 풀러렌을 발견한 공로로 1996년 노벨 화학상을 수상했다.[11]
이 분자는 미국의 건축가이자 발명가인 R. 버크민스터 풀러의 이름을 따서 명명되었다. 풀러는 C60과 유사한 지오데식 돔 구조를 설계했으며, 버크민스터풀러렌이 발견되기 전 해인 1983년에 사망했다.[11] "버키볼"이라는 별명으로도 불린다.[24][25]
2. 2. 초기 연구
1960년대 후반과 1970년대 초, 버크민스터풀러렌 분자에 대한 이론적 예측이 있었다.[11][12][13][14] 1984년 에릭 롤핑, 도널드 콕스, 앤드루 캘더는 초음속 헬륨 빔에서 레이저를 사용하여 탄소를 증발시키는 실험을 통해 최초로 C60을 생성했지만, 이것이 버크민스터풀러렌이라는 것을 인지하지는 못했다.[14][15]1985년 라이스 대학교의 해럴드 크로토, 제임스 R. 히스, 숀 C. 오브라이언, 로버트 컬, 리처드 스몰리는 롤핑, 콕스, 캘더의 연구를 반복하여 C60의 구조를 버크민스터풀러렌으로 인식했다.[20]
1989년 물리학자 볼프강 크래치머, 콘스탄티노스 포스티로풀로스, 도널드 R. 호프만은 탄소 먼지(그을음)의 얇은 필름에서 비정상적인 광학 흡수를 관찰했는데, 이는 C60의 존재를 시사하는 증거였다.[21][22]
1990년 크래치머 연구팀은 아크 생성 그을음으로부터 C60을 분리하고 정제하는 데 성공했다. 이 추출물은 투과 전자 현미경과 X선 결정 분석에서 약 1.0 nm의 반 데르 발스 반경에서 구형 C60 분자의 배열과 일치했으며, 질량 분석에서 C60에 대해 예상되는 분자 질량 720 Da(및 C70에 대해 840 Da)와 일치했다.[23] 이 방법은 하루에 그램 단위로 물질을 준비하기에 간단하고 효율적이었으며, 풀러렌 연구를 촉진했고 오늘날에도 풀러렌의 상업적 생산에 적용되고 있다.
3. 구조
버크민스터풀러렌은 60개의 꼭짓점과 32개의 면(20개의 육각형과 12개의 오각형, 오각형끼리는 꼭짓점을 공유하지 않음), 90개의 모서리를 가진 절단된 정이십면체이다. 각 다각형의 꼭짓점에는 탄소 원자가 있고 각 다각형 모서리에는 결합이 있다.[29] 
분자의 반 데르 발스 지름은 약 1.01 나노미터(nm)이다. 핵간 거리는 약 0.71 nm이다. 탄소 원자는 6개의 전자를 가지고 있어 전자 구조는 2, 4이다. 안정화되기 위해서는 최외각에 8개의 전자가 필요하지만, 3개의 탄소 원자와 공유 결합을 하면 최외각 전자가 7개뿐이다. 이는 결합에 참여하지 않는 전자가 분자 전체에 걸쳐 비편재화되어 있음을 의미한다. 이 자유 전자 운동으로 인해 백민스터풀러렌은 매우 좋은 도체가 되며, 나노기술에서 유용하게 사용된다. 탄소 원자는 질소 또는 붕소 원자로 대체될 수 있으며, 각각 C59N 또는 C59B를 생성한다.[30]
3. 1. 결합 특징
버크민스터풀러렌은 20개의 육각형과 12개의 오각형으로 이루어진 절단된 정이십면체 구조를 가지며, 각 다각형의 꼭짓점은 탄소원자이고 다각형의 변은 탄소-탄소 결합이다. C60 분자에는 두 종류의 결합 거리가 있다. 6:6 고리 결합(두 육각형 사이)은 이중 결합으로 간주할 수 있으며, 6:5 결합(육각형과 오각형 사이)보다 짧다. 평균 결합 길이는 약 0.14 nm이다.[1] C60 구조 내의 탄소 원자는 각각 3개의 다른 탄소 원자와 공유 결합을 한다.4. 성질
버크민스터풀러렌(C60)은 벤젠, 톨루엔, 이황화 탄소 등 유기 용매에 녹으며, 용액은 보라색을 띤다.[33][34][35] 고체 상태에서는 면심 입방(fcc) 구조를 가지며, 약 -20 °C에서 회전 전이를 일으켜 격자 상수가 1.411에서 1.4154 nm로 급격히 증가한다.[38] 높은 압력 하에서는 다이아몬드보다 단단한 초경재료로 변환될 수 있다.[38]
C60의 용해도(g/L)는 아래 표와 같다.[33][34][35]
| 용매 | 용해도 (g/L) |
|---|---|
| 1-클로로나프탈렌 | 51 |
| 1-메틸나프탈렌 | 33 |
| 1,2-다이클로로벤젠 | 24 |
| 1,2,4-트라이메틸벤젠 | 18 |
| 테트라하이드로나프탈렌 | 16 |
| 이황화 탄소 | 8 |
| 1,2,3-트라이브로모프로페인 | 8 |
| 자일렌 | 5 |
| 브로모포름 | 5 |
| 쿠멘 | 4 |
| 톨루엔 | 3 |
| 벤젠 | 1.5 |
| 사염화 탄소 | 0.447 |
| 클로로포름 | 0.25 |
| 헥산 | 0.046 |
| 사이클로헥산 | 0.035 |
| 테트라하이드로푸란 | 0.006 |
| 아세토니트릴 | 0.004 |
| 메탄올 | 0.00004 |
| 물 | 1.3 × 10−11 |
| 펜탄 | 0.004 |
| 옥탄 | 0.025 |
| 아이소옥탄 | 0.026 |
| 데칸 | 0.070 |
| 도데칸 | 0.091 |
| 테트라데칸 | 0.126 |
| 다이옥산 | 0.0041 |
| 메시틸렌 | 0.997 |
| 다이클로로메탄 | 0.254 |

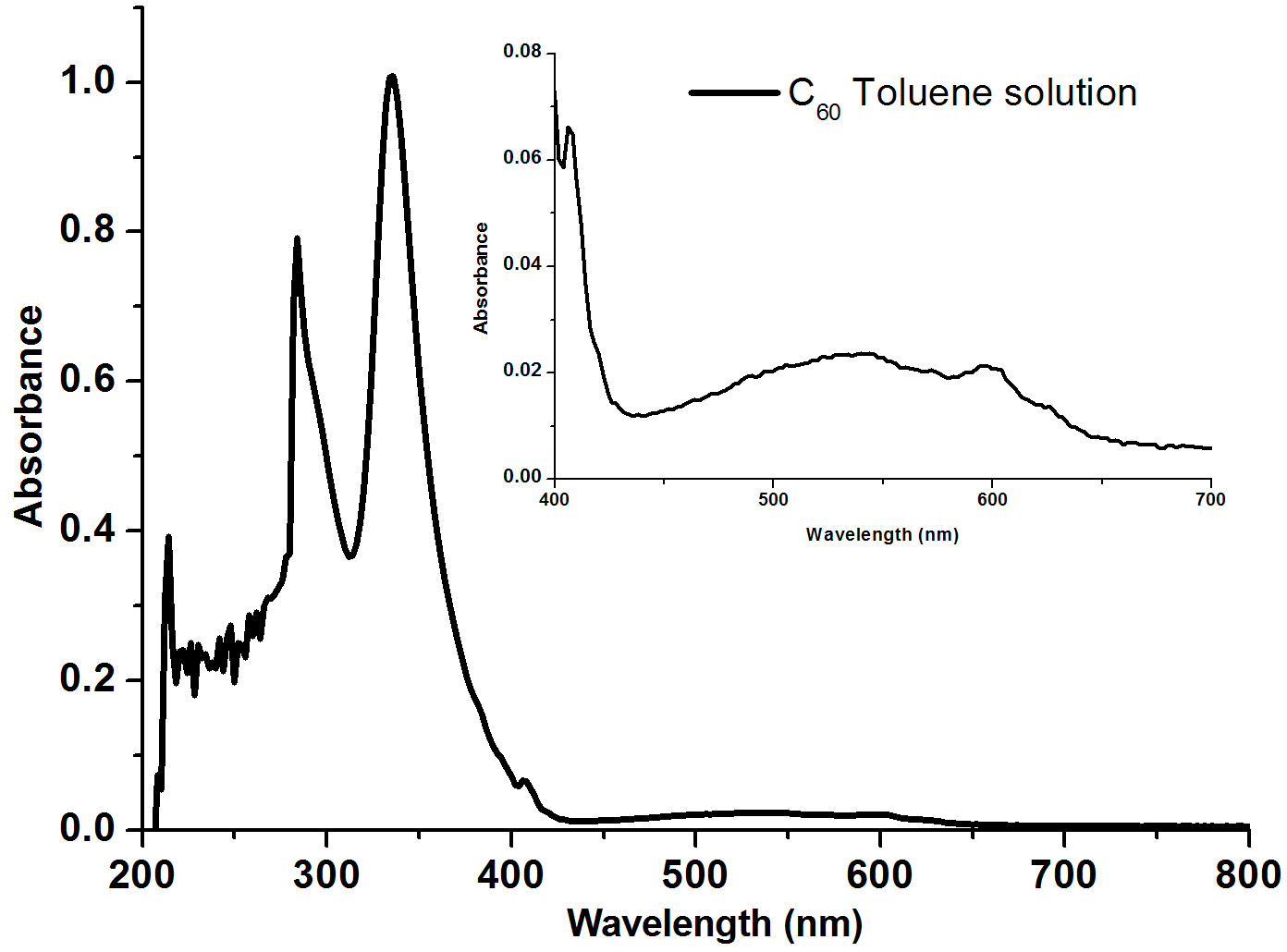
순수한 C60 용액은 짙은 보라색을 띠며, 용액을 증발시키면 갈색 잔류물이 남는다. 이는 C60 분자가 녹색광을 흡수하는 분자 수준의 띠 에너지 폭이 좁아 파란색과 빨간색 빛을 일부 투과하기 때문이다. 건조 시에는 분자 간 상호 작용으로 에너지 띠가 넓어져 보라색이 갈색으로 변한다.[16]
C60 필름과 용액은 강한 비선형 광학 특성을 가지며, 특히 빛의 세기에 따라 광학 흡수가 증가하는 포화 흡수 현상을 보인다.
한동안 버크민스터풀러렌은 파동-입자 이중성을 보이는 가장 큰 분자로 알려졌었다.[31] 2020년에는 프탈로시아닌이라는 염료 분자가 이러한 이중성을 보였다.[32]
4. 1. 전기적 성질
는 약 ≈1.6 eV에서 광학 흡수 임계값을 갖는 갈색 고체이다.[39] 이는 0.1–0.3 eV의 낮은 활성화 에너지를 갖는 n형 반도체이다.[40] 이 전도성은 고유 또는 산소 관련 결함에 기인한다.[40] Fcc C60은 팔면체 및 사면체 위치에 불순물 원자를 수용할 수 있을 정도로 충분히 큰(각각 0.6 및 0.2 nm) 공극을 포함하고 있다. 알칼리 금속이 이러한 공극에 도핑되면 C60은 반도체에서 도체 또는 심지어 초전도체로 변환된다.[38][41]버크민스터풀러렌 구조 내의 탄소 원자는 각각 3개의 다른 탄소 원자와 공유 결합을 한다. 탄소 원자는 6개의 전자를 가지고 있으므로, 전자 구조는 2,4이다. 탄소 원자가 안정화되기 위해서는 최외각에 8개의 전자가 필요하지만, 3개의 탄소 원자와의 공유 결합으로는 최외각 전자가 7개밖에 되지 않는다. 이는 모든 탄소 원자상의 결합에 관여하지 않는 전자가 분자 전체에 걸쳐 비편재화되어 있음을 의미한다. 전자는 전하를 가지고 있으므로, 이 자유 전자 운동은 버크민스터풀러렌이 매우 좋은 도체가 될 수 있음을 뜻한다.
4. 2. 화학적 성질
는 6개의 가역적인 1전자 환원을 거쳐 궁극적으로 을 생성한다. 산화는 비가역적이다. 첫 번째 환원은 약 -1.0 V (Fc/)에서 일어나는데, 이는 C60이 전자 수용에 소극적임을 보여준다.[43] C60은 오각형 고리에 이중 결합을 갖는 것을 피하려는 경향이 있어 전자 비편재화가 좋지 않으며, 이로 인해 이 "초방향족성"이 되지 않는다. C60은 전자 결핍 알켄처럼 작용한다. 예를 들어, 일부 친핵체와 반응한다.[43]C60은 약간의 방향족성을 나타내지만, 여전히 국소적인 이중 및 단일 C-C 결합 특성을 반영한다. 따라서 C60은 수소와 부가 반응을 거쳐 폴리하이드로풀러렌을 생성할 수 있다. C60은 또한 버치 환원 반응을 겪는다. 예를 들어, C60은 액체 암모니아에서 리튬과 반응한 후, ''tert''-부탄올과 반응하여 C60H18, C60H32, C60H36과 같은 폴리하이드로풀러렌 혼합물을 생성하며, C60H32가 주요 생성물이다. 이 폴리하이드로풀러렌 혼합물은 2,3-디클로로-5,6-디시아노-1,4-벤조퀴논에 의해 다시 C60으로 산화될 수 있다.
선택적 수소화 방법이 존재한다. 동일한 조건에서 C60과 9,9′,10,10′-다이하이드로안트라센의 반응은 반응 시간에 따라 각각 C60H32 및 C60H18을 선택적으로 생성한다.[42]
C60에는 플루오린, 염소, 브로민의 첨가가 일어난다. 플루오린 원자는 1,2-첨가에 충분히 작지만, Cl2와 Br2는 입체 효과로 인해 먼 C 원자에 첨가된다. 예를 들어, C60Br8 및 C60Br24에서 Br 원자는 서로 1,3- 또는 1,4-위치에 있다. 다양한 조건에서 C60의 수많은 할로겐화 유도체를 생성할 수 있으며, 일부는 다른 가능한 이성질체보다 하나 또는 두 개의 이성질체에 대해 특이한 선택성을 보인다. 플루오린과 염소의 첨가는 일반적으로 C60 골격을 드럼 모양의 분자로 평평하게 만든다.[42]
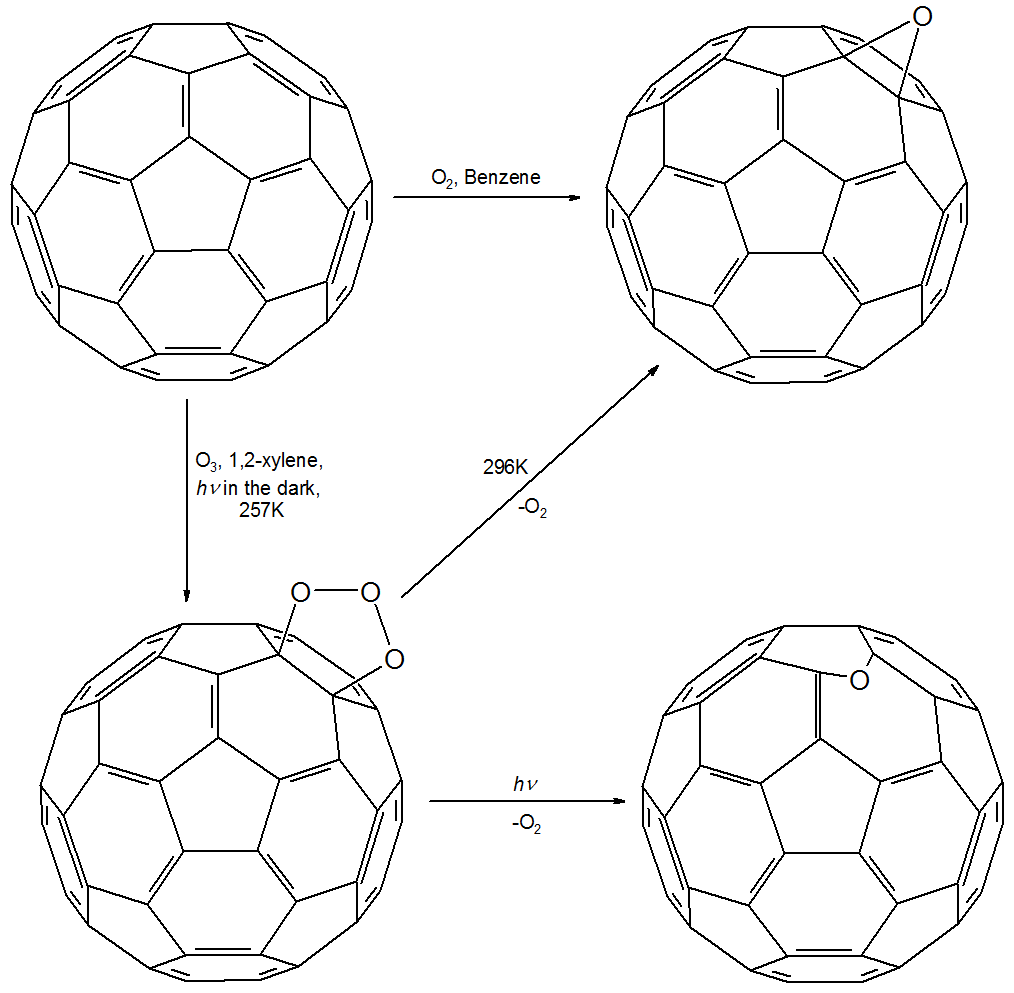
C60의 용액은 산소화되어 에폭사이드 C60O가 될 수 있다. C60을 1,2-자일렌에서 257K로 오존화하면 중간 오존화물 C60O3가 생성되며, 이는 두 가지 형태의 C60O로 분해될 수 있다. 296K에서 C60O3를 분해하면 에폭사이드가 생성되지만, 광분해를 하면 O 원자가 5,6-가장자리를 연결하는 생성물이 생성된다.[42]
딜스-알더 반응은 C60을 기능화하는 데 흔히 사용된다. C60과 적절하게 치환된 다이엔의 반응은 해당 부가물을 생성한다. C60과 3,6-다이아릴-1,2,4,5-테트라진 사이의 딜스-알더 반응은 C62를 생성한다. C62는 4원 고리가 6원 고리 4개에 둘러싸인 구조를 갖는다.
C60 분자는 [2+2] 고리 첨가 반응을 통해 결합될 수도 있으며, 덤벨 모양의 화합물 C120을 생성한다. 이 결합은 C60을 소량의 KCN 촉매와 함께 고속 진동 밀링하여 얻어진다. 이 반응은 가역적이어서 C120은 450K에서 가열하면 다시 두 개의 C60 분자로 해리된다. 고압 및 고온 조건에서 C60 간의 반복적인 [2+2] 고리 첨가 반응은 중합된 풀러렌 사슬과 네트워크를 생성한다. 이러한 중합체는 일단 형성되면 상온 및 상압에서 안정하게 유지되며, 실온 이상에서 강자성을 나타내는 것과 같이 매우 흥미로운 전자적 및 자기적 특성을 갖는다.[42]
C60은 자유 라디칼과의 반응이 쉽게 일어난다. C60을 이황화물 RSSR과 혼합하면 혼합물을 조사했을 때 라디칼 C60SR•이 자연적으로 형성된다. 라디칼 종 C60Y•의 안정성은 Y의 입체 효과에 크게 의존한다. ''tert''-부틸 할라이드를 광분해하여 C60과 반응시키면 가역적인 케이지 간 C-C 결합이 형성된다.[42]
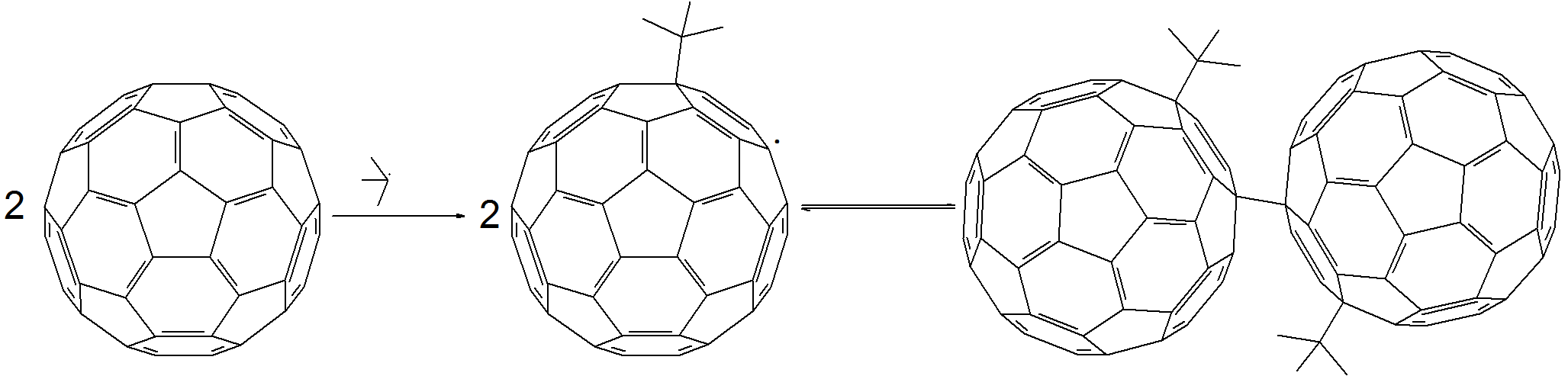
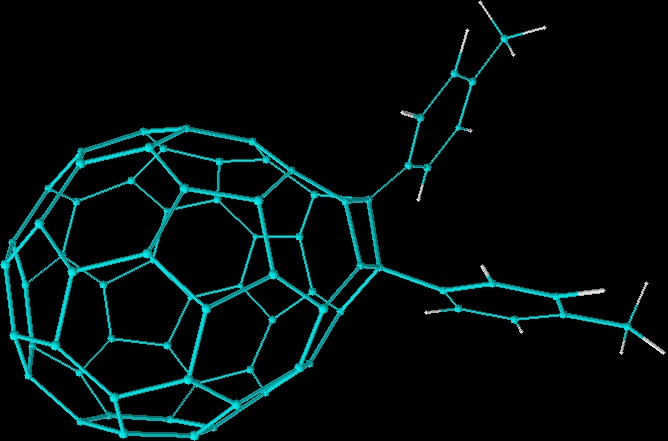
사이클로프로파네이션(Cyclopropanation)(빙겔 반응)은 C60을 기능화하는 또 다른 일반적인 방법이다. C60의 사이클로프로파네이션은 입체적 요인으로 인해 주로 두 개의 육각형의 접합부에서 발생한다. 첫 번째 사이클로프로파네이션은 염기 존재 하에서 β-브로모말론산염을 C60과 반응시켜 수행되었다. 사이클로프로파네이션은 또한 디아조메탄과 쉽게 일어난다. 예를 들어, 디페닐디아조메탄은 C60과 쉽게 반응하여 화합물 C61Ph2를 생성한다.[42] 사이클로프로파네이션을 통해 제조된 페닐-C61-부티르산 메틸 에스터 유도체는 유기 태양 전지에 사용하기 위해 연구되었다.
C60은 더 흔한 알켄과 유사한 착물을 형성한다. 몰리브덴, 텅스텐, 백금, 팔라듐, 이리듐, 티타늄 등의 착물이 보고되었다. 펜타카르보닐 종은 광화학 반응에 의해 생성된다.
: M(CO)6 + C60 → M(''η''2-C60)(CO)5 + CO (M = Mo, W)
백금 착물의 경우, 불안정한 에틸렌 리간드는 열 반응에서 이탈기이다.
: Pt(''η''2-C2H4)(PPh3)2 + C60 → Pt(''η''2-C60)(PPh3)2 + C2H4
티타노센 착물 또한 보고되었다.
: (''η''5-Cp)2Ti(''η''2-(CH3)3SiC≡CSi(CH3)3) + C60 → (''η''5-Cp)2Ti(''η''2-C60) + (CH3)3SiC≡CSi(CH3)3
C60과의 첨가물을 위한 바스카 착물과 같은 배위 불포화 전구체:
: ''trans''-Ir(CO)Cl(PPh3)2 + C60 → Ir(CO)Cl(''η''2-C60)(PPh3)2
이리듐 착물 중 하나인 [Ir(''η''2-C60)(CO)Cl(Ph2CH2C6H4OCH2Ph)2]가 제조되었으며, 여기서 금속 중심은 C60 게스트를 감싸는 두 개의 전자 풍부한 '팔'을 투사한다.[44]
금속 원자 또는 H2 및 비활성 기체와 같은 특정 작은 분자는 C60 케이지 내부에 캡슐화될 수 있다. 이러한 내포 풀러렌은 일반적으로 아크 반응기에서 금속 원자를 도핑하거나 레이저 증발을 통해 합성된다. 이러한 방법은 내포 풀러렌의 수율이 낮으며, 더 나은 방법은 케이지를 열고, 원자 또는 분자를 채워 넣고, 특정 유기 반응을 사용하여 개구부를 닫는 것이다. 그러나 이 방법은 아직 미성숙하며 이러한 방식으로 소수의 종만 합성되었다.[45]
내포 풀러렌은 캡슐화된 원자 또는 분자뿐만 아니라 풀러렌 자체와도 완전히 다른 뚜렷하고 흥미로운 화학적 특성을 보인다. 캡슐화된 원자는 C60 케이지 내부에서 원형 운동을 수행하는 것으로 나타났으며, 그들의 운동은 핵자기 공명 분광법을 사용하여 추적되었다.[44]
5. 합성
버크민스터풀러렌은 흑연의 레이저 제거 또는 방향족 탄화수소의 열분해로 생성되는 그을음을 이용하여 합성한다. 삭스렛 추출기를 사용하여 유기 용매로 그을음을 추출하는데,[26] 이 과정을 거치면 최대 75%의 C60뿐만 아니라 다른 풀러렌도 포함하는 용액이 만들어진다. 이러한 분획은 크로마토그래피를 사용하여 분리한다.[27] 일반적으로 풀러렌은 탄화수소 또는 할로겐화 탄화수소에 용해되어 알루미나 컬럼을 사용하여 분리한다.[28]
6. 존재
버크민스터풀러렌은 자연에서 가장 흔하게 발견되는 풀러렌이다. 소량의 버크민스터풀러렌은 그을음에서 발견될 수 있다.[5][6]
또한 우주에도 존재한다. 중성 C60은 행성상 성운[7]과 여러 종류의 별에서 관찰되었다.[8] 이온화된 형태인 C60+는 성간 매질에서 확인되었으며,[9] 근적외선에서 확산 성간 띠로 알려진 여러 흡수 특징의 원인이 된다.[10]
7. 응용
버크민스터풀러렌은 독특한 물리적, 화학적 성질을 가지고 있어 다양한 분야에서 활용될 가능성이 높다.
- 광전자 재료: 태양광 발전 분야에서 전자 수용체로 활용될 수 있다.
- 윤활제: 풀러렌의 분자 구조는 윤활 특성을 띌 수 있게 한다.
- 촉매: 풀러렌의 넓은 표면적과 전자 구조는 촉매로 사용될 가능성이 있다.
- 약물 전달체: 풀러렌 내부에 다른 물질을 가두는 방식으로 약물 전달 시스템에 응용될 수 있다.
- 화장품: 일부 화장품 회사에서는 풀러렌을 항산화제로 활용하여 제품을 개발하고 있다.
7. 1. 광전자 재료
버크민스터풀러렌(C60)의 광학 흡수 특성은 태양 스펙트럼과 일치하여 C60 기반 필름이 태양광 발전에 유용할 수 있음을 시사한다. 버크민스터풀러렌은 높은 전자 친화도[46]를 가지고 있어 도너/억셉터 기반 태양 전지에서 가장 흔하게 사용되는 전자 수용체 중 하나이다. C60–고분자 전지에서 최대 5.7%의 변환 효율이 보고되었다.[47]8. 안전성 및 독성
버크민스터풀러렌(C60)은 빛에 민감하여,[52] 빛에 노출되면 분해되어 위험해진다. 빛에 노출된 C60 용액을 섭취하면 암(종양)이 발생할 수 있다.[48][51] 따라서 인체 섭취용 C60 제품은 매우 어두운 환경에서 제조하고, 불투명한 병에 담아 어두운 곳에 보관하며, 저조도 조건에서 섭취하고, 빛에 의한 문제점에 대한 경고 라벨을 부착하는 등 주의가 필요하다.[51]
올리브 오일이나 물에 용해된 C60 용액은 빛을 차단하면 설치류에게 무독성인 것으로 밝혀졌다.[49]
한편, C60은 신체 내, 특히 간에 축적되어 일반적인 경우보다 오랫동안 잔류하며, 잠재적으로 유해한 건강 영향을 유발할 수 있다는 연구 결과가 있다.[50] 2011년부터 2012년까지 진행된 실험에서 C60을 올리브 오일에 녹인 용액을 쥐에게 투여한 결과, 수명이 크게 연장되었다.[49] 이후, C60이 함유된 많은 오일들이 항산화 제품으로 판매되었지만, 빛에 민감하여 독성으로 변할 수 있다는 문제는 해결되지 않았다. 이후 연구에서 빛에 노출되면 오일에 녹인 C60 용액이 분해되어 독성을 띠게 되고, 섭취 후 암(종양) 발생 위험이 "대폭" 증가한다는 사실이 확인되었다.[48][51]
빛에 의한 분해를 피하기 위해 C60 오일은 매우 어두운 환경에서 제조되어야 하며, 불투명한 병에 담아 어두운 곳에 보관하고, 저조도 환경에서 섭취해야 하며, C60에 대한 빛의 위험성을 경고하는 라벨이 부착되어야 한다.[51][52]
일부 생산자는 오일과 관련된 잠재적 문제를 피하기 위해 C60을 물에 용해할 수 있었지만, 이는 C60을 빛으로부터 보호하지 못하므로 동일한 주의가 필요하다.[52]
9. 갤러리
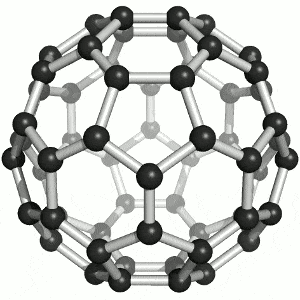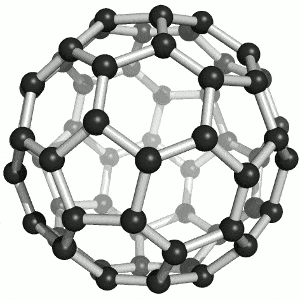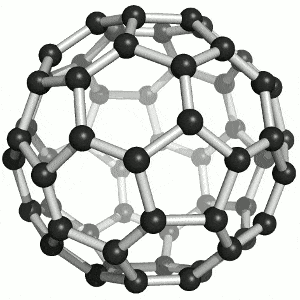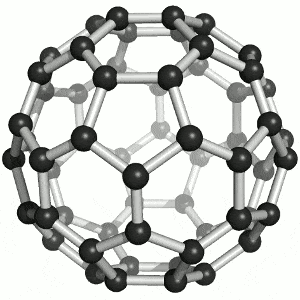
참조
[1]
서적
Nomenclature of Organic Chemistry: IUPAC Recommendations and Preferred Names 2013
The Royal Society of Chemistry
2014
[2]
간행물
Vapor Pressure of C60 Buckminsterfullerene
[3]
웹사이트
Buckyball
https://www.oed.com/[...]
Oxford University Press
2024-04-13
[4]
뉴스
Buckminsterfullerene
The AZo Journal of Materials Online. AZoM.com
2006
[5]
간행물
Fullerenes C60 and C70 in flames
[6]
간행물
Fullerenes synthesis in combustion
[7]
간행물
Detection of C60 and C70 in a Young Planetary Nebula
[8]
간행물
Detection of C60 in embedded young stellar objects, a Herbig Ae/Be star and an unusual post-asymptotic giant branch star
[9]
간행물
Interstellar C60+
[10]
간행물
Laboratory confirmation of C60+ as the carrier of two diffuse interstellar bands
2015-07
[11]
문서
Katz
[12]
문서
Osawa, E. (1970). Kagaku (Kyoto) (in Japanese). 25: 854
[13]
간행물
Hollow molecules
[14]
간행물
Discovering the fullerenes
1997-07-01
[15]
간행물
Production and characterization of supersonic carbon cluster beams
[16]
서적
Science of Fullerenes and Carbon Nanotubes
Academic Press
1996
[17]
간행물
The diffuse interstellar bands. IV – the region 4400-6850 A
[18]
간행물
Remarkable candidates for the carrier of the diffuse interstellar bands: C60+ and other polyhedral carbon ions
[19]
간행물
Laser production of supersonic metal cluster beams
[20]
간행물
C60: Buckminsterfullerene
[21]
문서
"Search for the UV and IR spectra of C60 in laboratory-produced carbon dust"
https://www.springer[...]
[22]
간행물
The infrared and ultraviolet absorption spectra of laboratory-produced carbon dust: evidence for the presence of the C60 molecule
[23]
간행물
Solid C60: A new form of carbon
[24]
웹사이트
What is a geodesic dome?
https://exhibits.sta[...]
Stanford University
2017-04-06
[25]
뉴스
Buckminsterfullerene
The AZo Journal of Materials Online. AZoM.com
2006
[26]
서적
Synthesis and Teknique in Inorganic Chemistry
University Science Books
1999
[27]
문서
Katz
[28]
서적
Inorganic Chemistry
W. H. Freeman
[29]
문서
Katz
[30]
문서
Katz
[31]
간행물
Wave–particle duality of C60
[32]
뉴스
Wave-particle duality in action—big molecules surf on their own waves
https://arstechnica.[...]
2020-07-21
[33]
간행물
Solubility of C60
[34]
간행물
Fullerenes in solutions
[35]
간행물
Solubility of fullerene (C60) in a variety of solvents
[36]
학술지
Phase Transition C60−C60*4C6H6 in Liquid Benzene
[37]
학술지
C70 in Benzene, Hexane, and Toluene Solutions
[38]
문서
Katz
[39]
문서
Katz
[40]
문서
Katz
[41]
문서
Katz
[42]
서적
Inorganic Chemistry
Pearson
[43]
학술지
Discrete Fulleride Anions and Fullerenium Cations
https://escholarship[...]
[44]
서적
Supramolecular Chemistry
Wiley
[45]
학술지
Endohedral metallofullerenes: a unique host–guest association
[46]
학술지
Electronic Structures and Chemical Bonding of Fluorinated Fullerenes Studied
1998
[47]
학술지
Ultrahard bulk amorphous carbon from collapsed fullerene
https://www.nature.c[...]
2021-11
[48]
웹사이트
Comp grad leads research
http://weyburnreview[...]
2021-04-17
[49]
학술지
The prolongation of the lifespan of rats by repeated oral administration of [60]fullerene
2012-06
[50]
학술지
Disposition of fullerene C60 in rats following intratracheal or intravenous administration
[51]
웹사이트
C60 in olive oil causes light-dependent toxicity
https://gwern.net/do[...]
2021-04-15
[52]
간행물
Degradation of C60 by light
https://nature.com/a[...]
1991-05-23
[53]
학술지
フラーレン量産技術
http://www.plastics-[...]
[54]
학술지
Compressibility of solid C60
[55]
학술지
Crystal structure and bonding of ordered C60
[56]
학술지
C60: Buckminsterfullerene
[57]
학술지
Fullerenes C60 and C70 in flames
[58]
학술지
[59]
학술지
[60]
학술지
Wave-particle duality of C60 molecules
[61]
학술지
Vapor Pressure of C60 Buckminsterfullerene
[62]
학술지
C60: Buckminsterfullerene
본 사이트는 AI가 위키백과와 뉴스 기사,정부 간행물,학술 논문등을 바탕으로 정보를 가공하여 제공하는 백과사전형 서비스입니다.
모든 문서는 AI에 의해 자동 생성되며, CC BY-SA 4.0 라이선스에 따라 이용할 수 있습니다.
하지만, 위키백과나 뉴스 기사 자체에 오류, 부정확한 정보, 또는 가짜 뉴스가 포함될 수 있으며, AI는 이러한 내용을 완벽하게 걸러내지 못할 수 있습니다.
따라서 제공되는 정보에 일부 오류나 편향이 있을 수 있으므로, 중요한 정보는 반드시 다른 출처를 통해 교차 검증하시기 바랍니다.
문의하기 : help@durumis.com
