이식편대숙주병
"오늘의AI위키"의 AI를 통해 더욱 풍부하고 폭넓은 지식 경험을 누리세요.
1. 개요
이식편대숙주병(GvHD)은 면역 기능이 저하된 환자에게 이식된 면역 세포가 환자의 조직을 공격하여 발생하는 질환이다. 이식편대숙주병은 주로 골수 이식 후에 발생하며, 급성과 만성 두 가지 형태로 나타난다. 급성 이식편대숙주병은 이식 후 10~100일 사이에 발생하며 피부, 간, 위장관 등을 손상시키고, 만성 이식편대숙주병은 이식 후 90~600일 사이에 발생하여 결합 조직과 외분비선에도 영향을 미친다. 이식편대숙주병의 원인은 면역학적 부조화, 면역 억제, T 세포의 활성화 등이 있으며, 증상으로는 발열, 발진, 설사, 간 기능 장애 등이 나타난다. 치료는 면역억제제와 스테로이드를 사용하며, 예방을 위해서는 HLA 일치, T 세포 제거, 면역억제제 예방 요법 등이 활용된다. 수혈 후 이식편대숙주병은 방사선 처리되지 않은 혈액 수혈로 인해 발생하며, 예방이 중요하고, 일단 발병하면 치사율이 매우 높다.
더 읽어볼만한 페이지
- 면역 질환 - 알레르기
알레르기는 면역 체계가 무해한 물질에 과도하게 반응하여 아토피 피부염, 비염, 천식, 두드러기 등 다양한 증상을 일으키는 질환으로, Gell과 Coombs 분류법에 따라 여러 유형으로 나뉘며, 심각한 경우 아나필락시스를 유발할 수 있고, 유전적, 환경적 요인이 복합적으로 작용하여 발생하며, 알레르겐 회피, 약물, 면역요법 등으로 치료한다. - 면역 질환 - 기회감염
기회감염은 면역 체계가 약화된 사람에게 다양한 병원체에 의해 발생하는 감염으로, 면역력 저하, HIV 감염, 치료 등의 원인에 의해 발생하며, 예방을 위해 면역력 회복, 감염원 회피, 예방적 약물 사용 등의 조치를 취하고, 치료는 원인균에 따라 적절한 약제를 사용하는 것이 중요하다.
| 이식편대숙주병 | |
|---|---|
| 질병 개요 | |
| 이름 | 이식편대숙주병 |
| 영어 이름 | Graft-versus-host disease |
| 약어 | GVHD |
| 증상 | |
| 증상 | (증상에 대한 정보가 제공되지 않았습니다.) |
| 합병증 | |
| 합병증 | (합병증에 대한 정보가 제공되지 않았습니다.) |
| 발병 시기 | |
| 발병 시기 | (발병 시기에 대한 정보가 제공되지 않았습니다.) |
| 지속 기간 | |
| 지속 기간 | (지속 기간에 대한 정보가 제공되지 않았습니다.) |
| 유형 | |
| 유형 | (유형에 대한 정보가 제공되지 않았습니다.) |
| 원인 | |
| 원인 | (원인에 대한 정보가 제공되지 않았습니다.) |
| 위험 요인 | |
| 위험 요인 | (위험 요인에 대한 정보가 제공되지 않았습니다.) |
| 진단 | |
| 진단 | (진단에 대한 정보가 제공되지 않았습니다.) |
| 감별 진단 | |
| 감별 진단 | (감별 진단에 대한 정보가 제공되지 않았습니다.) |
| 예방 | |
| 예방 | (예방에 대한 정보가 제공되지 않았습니다.) |
| 치료 | |
| 치료 | (치료에 대한 정보가 제공되지 않았습니다.) |
| 약물 | |
| 약물 | (약물에 대한 정보가 제공되지 않았습니다.) |
| 예후 | |
| 예후 | (예후에 대한 정보가 제공되지 않았습니다.) |
| 빈도 | |
| 빈도 | (빈도에 대한 정보가 제공되지 않았습니다.) |
| 사망률 | |
| 사망률 | (사망률에 대한 정보가 제공되지 않았습니다.) |
| 관련 질환 | |
| 관련 질환 | 수혈 관련 이식편대숙주병 |
| 이미지 | |
 | |
2. 원인
이식편대숙주병(GVHD)은 일반적으로 두 가지 원인, 즉 골수 이식과 수혈로 인해 발생한다. 이식편대숙주병이 발생하려면 빌링햄 기준이라고 알려진 다음 세 가지 기준을 충족해야 한다.[17]
| 빌링햄 기준 |
|---|
| 1. 생존 가능하고 기능적인 면역 세포를 가진 면역능력이 있는 이식편이 투여되어야 한다. |
| 2. 수혜자는 기증자와 면역학적으로 달라야 한다. (조직적합성이 맞지 않음) |
| 3. 수혜자는 면역억제(면역저하)되어 이식된 세포를 파괴하거나 비활성화할 수 없어야 한다. 특히, 수혜자의 세포 매개 면역이 기증자로부터의 생존 가능한 림프구를 파괴하거나 비활성화할 수 없는 경우를 포함한다.[18] |
- 골수 이식: 이식편에 존재하는 T 세포가 숙주 조직을 이질적인 것으로 인식하여 공격한다. 이때 TNF-α 및 인터페론-감마(IFNγ) 등 과도한 사이토카인이 생성된다.[19] 인간 백혈구 항원(HLA)을 포함한 광범위한 숙주 항원이 관여하며,[19] HLA가 동일한 형제자매 간에도 소수 조직 적합성 항원의 차이로 인해 발생할 수 있다.[20][21] 이식 손실에 가장 큰 영향을 미치는 항원은 HLA-DR(처음 6개월), HLA-B(처음 2년), HLA-A(장기 생존) 순이다.[22] 기증자 T 세포는 이식편대숙주병을 유발하지만, 이식편 대 종양 효과도 있어 최근 연구에서는 이 둘을 분리하려는 시도가 이루어지고 있다.[23][24]
- 수혈: 수혈 후 이식편대숙주병(GVHD)의 원인은 명확하게 밝혀지지 않았지만, HLA가 공여자의 HLA형이 동형 접합이고, 수여자와 반일치하는 경우와 수여자의 면역 기능이 저하된 경우가 원인으로 고려되고 있다.
- 기타: 가슴샘 이식은 수혜자의 흉선 세포가 공여자의 가슴샘 세포를 모델로 음성 선택을 거치면서 자가면역 질환을 유발할 수 있다.[26] 흉선종 환자는 악성 흉선이 자기 반응성 T 세포를 제대로 제거하지 못해 흉선종 관련 다기관 자가면역 질환(TAMA)이 발생할 수 있다.[29]
2. 1. 면역력 약화
정상인의 경우 타인의 백혈구가 들어오면 면역체계가 작동하여 우리 몸에 있는 백혈구에 의해 잡아먹히지만, 면역력이 약해져 있을 경우 타인의 백혈구가 혈중에 살아서 돌아다니고 심지어는 체세포분열을 통해 증식하게 된다.[18]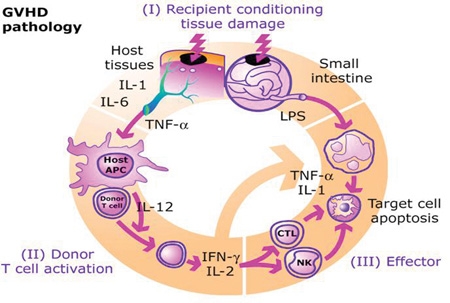
이식편대숙주병(GVHD)이 발생하려면 다음 세 가지 조건이 필요하다.
- 생존 가능하고 기능적인 면역 세포를 가진 면역능력이 있는 이식편이 투여되어야 한다.
- 수혜자는 기증자와 면역학적으로 달라야 한다. (조직적합성이 맞지 않음)
- 수혜자는 면역억제(면역저하)되어 이식된 세포를 파괴하거나 비활성화할 수 없어야 한다.
특히, 수혜자의 세포 매개 면역이 기증자로부터의 생존 가능한 림프구를 파괴하거나 비활성화할 수 없는 경우를 포함한다.[18]
수혈 후 GVHD는 수혈자의 면역 기능이 저하된 경우 발생할 수 있다. 노인이나 면역 부전 환자, 수술 시에 고빈도로 발생한다. 이전에는 수여자가 면역 부전 상태에 있는 경우에만 발병한다고 생각되었지만, 현재는 면역 정상자에게도 발병하는 것으로 알려져 있다. HLA가 유사하지 않은 공여자로부터의 수혈 시 발생하는 GVHD는 면역 기능 저하가 원인이라고 생각할 수 있다.[52][53]
2. 2. 가족 간 수혈
부모의 백혈구가 침입하면 면역체계는 침입한 백혈구가 자신의 것과 비슷하므로 이를 살려두는데, 마찬가지로 혈중에 부모의 백혈구가 살아돌아다니고, 심지어는 세포분열을 통해 증식한다. 자식의 나이가 어릴수록 면역체계가 미숙하므로 더욱 이런 일이 잘 일어난다.이 유형의 이식편대숙주병(GvHD)은 면역 기능이 저하된 수혜자에게 방사선 처리되지 않은 혈액을 수혈하는 것과 관련이 있다. 또한 혈액 공여자가 동형접합이고 수혜자가 HLA 반수체에 대해 이형접합인 경우에도 발생할 수 있다.[25]
수혈 혈액에 포함된 혈액 제공자의 림프구가 증식하여 수혈자의 전신 조직을 공격, 파괴하는 질환으로, 수혈을 동반한 수술 후에 격렬한 알레르기양 반응을 일으켜 사망하는 사례는 옛날부터 "수술 후 홍피증"이라고도 불렸다.[52][53][54][55]
현재에는 적혈구・혈소판 등 혈액의 구성 성분별 수혈이 보급되어 수혈 제제 중의 림프구는 제제 과정 중에 거의 제거되고 있지만, 그래도 소량의 림프구가 제제 중에 잔존한다. 통상적인 경우, 수혈 혈액에 포함된 림프구와 수혈자의 체조직은 서로를 이물질로 인식하고 공격하지만, 수혈 내 림프구는 소수이므로 전자가 후자에게 세력에서 이기는 일은 통상적으로 있을 수 없다. 결국, 잔존 림프구는 수혈자의 면역 반응에 의해 완전히 제거된다.
그러나 드물게 수혈 중의 잔존 림프구가 수혈자의 체내에서 제한을 받지 않고 증식하여, 결국 수혈자의 정상적인 체조직을 손상시키는 경우가 있으며, 이를 수혈 후 GVHD라고 부른다.[52][53]
원인은 아직 명확하게 확립되지 않았지만, 다음과 같은 요인들이 고려되고 있다.
- HLA가 공여자의 HLA형이 동형 접합이고, 수여자와 반일치하는 경우: HLA의 일방향 적합(one-way match)이라고 불리는 "공여자의 림프구에게 수여자는 이물질이지만, 수여자에게 공여자의 혈액을 이물질로 인식할 수 없는" 상태가 있을 수 있다는 것이 알려져 있으며, 이러한 경우 공여자의 림프구는 수여자의 체내에서 공격을 받지 않고 증식할 수 있다. 친족 간의 수혈에서 발병률이 높은 것은 HLA 적합이 중요한 역할을 한다는 것을 설명한다.[52][53][55]
- 수여자의 면역 기능이 저하된 경우: 수혈 후 GVHD는 노인이나 면역 부전 시, 수술 시에 고빈도로 발생한다. 다만 이전에는 수여자가 면역 부전 상태에 있는 경우에만 발병한다고 생각되었지만, 현재는 면역 정상자에게도 발병하는 것으로 알려져 있다. 따라서 HLA가 유사하지 않은 공여자로부터의 수혈 시 발생하는 GVHD는 이것이 원인이라고 생각할 수 있다.[52][53]
2. 3. 기타 요인
골수 이식 후, 오염 물질이나 의도적으로 숙주에 도입된 이식편에 존재하는 T 세포는 숙주 조직을 항원적으로 이질적인 것으로 인식한 후 이식 수혜자의 생물학적 조직을 공격한다. T 세포는 TNF-α 및 인터페론-감마(IFNγ)를 포함한 과도한 사이토카인을 생성한다.[19] 광범위한 숙주 항원이 이식편대숙주병을 시작할 수 있으며, 그중에는 인간 백혈구 항원(HLA)이 있다.[19] 그러나 HLA가 동일한 형제자매가 기증자인 경우에도 이식편대숙주병이 발생할 수 있다.[20] HLA가 동일한 형제자매 또는 HLA가 동일하지 않은 관련 없는 기증자는 종종 기증자의 T 세포에 의해 이물질로 간주되어 면역 반응을 일으키는 주요 조직 적합성 복합체(MHC) 분자에 의해 제시될 수 있는 유전적으로 다른 단백질(소수 조직 적합성 항원이라고 함)을 가지고 있다.[21]이식 손실에 가장 책임이 있는 항원은 HLA-DR(처음 6개월), HLA-B(처음 2년) 및 HLA-A(장기 생존)이다.[22]
기증자 T 세포는 이식편대숙주병의 효과기 세포로서는 바람직하지 않지만, 수혜자의 잔여 면역 체계가 골수 이식편을 거부하는 것을 방지하여 착상에 중요하다 (숙주 대 이식). 또한, 골수 이식은 주로 백혈병을 포함한 암을 치료하는 데 자주 사용되므로, 기증자 T 세포는 귀중한 이식편대종양 효과가 있는 것으로 입증되었다.[23] 동종 골수 이식에 대한 현재 많은 연구는 바람직하지 않은 이식편대숙주병 측면의 T 세포 생리학을 바람직한 이식편 대 종양 효과로부터 분리하려는 시도를 포함한다.[24]
가슴샘 이식은 수혜자의 흉선 세포가 자기 항원을 인식하기 위해 음성 선택을 거칠 때 공여자의 가슴샘 세포를 모델로 사용하기 때문에 특별한 유형의 이식편대숙주병(GvHD)을 유발할 수 있다. 따라서 신체의 나머지 부분에서 자신의 구조를 비자신으로 오인할 수 있다. 이는 이식편 자체의 세포가 직접적인 원인이 아니라 이식편의 세포가 수혜자의 T 세포가 공여자의 T 세포처럼 작용하게 만들기 때문에 다소 간접적인 GvHD이다. 이는 서로 다른 종 사이의 가슴샘 이종 이식 실험에서 다중 장기 자가면역으로 볼 수 있다.[26] 자가면역 질환은 인간 동종 이계 가슴샘 이식 후 흔한 합병증으로, 이식 후 1년 이상 지난 대상자의 42%에서 발견된다.[27] 그러나 이는 완전한 디조지 증후군과 같은 적응증 자체가 자가면역 질환의 위험을 증가시킨다는 사실로 부분적으로 설명된다.[28]
흉선종 관련 다기관 자가면역 질환(TAMA)이라고 불리는 이식편대숙주병 유사 질환은 흉선종 환자에게 발생할 수 있다. 이러한 환자에서 병원성 T 세포의 공급원은 기증자가 아니라, 환자 자신의 악성 흉선이 자기 지향 T 세포를 생성한다. 이는 악성 흉선이 자기 반응성 T 세포를 제거하도록 발달 중인 흉선 세포를 적절하게 교육할 수 없기 때문이다. 그 결과는 이식편대숙주병과 거의 구별할 수 없는 질환이 발생한다.[29]
수혈 후 이식편대숙주병(GVHD)의 원인은 아직 명확하게 확립되지 않았지만, 다음과 같은 요인들이 고려되고 있다.
- HLA가 공여자의 HLA형이 동형 접합이고, 수여자와 반일치하는 경우: HLA의 일방향 적합(one-way match)이라고 불리는 "공여자의 림프구에게 수여자는 이물질이지만, 수여자에게 공여자의 혈액을 이물질로 인식할 수 없는" 상태가 있을 수 있다. 이러한 경우 공여자의 림프구는 수여자의 체내에서 공격을 받지 않고 증식할 수 있다. 친족 간의 수혈에서 발병률이 높은 것은 HLA 적합이 중요한 역할을 한다는 것을 설명한다.[52][53][55]
- 수여자의 면역 기능이 저하된 경우: 수혈 후 GVHD는 노인이나 면역 부전 시, 수술 시에 고빈도로 발생한다. 다만 이전에는 수여자가 면역 부전 상태에 있는 경우에만 발병한다고 생각되었지만, 현재는 면역 정상자에게도 발병하는 것으로 알려져 있다. 따라서 HLA가 유사하지 않은 공여자로부터의 수혈 시 발생하는 GVHD는 이것이 원인이라고 생각할 수 있다.[52][53]
3. 종류
이식편대숙주병은 임상적으로 급성과 만성으로 나뉘며, 발병 시기, 영향을 받는 조직, 반응의 심각성에 따라 점수나 등급이 매겨진다.[3][4]
3. 1. 급성 이식편대숙주병 (aGVHD)
정상인의 경우 타인의 백혈구가 들어오면 면역체계가 작동하여 잡아먹지만, 면역력이 약해진 경우 타인의 백혈구가 혈중에 살아남아 체세포분열을 통해 증식하게 된다. 증식한 타인의 백혈구 중 자연 살해 세포, 세포독성 T세포 등 림프구는 숙주를 적으로 여기고 뇌, 골수, 간 등 모든 조직을 공격한다. 피부를 공격하면 피부병, 간을 공격하면 간 기능에 문제가 생기는 등 거의 모든 부위에서 증상이 나타난다.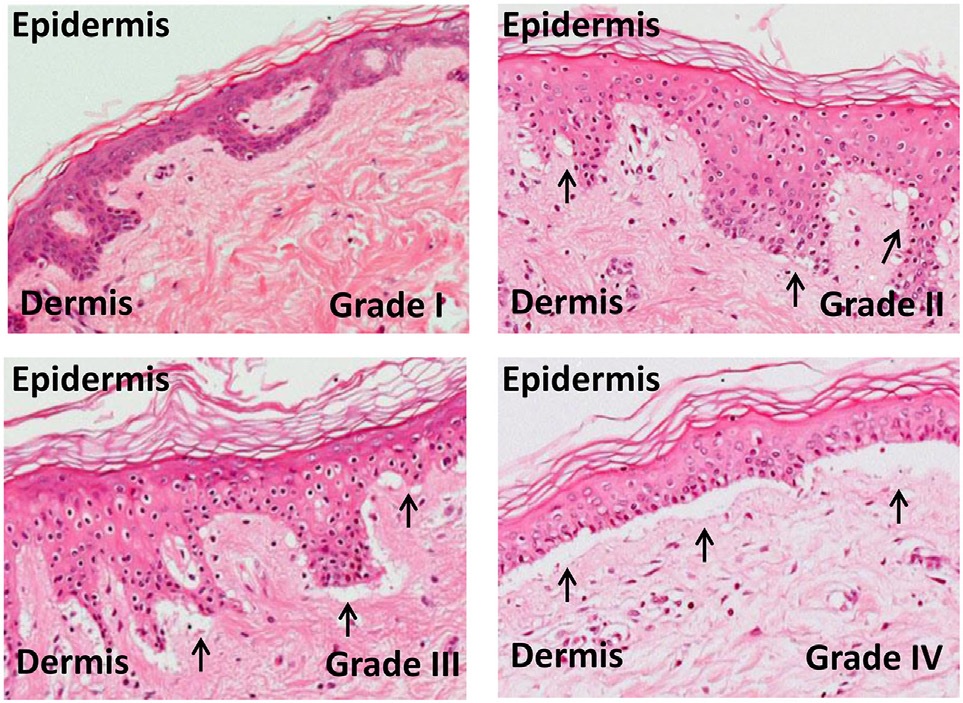
임상 환경에서 이식편대숙주병은 급성 및 만성 형태로 나뉜다.[3][4]
고전적인 의미에서 급성 이식편대숙주병은 간, 피부 (발진), 점막 및 위장관에 대한 선택적인 손상으로 특징지어진다. 최신 연구에 따르면 이식편대숙주병의 다른 표적 장기에는 면역 체계(예: 조혈 시스템, 골수 및 흉선) 자체와 면역 매개 폐렴증 형태의 폐가 포함된다.[5] 생체 지표를 사용하여 피부의 엘라핀과 같은 이식편대숙주병의 특정 원인을 식별할 수 있다.[6]
질의 점막 손상은 심한 통증과 흉터를 유발할 수 있으며 급성 이식편대숙주병에서 나타난다. 이로 인해 성교가 불가능해질 수 있다.[8]
급성 형태의 이식편대숙주병(aGvHD)은 일반적으로 이식 후 10일에서 100일 사이에 관찰되며,[9][10] 동종 조혈모세포 이식 수혜자의 약 3분의 1에서 2분의 1이 겪게 된다.[10] 급성 GvHD는 젊은 환자, 그리고 공여자와 환자 간의 인간 백혈구 항원(HLA) 일치가 더 가까운 환자에게서는 덜 흔하게 나타난다.[10]
첫 번째 징후는 보통 손바닥과 발바닥의 발진, 화끈거림, 붉어짐이며, 전신으로 퍼질 수 있다. 다른 증상으로는 메스꺼움, 구토, 위 경련, 설사(묽고 때로는 혈변), 식욕 부진, 황달, 복통, 체중 감소 등이 있다.[10]
위장관의 급성 GvHD는 심각한 장 염증, 점막 막의 탈락, 심한 설사, 복통, 메스꺼움 및 구토를 유발할 수 있으며,[11] 일반적으로 장 생검을 통해 진단된다. 간 GvHD는 급성 환자의 빌리루빈 수치로 측정된다.[12] 피부 GvHD는 때때로 레이스 모양의 확산성 홍반성 반점 구진 발진을 유발한다.[13]
급성 GvHD는 다음과 같이 단계별로 진행된다.
| 장기 | 1단계 | 2단계 | 3단계 | 4단계 |
|---|---|---|---|---|
| 피부 | 반점 구진 발진이 체표면적의 25% 미만 | 체표면적의 25~50%에 반점 구진 발진 | 전신 홍피증 | 물집 및 낙설을 동반한 전신 홍피증 |
| 간 | 빌리루빈 2~3 mg/dL | 빌리루빈 3~6 mg/dL | 빌리루빈 6~15 mg/dL | 빌리루빈 > 15 mg/dL |
| 장 | 설사 500~1000 mL/일 | 설사 1000~1500 mL/일 | 설사 1500~2000 mL/일 | 설사 > 2000 mL/일 |
전체 등급(피부-간-장)은 각 장기별로 1단계에서 4단계까지 개별적으로 평가되며, 4단계 GvHD 환자는 일반적으로 예후가 좋지 않다. GvHD가 심하고 스테로이드 및 추가 약물을 포함한 강렬한 면역 억제를 통해 통제해야 하는 경우, 환자는 면역 억제의 결과로 심각한 감염이 발생할 수 있으며[11] 감염으로 사망할 수도 있다. 그러나 2016년 연구에 따르면 4단계 GvHD 환자의 예후가 최근 몇 년 동안 개선되었다.[14]
3. 2. 만성 이식편대숙주병 (cGVHD)
만성 이식편대숙주병(cGVHD)은 일반적으로 이식 후 90일에서 600일 사이에 시작되며,[10] 중등도에서 중증의 cGVHD가 나타나는 것은 장기 생존에 부정적인 영향을 미친다.[15]
만성 이식편대숙주병은 급성 이식편대숙주병과 마찬가지로 간, 피부, 점막, 위장관 등을 공격하지만, 장기적으로는 결합 조직 및 외분비선에도 손상을 일으킬 수 있다.[7]
cGvHD의 첫 번째 증상은 흔히 손바닥이나 발바닥에 나타나는 발진이며, 이 발진은 퍼질 수 있고 보통 가렵고 건조하다. 심한 경우, 피부가 물집이 생기고 벗겨질 수 있으며, 심한 햇볕 화상과 유사하다. 열이 발생할 수도 있다. 만성 GVHD의 다른 증상은 다음과 같다:[10]
- 식욕 감소
- 설사
- 복부 경련
- 체중 감소
- 황달
- 간비대
- 복부 팽만
- 복부 오른쪽 윗부분의 통증
- 혈액 내 간 효소 수치 증가 (혈액 검사에서 확인)
- 피부가 팽팽하게 느껴짐
- 건조하고 따가운 눈
- 입안의 건조함 또는 고통스러운 궤양
- 산성 음식을 먹을 때 타는 듯한 느낌
- 세균 감염
- 폐의 작은 기도 막힘
질의 점막 손상은 심한 통증과 흉터를 유발할 수 있으며, 이로 인해 성교가 불가능해질 수 있다.[8]
구강에서는 만성 이식편대숙주병이 전형적인 구강 편평태선에 비해 구강 편평 세포 암종으로의 악성 종양 위험이 더 높은 점막 편평태선으로 나타난다.[16] 이식편대숙주병과 관련된 구강암은 비조혈 줄기 세포 이식 환자의 구강암에 비해 더 공격적인 경과를 보이며 예후가 좋지 않을 수 있다.[14]
급성 이식편대숙주병(GVHD)은 이식 후 1~2주 이내, 만성 이식편대숙주병(GVHD)은 이식 후 120일 이후에 발병하는 것으로 분류하지만, 반드시 발병 시기로 분류할 수 있는 병태는 아니다.
4. 증상
조혈모세포 이식 후 증식한 타인의 백혈구 중 자연 살해 세포, 세포독성 T세포 등 각종 림프구는 숙주를 적으로 여기고 공격하기 시작하며, 뇌, 골수, 간 등 숙주의 모든 조직을 공격한다. 피부를 공격하면 피부병을 일으키며, 간을 공격하면 간 기능에 문제가 생긴다. 증식한 면역세포가 모든 조직을 공격하므로 발열이나 피부병 등 거의 모든 부위에서 증상이 일어난다.[9][10][40]
급성 이식편대숙주병(aGvHD)의 첫 번째 징후는 보통 손바닥과 발바닥의 발진, 화끈거림, 붉어짐이며, 이는 전신으로 퍼질 수 있다. 다른 증상으로는 메스꺼움, 구토, 위 경련, 설사(묽고 때로는 혈변), 식욕 부진, 황달, 복통, 체중 감소 등이 있다.[10]
위장관의 급성 GvHD는 심각한 장 염증, 점막 막의 탈락, 심한 설사, 복통, 메스꺼움 및 구토를 유발할 수 있으며, 일반적으로 장 생검을 통해 진단된다.[11] 간 GvHD는 급성 환자의 빌리루빈 수치로 측정된다.[12] 피부 GvHD는 때때로 레이스 모양의 확산성 홍반성 반점 구진 발진을 유발한다.[13]
급성 GvHD는 다음과 같이 단계별로 진행된다.
| 단계 | 피부 | 간 (빌리루빈) | 장 (설사) |
|---|---|---|---|
| 1 | 반점구진 발진이 체표면적의 25% 미만 | 2mg/dL - 3mg/dL | 500ml - 1000ml |
| 2 | 반점구진 발진이 체표면적의 25-50% | 3mg/dL - 6mg/dL | 1000ml - 1500ml |
| 3 | 반점구진 발진이 체표면적의 50% 이상 | 6mg/dL - 15mg/dL | 1500ml - 2000ml |
| 4 | 전신 홍반 및 수포 형성 | 15mg/dL 초과 | 2000ml 초과, 심한 복통 |
전체 등급(피부-간-장)은 각 장기별로 1단계에서 4단계까지 개별적으로 평가되며, 4단계 GvHD 환자는 일반적으로 예후가 좋지 않다. GvHD가 심하고 스테로이드 및 추가 약물을 포함한 강렬한 면역 억제를 통해 통제해야 하는 경우, 환자는 면역 억제의 결과로 심각한 감염이 발생할 수 있으며[11] 감염으로 사망할 수도 있다. 그러나 2016년 연구에 따르면 4단계 GvHD 환자의 예후가 최근 몇 년 동안 개선되었다.[14]
만성 이식편대숙주병(cGvHD)의 첫 번째 증상은 흔히 손바닥이나 발바닥에 나타나는 발진이며, 이 발진은 퍼질 수 있고 보통 가렵고 건조하다. 심한 경우, 피부가 물집이 생기고 벗겨질 수 있으며, 심한 햇볕 화상과 유사하다. 열이 발생할 수도 있다.
만성 GVHD의 다른 증상은 다음과 같다:[10]
- 식욕 감소
- 설사
- 복부 경련
- 체중 감소
- 피부와 눈의 황달
- 간 비대
- 복부 팽만
- 복부 오른쪽 윗부분의 통증
- 혈액 내 간 효소 수치 증가(혈액 검사에서 확인)
- 피부가 팽팽하게 느껴짐
- 건조하고 따가운 눈
- 입안의 건조함 또는 고통스러운 궤양
- 산성 음식을 먹을 때 타는 듯한 느낌
- 세균 감염
- 폐의 작은 기도 막힘
구강에서는 만성 이식편대숙주병이 전형적인 구강 편평태선에 비해 구강 편평 세포 암종으로의 악성 변화 위험이 더 높은 점막 편평태선으로 나타난다.[16] 이식편대숙주병과 관련된 구강암은 비조혈 줄기 세포 이식 환자의 구강암에 비해 더 공격적인 경과를 보이며 예후가 좋지 않을 수 있다.[14]
수혈 후 약 1~2주 후에 발열과 홍반이 나타나고, 이내 홍반은 전신으로 퍼진다. 또한 다음 증상이 나타난다.
이러한 증상은 격렬하고 치료가 어려우며, 대부분의 경우 골수 무형성을 일으켜 곧 사망에 이르게 된다.
5. 검사
수혈 후 발열 등 여러 이상 증세가 나타나고, 간 수치가 증가되어 있으며 전반적으로 혈액세포 수가 감소되어 있다면 이식편대숙주병을 의심할 수 있다.
6. 치료
이식편대숙주병(GVHD) 치료에는 주로 면역억제제와 스테로이드가 사용된다. 프레드니손과 같은 글루코코르티코이드는 급성 및 만성 이식편대숙주병의 표준 치료법으로 정맥 내 투여된다.[41] 그러나 고용량 스테로이드는 감염 및 암 재발 위험을 높일 수 있어 용량 조절이 필요하다.
사이클로스포린과 타크로리무스는 칼시뉴린 억제제로, T 세포 활성화를 억제한다. 이 외에도 시롤리무스, 펜토스타틴, 에타너셉트, 알렘투주맙 등이 치료제로 연구되었다.[44]
최근 미국 식품의약국(US FDA)은 이브루티닙과 악사티리맙을 특정 조건의 만성 이식편대숙주병 치료제로 승인했다.[45][46] 만성 이식편대숙주병의 경우, 광생물조절요법이나 전기 자극과 같은 비약물 치료법도 활용될 수 있다.[47]
수혈 후 이식편대숙주병은 매우 치명적이며 치료가 어렵다. 사이클로스포린 A나 골수 이식을 통해 생존한 극소수 사례가 보고되었다.[52]
6. 1. 면역억제제
면역억제제와 스테로이드를 복용하여 이식편대숙주병을 치료한다. 스테로이드로 조절되지 않는 중증 숙주반응의 경우 경구 항암제로 조절한다.글루코코르티코이드의 일종인 프레드니손은 정맥 내 투여를 통해 급성 및 만성 이식편대숙주병의 표준 치료법으로 사용된다.[41] 글루코코르티코이드는 T 세포 매개 면역 공격을 억제하여 숙주 조직을 보호하지만, 고용량 투여 시 감염 및 암 재발 위험을 증가시킨다. 따라서 이식 후에는 고용량 스테로이드 투여량을 점차 줄이는 것이 바람직하며, 이 과정에서 경미한 이식편대숙주병이 나타나는 것은 이식편대종양 효과와 관련되어 긍정적인 신호로 간주될 수 있다. 그러나 글루코코르티코이드는 급성 이식편대숙주병 환자의 약 50%에게만 효과가 있으며, 나머지 환자들은 스테로이드 불응성 이식편대숙주병(SR-GVHD)을 겪게 된다.[42] SR-GVHD 치료를 위해 체외 광선요법(ECP), 중간엽 줄기 세포(MSC), 분변 미생물 이식(FMT), 룩소리티닙 등의 다양한 치료 옵션이 연구되고 있다.[42]
사이클로스포린과 타크로리무스는 칼시뉴린 억제제에 속한다. 사이클로스포린은 사이클로필린에 결합하고, 타크로리무스는 FKBP12에 결합하여 칼시뉴린을 억제한다. 칼시뉴린 억제는 활성화된 T 세포 전사 인자 NFAT의 탈인산화를 차단하고 핵으로의 이동을 막는다.[43] 표준 예방 요법으로는 메토트렉세이트와 함께 6개월간 사이클로스포린을 사용하는 것이 포함되며, 사이클로스포린 혈중 농도는 200ng/ml 이상으로 유지해야 한다.[44]
이 외에도 시롤리무스, 펜토스타틴, 에타너셉트, 알렘투주맙 등이 GvHD 치료를 위해 연구되었다.[44]
2017년 8월, 미국 식품의약국(US FDA)은 하나 이상의 전신 치료에 실패한 만성 GvHD 환자에게 이브루티닙 사용을 승인했다.[45] 2024년 8월에는 악사티리맙이 미국에서 의학적 사용 승인을 받았다.[46]
급성기에는 면역 억제제나 스테로이드가 효과적이지만, 만성기의 예방법은 아직 확립되지 않았다. BTK 억제제, 면역억제제, 스테로이드의 지속적 투여, 증량, 펄스 투여 등이 시도되고 있지만, 이러한 약물들이 면역 기능의 적합성을 개선하는지는 불분명하다. 급성기에 이러한 치료를 통해 치명률을 개선할 수 있지만, 조절이 어렵거나 부작용으로 인한 합병증으로 생명이 위협받는 경우도 적지 않다.
만성기에도 면역억제제나 스테로이드 등을 투여하여 증상 개선을 시도하지만, 많은 경우 증상이 지속되거나 악화되며, 약물이나 시간 경과에 따른 면역 기능 적합성 개선 여부는 불분명하다. 일반적으로 장기 생존자들의 QOL은 낮은 경향을 보인다.
6. 2. 기타 치료
면역억제제와 스테로이드를 복용하여 치료한다. 스테로이드로 조절되지 않는 중증 숙주반응의 경우 경구 항암제로 조절한다. 정맥 내 투여되는 글루코코르티코이드(프레드니손 등)는 급성 및 만성 이식편대숙주병의 표준 치료법이다.[41] 이러한 글루코코르티코이드의 사용은 T 세포 매개 면역 공격을 억제하지만, 고용량에서는 감염 및 암 재발 위험을 높인다. 따라서 이식 후 스테로이드 투여량을 줄이는 것이 바람직하며, 경미한 이식편대숙주병은 이식편대종양 효과와 관련이 있어 HLA 불일치 환자에게는 유익할 수 있다. 글루코코르티코이드는 급성 이식편대숙주병의 1차 치료제이지만, 환자의 약 50%만이 반응하며, 나머지는 스테로이드-불응성 이식편대숙주병(SR-GVHD)을 겪는다.[42] SR-GVHD 치료 옵션으로는 체외 광선요법(ECP), 중간엽 줄기 세포(MSC), 분변 미생물 이식(FMT), 룩소리티닙 등이 연구되고 있다.[42]만성 이식편대숙주병 환자의 경우 비약물 치료법이 중요하며, 가능하면 우선적으로 고려된다. 예를 들어, 광생물조절요법은 이식편대숙주병 관련 구강 점막 궤양에, 전기 자극은 구강 건조증에 사용된다.[47]
BTK 억제제, 면역억제제, 스테로이드의 지속적 투여, 증량, 펄스 투여가 시도된다. 이러한 약물은 일시적으로 면역 기능을 억제하여 염증을 억제하지만, 면역 기능 개선 여부는 불분명하다. 급성기에는 치명률을 개선할 수 있지만, 조절되지 않거나 부작용으로 인한 합병증으로 생명이 위협받는 경우도 있다.
만성기에도 면역억제제나 스테로이드 투여가 시도되어 증상 개선이 나타나기도 한다. 그러나 많은 경우 증상이 지속되거나 악화되며, 면역 기능 개선 여부는 불분명하다. 일반적으로 장기 생존자의 QOL은 낮다.
수혈 후 이식편대숙주병(GVHD)은 발병 시 치사율이 매우 높으며, 거의 모든 사례가 사망한다. 혈장 교환은 효과가 없고 치료가 어렵다. 사이클로스포린 A나 골수 이식을 통해 생존한 극소수 사례가 보고되었다.[52] 단백질 분해 효소 억제제가 효과적이었다는 증례 보고도 있다.[55]
7. 예방
타인의 피를 수혈해야 하며, 가족의 피를 수혈할 때는 방사선 처리를 통해 헌혈한 혈액 내의 백혈구를 모두 죽여야 한다. DNA 기반 조직형 검사를 통해 공여자와 이식 환자 간의 보다 정확한 HLA 일치가 가능하며, 이는 이식편대숙주병(GvHD) 발생률과 심각성을 줄이고 장기 생존율을 높이는 것으로 입증되었다.[33] 제대혈 T세포는 본질적인 면역학적 미성숙을 가지고 있으며,[34] 비관련 공여자 이식 시 제대혈 줄기세포를 사용하면 GvHD의 발생률과 심각성이 감소한다.[35]
메토트렉세이트, 사이클로스포린, 타크로리무스는 GvHD 예방에 사용되는 일반적인 약물이다.[36] 간엽 줄기 세포가 예방에 사용될 수 있는지 평가하기 위한 추가 연구가 필요하다.[37] T세포 제거 골수 이식을 수행하면 이식편대숙주병을 상당 부분 피할 수 있지만, 이식편대종양 효과 감소, 이식 실패 위험 증가, 암 재발,[38] 및 일반적인 면역 결핍과 같은 위험이 따른다. 이로 인해 환자는 바이러스, 세균, 곰팡이 감염에 더 취약해진다. 다기관 연구에서 3년 무병 생존율은 T세포 제거 이식과 T세포 완전 이식 간에 차이가 없었다.[39]
수혈 제제에 방사선 조사를 하는 것은 림프구를 비활성화하는 매우 효과적인 방법이다. 수혈용 제제는 림프구 제거를 실시해도 완전히 제거하는 것은 어려우므로 채혈 후 2주 이내의 비조사 혈액 제제에서는 수혈 후 이식편대숙주병(GVHD)이 발생할 수 있다. 수혈 제제 중 분열 능력을 가진 림프구는 시간이 지남에 따라 감소하므로 일반적으로 신선한 혈액일수록 위험이 높다고 여겨진다. 혈액 제제에 방사선 조사를 할 수 없는 경우에는 신선한 혈액을 피한다.[52][53][55]
그 외에도 다음과 같은 예방법이 있다.
- 자가 수혈을 실시한다.
- 근친자 간의 수혈을 피한다.
- 수혈을 하지 않는다. (자세한 내용은 무수혈 수술 참조)
7. 1. HLA 일치
조직적합성이 맞지 않은 수혜자는 기증자와 면역학적으로 다르다. 인간 백혈구 항원(HLA)은 이식편대숙주병을 시작할 수 있는 항원 중 하나이다.[19] HLA가 동일한 형제자매가 기증자인 경우에도 이식편대숙주병이 발생할 수 있다.[20] HLA가 동일한 형제자매 또는 HLA가 동일하지 않은 관련 없는 기증자는 종종 기증자의 T 세포에 의해 이물질로 간주되어 면역 반응을 일으키는 주요 조직 적합성 복합체(MHC) 분자에 의해 제시될 수 있는 유전적으로 다른 단백질(소수 조직 적합성 항원)을 가지고 있다.[21]이식 손실에 가장 책임이 있는 항원은 HLA-DR(처음 6개월), HLA-B(처음 2년), HLA-A(장기 생존)이다.[22]
DNA 기반 조직형 검사를 통해 공여자와 이식 환자 간의 보다 정확한 HLA 일치가 가능하며, 이는 이식편대숙주병(GvHD) 발생률과 심각성을 줄이고 장기 생존율을 높이는 것으로 입증되었다.[33]
7. 2. T 세포 제거
골수 이식 후, 이식편에 존재하는 T 세포는 숙주 조직을 항원적으로 이질적인 것으로 인식하여 이식 수혜자의 생물학적 조직을 공격한다. 이때 T 세포는 TNF-α 및 인터페론-감마(IFNγ)를 포함한 과도한 사이토카인을 생성한다.[19] 기증자 T 세포는 이식편대숙주병의 효과기 세포로서는 바람직하지 않지만, 수혜자의 잔여 면역 체계가 골수 이식편을 거부하는 것을 방지하여 착상에 중요하다 (숙주 대 이식).[23]T세포 제거 골수 이식을 수행하면 이식편대숙주병(GVHD)을 상당 부분 피할 수 있다. 그러나 이러한 유형의 이식은 이식편대종양 효과 감소, 이식 실패 위험 증가, 암 재발,[38] 및 일반적인 면역 결핍을 초래하여 환자가 바이러스, 세균, 곰팡이 감염에 더 취약해진다. 다기관 연구에서 3년 무병 생존율은 T세포 제거 이식과 T세포 완전 이식 간에 차이가 없는 것으로 나타났다.[39]
7. 3. 면역억제제 예방 요법
메토트렉세이트, 사이클로스포린, 타크로리무스는 이식편대숙주병(GvHD) 예방에 사용되는 일반적인 약물이다.[36] 간엽 줄기 세포가 예방에 사용될 수 있는지 평가하기 위한 추가 연구가 필요하다.[37]사이클로스포린과 타크로리무스는 칼시뉴린 억제제이다. 이 물질들은 구조적으로는 다르지만 작용 기전은 같다. 사이클로스포린은 세포질 단백질인 펩티딜-프롤릴 시스-트랜스 이성질체화 효소 A(사이클로필린으로 알려짐)에 결합하는 반면, 타크로리무스는 세포질 단백질인 펩티딜-프롤릴 시스-트랜스 이성질체화 효소 FKBP12에 결합한다. 이러한 복합체는 칼시뉴린을 억제하여 활성화된 T세포의 전사 인자 NFAT의 탈인산화를 차단하고 핵으로의 이동을 막는다.[43] 표준 예방요법에는 메토트렉세이트와 함께 6개월 동안 사이클로스포린을 사용하는 것이 포함된다. 사이클로스포린 수치는 200ng/ml 이상으로 유지해야 한다.[44]
7. 4. 수혈 시 주의사항
가족에게서 피를 수혈받을 때는 방사선 처리를 통해 헌혈된 혈액 내의 백혈구를 모두 죽여야 한다. DNA 기반 조직형 검사를 통해 공여자와 이식 환자 간의 보다 정확한 HLA 일치를 할 수 있으며, 이는 이식편대숙주병 발생률과 심각성을 줄이고 장기 생존율을 높이는 것으로 입증되었다.[33] 특히, 자식의 나이가 어릴수록 면역체계가 미숙하므로 더욱 이런 일이 잘 일어난다.수혈 제제에 방사선 조사를 하는 것은 림프구를 비활성화하는 매우 효과적인 방법이다. 수혈용 제제는 림프구 제거를 실시해도 완전히 제거하는 것은 어려우므로, 채혈 후 2주 이내의 비조사 혈액 제제에서는 수혈 후 이식편대숙주병이 발생할 수 있다. 수혈 제제 중 분열 능력을 가진 림프구는 시간이 지남에 따라 감소하므로, 일반적으로 신선한 혈액일수록 위험이 높다고 여겨진다. 혈액 제제에 방사선 조사를 할 수 없는 경우에는 신선한 혈액을 피해야 한다.[52][53][55]
따라서, 되도록 타인의 피를 수혈해야 하며, 다음 방법들이 권장된다.
- 자가 수혈을 실시한다.
- 근친자 간의 수혈을 피한다.
- 수혈을 하지 않는다. (자세한 내용은 무수혈 수술 참조)
8. 수혈 후 이식편대숙주병
수혈 후 이식편대숙주병(GVHD)은 수혈된 혈액 속 림프구가 수혈자의 몸을 공격하여 발생하는 질환이다. 1980년대에서 1990년대에 걸쳐 원인이 밝혀지기 전에는 "수술 후 홍피증"이라고도 불렸다.[52][53][54][55]
현대 의학에서는 적혈구와 혈소판 등 혈액 성분별 수혈이 보편화되면서 림프구가 대부분 제거되지만, 여전히 소량의 림프구가 남아있을 수 있다. 일반적으로는 이러한 잔존 림프구가 수혈자의 면역 반응에 의해 제거되지만, 드물게 림프구가 증식하여 수혈자의 체조직을 손상시키는 경우가 있는데, 이를 수혈 후 GVHD라고 한다.[52][53]
면역 기능이 저하된 환자에게 방사선 처리되지 않은 혈액을 수혈하거나, 혈액 공여자가 동형접합이고 수혜자가 HLA 반수체에 대해 이형접합인 경우 발생할 수 있다. 골수 림프 조직 침범으로 인해 사망률이 80~90%로 높다.[25] 현대 의학에서는 혈액 제제를 방사선 처리하여 백혈구를 비활성화함으로써 수혈 관련 GVHD를 거의 완전히 예방할 수 있다.[25]
8. 1. 원인
이식편대숙주병(GvHD)의 원인은 크게 두 가지로 나눌 수 있다.첫째, 면역력이 약해진 경우이다. 정상인의 경우 타인의 백혈구가 들어오면 면역체계가 작동하여 이를 제거하지만, 면역력이 약해진 경우에는 타인의 백혈구가 혈액 내에서 살아남아 체세포분열을 통해 증식할 수 있다.
둘째, 부모의 백혈구가 침입하는 경우이다. 부모의 백혈구는 면역체계가 자신의 것과 비슷하다고 판단하여 제거하지 않고, 혈액 내에서 살아남아 세포분열을 통해 증식한다. 특히 자식의 나이가 어릴수록 면역체계가 미숙하여 이러한 현상이 더 잘 일어난다.[25]
이러한 유형의 GvHD는 면역 기능이 저하된 환자에게 방사선 처리되지 않은 혈액을 수혈하는 경우 발생할 수 있다. 또한 혈액 공여자가 동형접합이고 수혜자가 HLA 반수체에 대해 이형접합인 경우에도 발생할 수 있다. 골수 림프 조직의 침범으로 인해 사망률이 높지만(80–90%), 임상 증상은 골수 이식으로 인한 GvHD와 유사하다. 현대 의학에서는 혈액 제제를 조절된 방사선 처리를 통해 백혈구(림프구 포함)를 비활성화하여 수혈 관련 GvHD를 거의 완전히 예방할 수 있다.[25]
이식에 의해 혈액 제공자의 면역 기구가 수혈자의 전신 조직을 공격, 파괴하는 질환으로, 원인은 확립되지 않았지만 급성기에는 혈액 제공자의 림프구(킬러 T 세포)가 주된 원인으로 추정된다. 만성기에는 더 많은 면역 기능의 작용이 관여하고 있다고 추정된다.
수혈 혈액에 포함된 혈액 제공자의 림프구가 증식하여 수혈자의 전신 조직을 공격, 파괴한다. 과거에는 "수술 후 홍피증"이라고도 불렸으나, 1980년대부터 1990년대에 걸쳐 원인이 거의 해명되었다.[52][53][54][55]
적혈구・혈소판 등 혈액의 구성 성분별 수혈이 보급되면서 수혈 제제 중의 림프구는 제제 과정 중에 거의 제거되지만, 소량의 림프구가 제제 중에 잔존한다. 일반적으로 수혈 혈액에 포함된 림프구와 수혈자의 체조직은 서로를 이물질로 인식하고 공격하지만, 수혈 내 림프구는 소수이므로 제거된다.
그러나 드물게 수혈 중의 잔존 림프구가 수혈자의 체내에서 증식하여 정상적인 체조직을 손상시키는 경우가 있는데, 이를 수혈 후 GVHD라고 부른다.[52][53]
원인은 아직 명확하게 확립되지 않았지만, 다음과 같은 요인들이 고려되고 있다.
- HLA가 공여자의 HLA형이 동형 접합이고, 수여자와 반일치하는 경우: "공여자의 림프구에게 수여자는 이물질이지만, 수여자에게 공여자의 혈액을 이물질로 인식할 수 없는" 상태(HLA의 일방향 적합(one-way match))에서는 공여자의 림프구가 수여자의 체내에서 공격받지 않고 증식할 수 있다. 친족 간의 수혈에서 발병률이 높은 것은 HLA 적합이 중요한 역할을 한다는 것을 보여준다.[52][53][55]
- 수여자의 면역 기능이 저하된 경우: 수혈 후 GVHD는 노인이나 면역 부전 시, 수술 시에 고빈도로 발생한다. 면역 정상자에게도 발병하는 것으로 알려져 있으며, HLA가 유사하지 않은 공여자로부터의 수혈 시 발생하는 GVHD는 이것이 원인이라고 생각할 수 있다.[52][53]
8. 2. 증상
타인의 백혈구 중에서도 자연 살해 세포, 세포독성 T세포 등 각종 림프구가 숙주를 적으로 여기고 공격하기 시작하며, 뇌, 골수, 간 등 숙주의 모든 조직을 공격한다. 피부를 공격하면 피부병을 일으키며, 간을 공격하면 간 기능에 문제가 생긴다. 증식한 면역세포가 모든 조직을 공격하므로 발열이나 피부병 등 거의 모든 부위에서 증상이 일어난다.[25]이식 후 1~2주 이내에 발병하는 급성 이식편대숙주병(GVHD)과 이식 후 120일 이후에 발병하는 만성 이식편대숙주병(GVHD)으로 분류하지만, 반드시 발병 시기로 분류할 수 있는 병태는 아니다. 수혈 후 약 1~2주 후에 발열과 홍반이 나타나고, 이내 홍반은 전신으로 퍼진다. 또한 다음 증상이 나타난다.
이러한 증상은 격렬하고 치료가 어려우며, 대부분의 경우 골수 무형성을 일으켜 곧 사망에 이르게 된다. 많은 증상이 있지만, 급성 GVHD의 표적은 피부, 소화관, 간이며, 만성 GVHD의 표적은 다발성 장기에 미친다.
8. 3. 예방
타인의 피를 수혈해야 하며, 가족의 피를 수혈할 때는 방사선 처리를 통해 헌혈한 혈액 내의 백혈구를 모두 죽여야 한다. 이식편대숙주병(GvHD)은 면역 기능이 저하된 수혜자에게 방사선 처리되지 않은 혈액을 수혈하는 것과 관련이 있다. 또한 혈액 공여자가 동형접합이고 수혜자가 HLA 반수체에 대해 이형접합인 경우에도 발생할 수 있다.[25]급성기에는 면역 억제제나 스테로이드가 유효하지만, 만성기의 예방법은 확립되어 있지 않다.
- 수혈 제제에 대한 방사선 조사 (Gamma irradiation|감마선 멸균영어)
- 림프구를 비활성화하는 방법으로 매우 효과적이다. 수혈용 제제는 림프구 제거를 실시해도 완전히 제거하는 것은 어려우므로 채혈 후 2주 이내의 비조사 혈액 제제에서는 수혈 후 GVHD가 발생할 수 있다.
- 자가 수혈을 실시한다.
- 근친자 간의 수혈을 피한다.
- 수혈을 하지 않는다. (자세한 내용은 무수혈 수술 참조)
수혈 제제 중 분열 능력을 가진 림프구는 시간이 지남에 따라 감소하므로 일반적으로 신선한 혈액일수록 위험이 높다고 여겨진다. 혈액 제제에 방사선 조사를 할 수 없는 경우에는 신선한 혈액을 피한다.[52][53][55]
8. 4. 치료
이식편대숙주병(GVHD)의 치료법은 면역억제제와 스테로이드를 복용하는 것이다. 스테로이드로 잡히지 않는 중증 숙주반응의 경우 경구 항암제로 숙주반응을 조절한다.[25]BTK 억제제, 면역억제제나 스테로이드의 지속적인 투여 및 증량, 펄스 투여가 시도되고 있다. 이러한 약물로 면역 기능을 일시적으로 억제하여 염증을 억제하지만, 면역 기능의 적합성이 개선되는지는 불분명하다. 급성기에는 치명률을 개선할 수 있지만, 조절할 수 없는 경우나, 이러한 약물의 부작용으로 합병증에 이르러 생명이 위협받는 경우도 적지 않다.
만성기에서도 면역억제제나 스테로이드 등의 투여가 시도되어 증상의 일부 개선이 보인다. 그러나 많은 사례에서 지속되거나 악화되는 것이 관찰되어, 면역 기능의 적합성이 약물이나 시간 경과에 따라 개선되는지는 불분명하다. 일반적으로 장기 생존자의 QOL은 낮은 경향이 있다.
수혈 후 이식편대숙주병(GVHD)은 일단 발병하면 치사율이 매우 높은 것으로 알려져 있으며, 거의 모든 사례가 사망한다. 증식한 림프구가 조직 내로 침투하기 때문에 혈장 교환도 효과가 없으며, 치료가 매우 어렵다. 사이클로스포린 A나 골수 이식을 통해 생명을 구한 극소수의 사례가 보고되었을 뿐이다.[52] 단백질 분해 효소 억제제가 수혈 후 GVHD에 효과적이었다는 증례 보고도 있다.[55]
참조
[1]
간행물
Transfusion associated graft versus host disease and its prevention
https://heart.bmj.co[...]
1998-09-01
[2]
간행물
Pathophysiology of GvHD and Other HSCT-Related Major Complications
[3]
간행물
Comparison of the classic Glucksberg criteria and the IBMTR Severity Index for grading acute graft-versus-host disease following HLA-identical sibling stem cell transplantation. International Bone Marrow Transplant Registry
1999-08
[4]
간행물
National Institutes of Health consensus development project on criteria for clinical trials in chronic graft-versus-host disease: I. Diagnosis and staging working group report
http://www.bbmt.org/[...]
2005-12
[5]
간행물
"[Graft-versus-host disease, a rare complication of lung transplantation]"
2016-02
[6]
간행물
Elafin is a biomarker of graft-versus-host disease of the skin
2010-01
[7]
간행물
Immune processes and pathogenic fibrosis in ocular chronic graft-versus-host disease and clinical manifestations after allogeneic hematopoietic stem cell transplantation
2010-11
[8]
간행물
Graft-versus-host disease of the vulva and/or vagina: diagnosis and treatment
2003-12
[9]
간행물
Acute and chronic Graft-versus-host disease after hematopoietic stem cell transplantation
2016-10
[10]
웹사이트
Stem Cell or Bone Marrow Transplant Side Effects
https://www.cancer.o[...]
2020-09-01
[11]
웹사이트
Graft-versus-host disease
https://medlineplus.[...]
National Library of Medicine
2019-05-06
[12]
간행물
Kinetics of bilirubin and liver enzymes is useful for predicting of liver graft-versus-host disease
http://www.elis.sk/d[...]
[13]
간행물
Cutaneous graft versus host disease in pediatric multivisceral transplantation
[14]
간행물
Improved Treatment-Related Mortality and Overall Survival of Patients with Grade IV Acute GVHD in the Modern Years
2016-05
[15]
간행물
Chronic graft-versus-host disease
2003-04
[16]
간행물
"[Gingival squamous cell carcinoma diagnosed on the occasion of osteonecrosis of the jaw in a patient with chronic GVHD]"
2019
[17]
간행물
The biology of graft-versus-host reactions
[18]
간행물
Mechanism of transfusion-associated graft-versus-host disease.
https://pubmed.ncbi.[...]
[19]
간행물
Effect of HLA mismatch on acute graft-versus-host disease
2013-09
[20]
간행물
Acute GVHD prophylaxis plus ATLG after myeloablative allogeneic haemopoietic peripheral blood stem-cell transplantation from HLA-identical siblings in patients with acute myeloid leukaemia in remission: final results of quality of life and long-term outcome analysis of a phase 3 randomised study
2019-02
[21]
간행물
Immunological considerations for embryonic and induced pluripotent stem cell banking
2011-08
[22]
간행물
Banking on iPSC--is it doable and is it worthwhile
2015-02
[23]
간행물
Graft versus tumor effects and why people relapse
2017-12
[24]
간행물
Differential effects of donor T-cell cytokines on outcome with continuous bortezomib administration after allogeneic bone marrow transplantation
2008-08
[25]
간행물
Principles of blood irradiation, dose validation, and quality control
https://zenodo.org/r[...]
1997-10
[26]
간행물
Transplantation tolerance and autoimmunity after xenogeneic thymus transplantation
2001-02
[27]
서적
Thymus Gland Pathology: Clinical, Diagnostic, and Therapeutic Features
[28]
간행물
Review of 54 patients with complete DiGeorge anomaly enrolled in protocols for thymus transplantation: outcome of 44 consecutive transplants
2007-05
[29]
간행물
Thymoma-associated multiorgan autoimmunity: a graft-versus-host-like disease
2007-10
[30]
간행물
Versus Host Disease: A Comprehensive Review
http://ar.iiarjourna[...]
2017-04
[31]
간행물
Regulatory T-cell immunotherapy for tolerance to self antigens and alloantigens in humans
2007-08
[32]
간행물
Cellular and molecular mechanisms in graft-versus-host disease
2016-02
[33]
간행물
The clinical significance of human leukocyte antigen (HLA) allele compatibility in patients receiving a marrow transplant from serologically HLA-A, HLA-B, and HLA-DR matched unrelated donors
2002-06
[34]
간행물
Unrelated donor hematopoietic cell transplantation: marrow or umbilical cord blood?
2003-06
[35]
간행물
Hematopoietic engraftment and survival in adult recipients of umbilical-cord blood from unrelated donors
2001-06
[36]
논문
A prospective randomized trial comparing cyclosporine/methotrexate and tacrolimus/sirolimus as graft-versus-host disease prophylaxis after allogeneic hematopoietic stem cell transplantation
2016-11
[37]
논문
Mesenchymal stromal cells as treatment or prophylaxis for acute or chronic graft-versus-host disease in haematopoietic stem cell transplant (HSCT) recipients with a haematological condition
2019-01
[38]
논문
Control of graft-versus-host disease and graft rejection by T cell depletion of donor and recipient with Campath-1 antibodies. Results of matched sibling transplants for malignant diseases
1994-05
[39]
논문
Effect of graft-versus-host disease prophylaxis on 3-year disease-free survival in recipients of unrelated donor bone marrow (T-cell Depletion Trial): a multi-centre, randomised phase II-III trial
[40]
논문
Acute graft-vs-host disease: pathobiology and management
2001-03
[41]
논문
Intraoral psoralen ultraviolet A irradiation (PUVA) treatment of refractory oral chronic graft-versus-host disease following allogeneic stem cell transplantation
2001-10
[42]
논문
Recent advances in graft-versus-host disease
2023-03-06
[43]
논문
Calcineurin is a common target of cyclophilin-cyclosporin A and FKBP-FK506 complexes
1991-08
[44]
웹사이트
Graft Versus Host Disease Treatment & Management: Medical Care
http://emedicine.med[...]
Medscape
2017-08-30
[45]
논문
FDA expands ibrutinib indications to chronic GVHD
https://www.fda.gov/[...]
2019-02-09
[46]
웹사이트
FDA approves axatilimab-csfr for chronic graft-versus-host disease
https://www.fda.gov/[...]
2024-08-14
[47]
논문
MASCC/ISOO Clinical Practice Statement: Management of oral manifestations of chronic graft-versus-host-disease.
2024-08
[48]
웹사이트
Search of: Graft-versus-host disease - List Results - ClinicalTrials.gov
https://clinicaltria[...]
[49]
웹사이트
World's First Stem-Cell Drug Approval Achieved in Canada
http://www.natlawrev[...]
Drinker Biddle & Reath LLP
2012-06-12
[50]
웹사이트
Increased Survival Using MSB Cells In Children With aGVHD
http://www.asx.com.a[...]
[51]
웹사이트
Immune war with donor cells after transplant may wipe out HIV
https://www.newscien[...]
NewScientist
2017-05-03
[52]
서적
三輪血液病学
文光堂
2006
[53]
서적
輸血学
中外医学社
2004
[54]
서적
内科学書
中山書店
2009
[55]
웹사이트
輸血後移植片対宿主病 2000年10月4日改訂
http://www.med.osaka[...]
大阪大学大学院医学系研究科・医学部HP寄稿記事
2000-10-04
본 사이트는 AI가 위키백과와 뉴스 기사,정부 간행물,학술 논문등을 바탕으로 정보를 가공하여 제공하는 백과사전형 서비스입니다.
모든 문서는 AI에 의해 자동 생성되며, CC BY-SA 4.0 라이선스에 따라 이용할 수 있습니다.
하지만, 위키백과나 뉴스 기사 자체에 오류, 부정확한 정보, 또는 가짜 뉴스가 포함될 수 있으며, AI는 이러한 내용을 완벽하게 걸러내지 못할 수 있습니다.
따라서 제공되는 정보에 일부 오류나 편향이 있을 수 있으므로, 중요한 정보는 반드시 다른 출처를 통해 교차 검증하시기 바랍니다.
문의하기 : help@durumis.com