비메발론산 경로
"오늘의AI위키"의 AI를 통해 더욱 풍부하고 폭넓은 지식 경험을 누리세요.
1. 개요
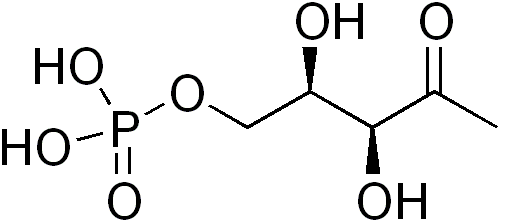
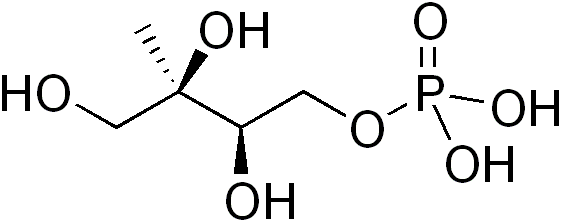
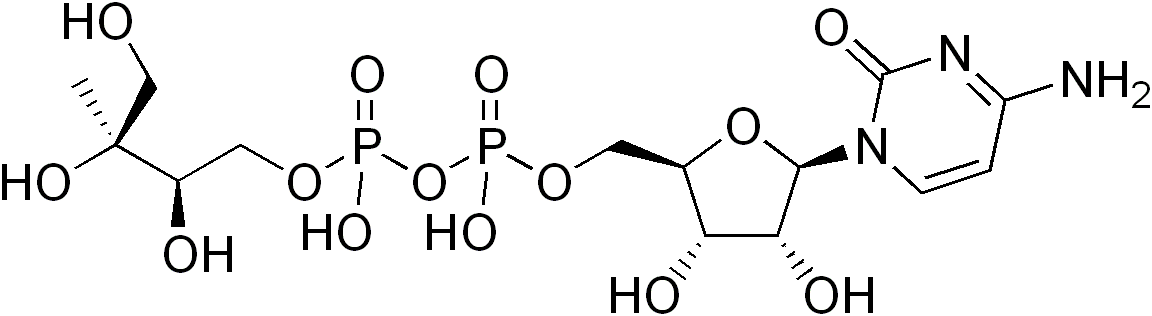
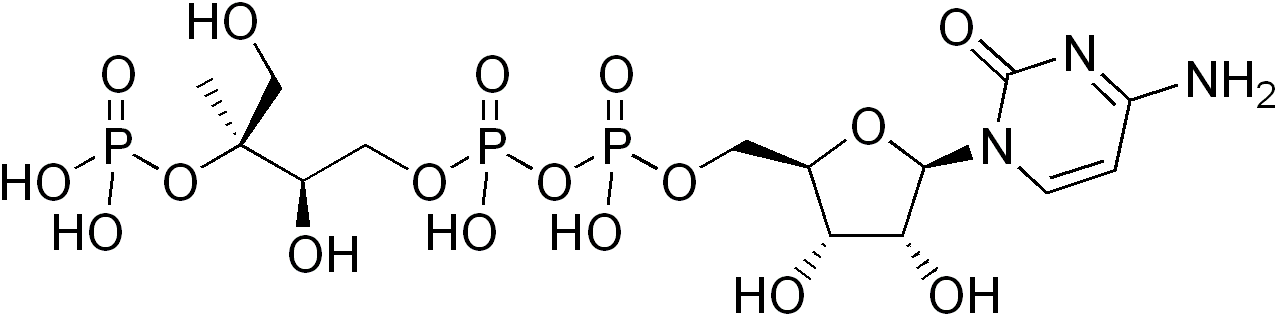
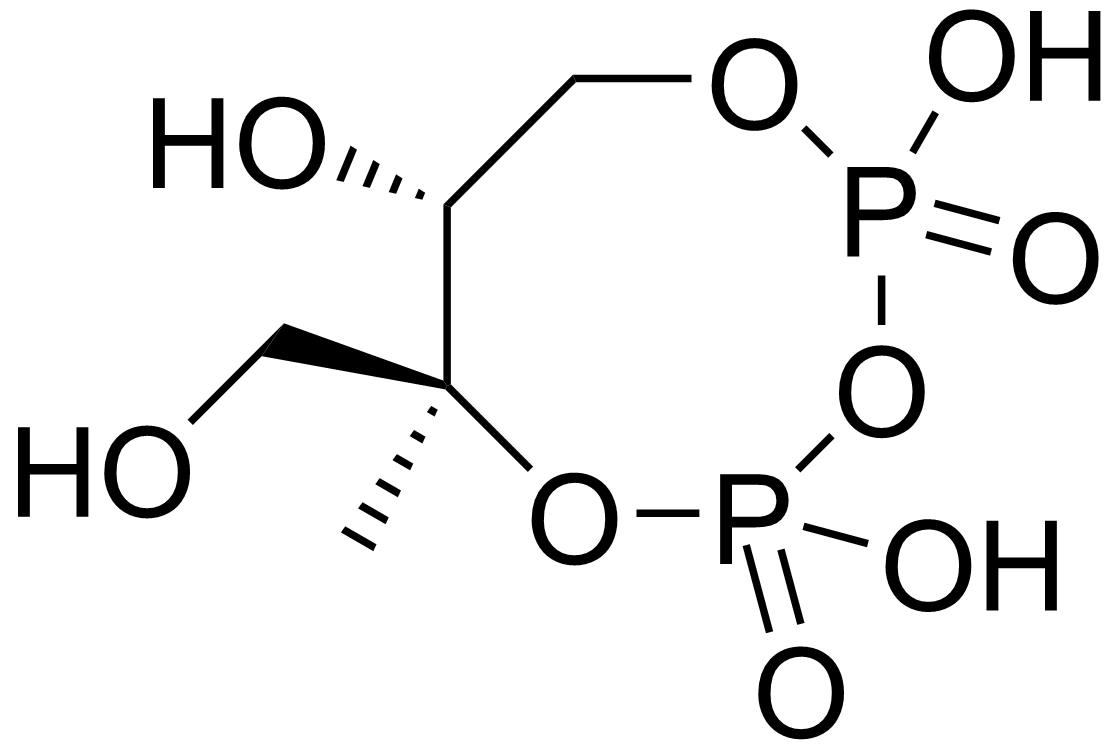
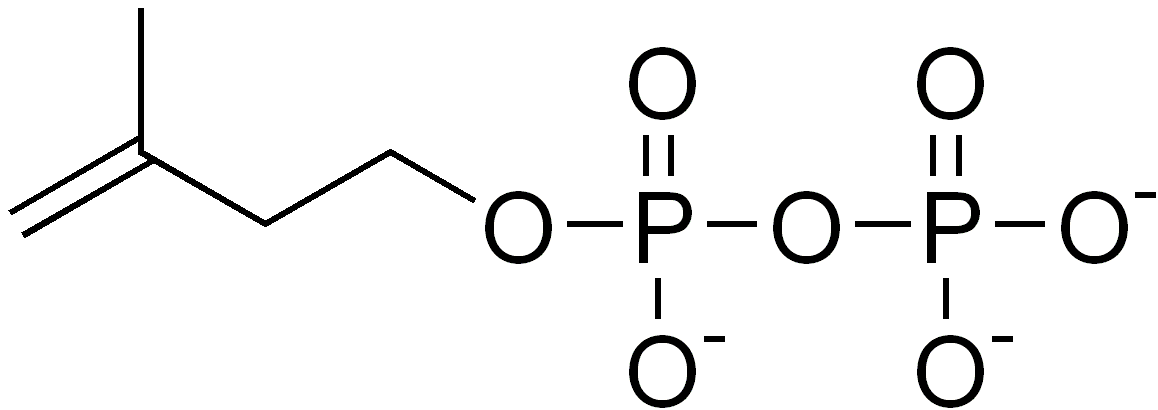
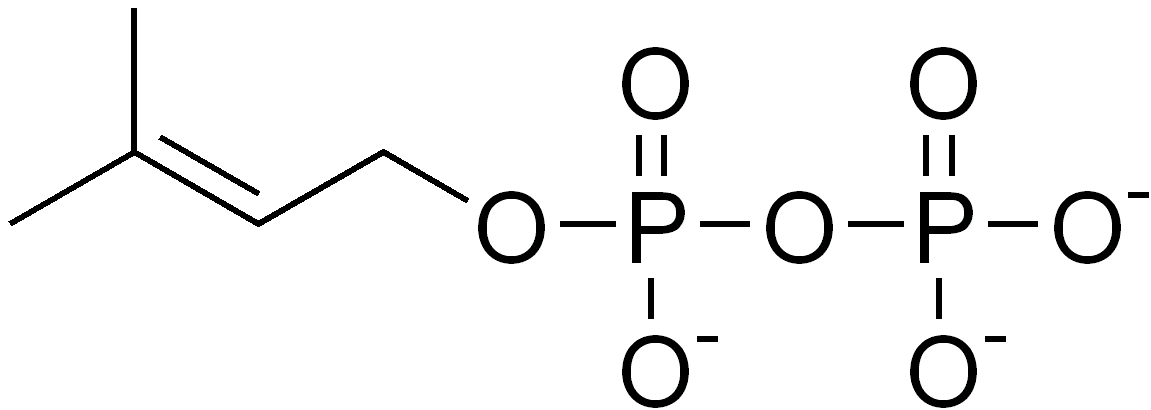
비메발론산 경로는 대부분의 고등 진핵생물과 일부 세균에서 발견되는 아이소프레노이드 전구체의 생합성 대사 경로이다. 이 경로는 아이소프레노이드 분자의 생합성에 필수적인 아이소펜테닐 피로인산(IPP)과 다이메틸알릴 피로인산(DMAPP)을 생성하며, 단백질 프레닐화, 세포막 유지, 호르몬 합성 등 다양한 과정에 사용된다. 세균, 식물, 원생동물은 비메발론산 경로를 통해 아이소프레노이드 전구체를 생성하며, 식물은 세포질에서 메발론산 경로를, 엽록체에서 비메발론산 경로를 사용한다. 비메발론산 경로는 DXP 리덕토아이소머레이스와 같은 효소에 의해 조절되며, 포스미도마이신과 같은 물질에 의해 억제될 수 있다. 이 경로는 항생제 및 항말라리아제 개발의 표적이 되며, 산업적으로는 테르페노이드 생산에 활용된다.
더 읽어볼만한 페이지
- 대사경로 - 스테로이드
스테로이드는 4개의 융합된 고리 구조를 가지는 유기 화합물로, 콜레스테롤, 스테로이드 호르몬, 담즙산 등 생물학적 활성 분자를 포함하며, 메발론산 경로를 통해 생합성되어 다양한 생리적 기능을 수행하고 의학적으로 사용되지만 오남용 시 부작용을 초래할 수 있다. - 대사경로 - 시트르산 회로
시트르산 회로는 아세틸-CoA를 이산화탄소로 산화시켜 NADH와 FADH₂를 생성, ATP 생산 및 생합성에 기여하며, 탄수화물, 지방, 단백질 대사를 연결하는 중심적인 대사 경로이다. - 물질대사 - 아라키드산
아라키드산은 탄소 20개로 이루어진 포화 지방산으로, 땅콩 기름과 같은 식물성 기름에 많이 함유되어 있으며, 인체 내에서 세포막 구성, 신호 전달 물질의 전구체, 에이코사노이드 합성에 관여하고, 제약 산업에서 프로스타글란딘의 전구체로 사용되는 경제적 가치가 높은 물질이다. - 물질대사 - 카프릴산
카프릴산은 8개의 탄소로 이루어진 포화 지방산으로, 식품, 향료, 소독제 등 다양한 산업에 사용되며, 식욕 촉진, 항균 작용, 간질 치료 등 의학적 용도로도 연구된다.
2. 생합성 경로
메발론산 경로는 대부분의 고등 진핵생물과 일부 세균에 존재하는 아이소프레노이드 전구체의 생합성 대사 경로이다. 메발론산 경로는 아이소프레노이드(테르페노이드) 분자의 생합성을 위한 필수적인 전구물질인 아이소펜테닐 피로인산(IPP)과 다이메틸알릴 피로인산(DMAPP)을 생성하기 때문에 중요하다. 아이소프레노이드는 단백질의 프레닐화, 세포막의 유지, 호르몬 합성, 지질-닻 단백질 및 N-글리코실화와 같은 다양한 과정에 사용된다.[30]
세균, 식물, 말라리아 원충과 같은 정단복합체충류 원생동물은 대체 경로인 비메발론산 경로를 사용하여 아이소프레노이드 전구체를 생성할 수 있다. 식물과 특정 원생동물의 경우, 아이소펜테닐 피로인산(IPP)과 다이메틸알릴 피로인산(DMAPP)의 생합성은 색소체에서 일어난다.[30] 식물은 세포질에서 메발론산 경로를 사용하고, 엽록체에서 비메발론산 경로를 사용하여 아이소프레노이드 전구체를 합성한다. 비메발론산 경로를 사용하는 세균에는 결핵균과 같은 중요한 병원균 등이 있다.[31]
메발론산 경로 (MVA 경로 또는 HMG-CoA 환원효소 경로)와 MEP 경로는 이소프레노이드 전구체인 IPP와 DMAPP의 생합성을 위한 대사 경로이다. 식물은 MVA 경로와 MEP 경로를 모두 사용하는 반면, 대부분의 생물은 이소프레노이드 전구체의 생합성에 이 두 경로 중 하나만 사용한다. 식물 세포에서 MEP 경로를 통한 IPP/DMAPP 생합성은 엽록체 소기관에서 일어나고, MVA 경로를 통한 생합성은 세포질에서 일어난다.[4] 대부분의 그람 음성 세균, 광합성 시아노박테리아 및 녹조류는 MEP 경로만 사용한다.[5] MEP 경로를 사용하는 세균에는 중요한 병원균인 ''결핵균''이 포함된다.[6]
IPP와 DMAPP는 단백질 프레닐화, 세포막 유지, 호르몬 합성, 단백질 앵커링 및 모든 생명체의 ''N''-당화와 같이 다양한 과정에 사용되는 이소프레노이드 (테르페노이드) 분자의 생합성을 위한 전구체 역할을 한다. 광합성 생물에서 MEP 유래 전구체는 카로티노이드 및 엽록소의 피톨 사슬과 광수집 색소와 같은 광합성 색소의 생합성에 사용된다.[5]
2. 1. 반응 단계
비메발론산 경로의 반응은 주로 아이젠라이크(Eisenreich)와 그의 동료들에 의해 밝혀졌다.[33][32]
비메발론산 경로는 메발론산 경로와 거의 공통점이 없지만, 4-다이포스포시티딜-2-C-메틸-D-에리트리톨 키네이스 (IspE)만 메발론산 경로에 포함된 일부 효소 (메발론산 키나아제 등)와 상동성을 가지며, 같은 GHMP 효소 패밀리에 속한다.
2. 2. 각 단계별 효소 및 반응 설명
비메발론산 경로는 대부분의 고등 진핵생물과 일부 세균에 존재하는 아이소프레노이드 전구체의 생합성 대사 경로이다. 이 경로는 아이소펜테닐 피로인산(IPP)과 다이메틸알릴 피로인산(DMAPP)을 생성하는데, 이들은 단백질의 프레닐화, 세포막 유지, 호르몬 합성, 지질-닻 단백질 및 N-글리코실화와 같은 다양한 과정에 사용되는 아이소프레노이드(테르페노이드) 분자의 생합성에 필수적인 전구물질이다.[30]세균, 식물, 말라리아 원충과 같은 정단복합체충류 원생동물은 비메발론산 경로를 사용하여 아이소프레노이드 전구체를 생성할 수 있다. 식물과 특정 원생동물의 경우, IPP와 DMAPP의 생합성은 색소체에서 일어난다.[30] 식물은 세포질에서 메발론산 경로를, 엽록체에서 비메발론산 경로를 사용하여 아이소프레노이드 전구체를 합성한다. 비메발론산 경로를 사용하는 세균에는 결핵균과 같은 중요한 병원균 등이 있다.[31]
비메발론산 경로의 반응들은 주로 아이젠라이크(Eisenreich)와 그의 동료들에 의해 밝혀졌다.[33][32]
Dxs는 비메발론산 경로의 첫 번째 효소로, 생성물인 IPP와 DMAPP에 의해 피드백 저해를 받는다. Dxs는 호모이량체로 활성화되는데, 효소 저해의 정확한 메커니즘에 대해서는 논쟁이 있었다. IPP/DMAPP가 보조 인자 TPP와 경쟁한다는 주장이 제기되었다.[11] 그러나 최근 연구에서는 IPP/DMAPP가 효소의 단량체화와 그에 따른 분해를 유발하며, 이는 효소의 활성 부위와 다른 단량체 상호작용 부위와의 상호작용을 통해 일어난다고 제안했다.[12]
메발론산 경로는 대부분의 고등 진핵생물과 일부 세균에 존재하는 아이소프레노이드 전구체의 생합성 대사 경로이다. 이 경로는 아이소펜테닐 피로인산(IPP)과 다이메틸알릴 피로인산(DMAPP)을 생성하는데, 이들은 단백질 프레닐화, 세포막 유지, 호르몬 합성, 지질-닻 단백질, N-글리코실화와 같은 다양한 과정에 사용되는 아이소프레노이드(테르페노이드) 분자 생합성에 필수적인 전구물질이다.[30]
대장균(Escherichia coli)은 비메발론산 경로(MEP 경로)가 광범위하게 연구되었고, 실험 연구 및 응용 분야에 일반적으로 사용되는 미생물 종으로 유전자 조작이 이루어졌다.[18] MEP 경로의 산물인 IPP와 DMAPP는 제약 및 화학 산업에서 높은 가치를 지닌 테르페노이드의 이종 생산을 위한 기질로 사용될 수 있다. 다양한 유기체에서 이종 발현 유전자를 발현시키면, 리모넨, 비사볼렌, 아이소프렌과 같은 테르페노이드를 다양한 미생물 섀시에서 생산할 수 있다.[19][20][21][22] 경로의 서로 다른 생합성 유전자를 과발현하는 연구를 통해, MEP 경로의 첫 번째 단계와 마지막 단계를 촉매하는 Dxs와 Idi의 발현이 MEP 유래 테르페노이드의 수율을 상당히 증가시킬 수 있다는 것이 밝혀졌다.[19][22] 경로의 첫 번째 효소인 Dxs는 경로에 들어가는 탄소의 흐름에 병목 현상을 나타낸다. IPP를 DMAPP로 상호 변환하는 Idi는 유전자 조작 균주에 이종 탄소 싱크를 도입한 후 필요한 각 기질을 제공하는 데 중요한 역할을 하는 것으로 보인다. MEP 경로에 대한 많은 대사 공학 연구가 시아노박테리아에서 이루어졌으며, 이들은 대기 중의 이산화 탄소를 테르페노이드를 포함한 다양한 탄소 함유 대사 산물로 동화할 수 있는 광합성 독립 영양 미생물이다.[20][19][21] 따라서 시아노박테리아는 생명 공학 분야에서 고부가가치 화합물의 지속 가능한 생산을 위한 매력적인 플랫폼이다.
[1]
저널
The discovery of a mevalonate-independent pathway for isoprenoid biosynthesis in bacteria, algae and higher plants
DXP 리덕토아이소머레이스는 비메발론산 경로의 핵심 효소이며, 천연물 포스미도마이신에 의해 저해될 수 있다. 포스미도마이신은 항생제 또는 항말라리아제 후보 약물 개발의 출발점으로 연구되고 있다.[34][35][36]
대사 중간생성물인 (E)-4-하이드록시-3-메틸뷰트-2-엔일 피로인산(HMB-PP)은 말초 혈액에서 주요 γδ T 세포 집단이자 미생물 병원체에 대한 면역 반응에 중요한 역할을 하는 사람의 Vγ9/Vδ2 T 세포의 천연 활성인자이다.[37]
3. 조절
DXP 환원 효소 (DXR, DOXP 환원 효소, IspC, MEP 합성 효소라고도 함)는 MEP 경로의 핵심 효소이다. 이 효소는 천연물 포스미도마이신에 의해 저해될 수 있으며, 포스미도마이신은 항생제 또는 항말라리아 약물 후보 개발의 출발점으로 연구되고 있다.[13][14][15]
중간체인 HMB-PP는 인간 Vγ9/Vδ2 T 세포의 자연 활성제이며, Vγ9/Vδ2 T 세포는 말초 혈액에서 주요 γδ T 세포 집단이며 "미생물 병원체에 대한 면역 반응에서 중요한 역할을 수행하는" 세포이다.[16]
IspH 저해제는 대부분의 박테리아에 필수적이지만 인간에게는 존재하지 않는 비메발론산 대사 경로를 표적으로 한다. 메틸-D-에리트리톨 인산(MEP) 또는 비메발론산 경로라고 불리는 이 경로는 대부분의 병원성 박테리아에서 세포 생존에 필요한 아이소프레노이드의 생합성을 담당하므로, 일반적으로 항생제에 내성을 보이는 박테리아에 도움이 될 것이다.[17]
4. 생물학적 중요성
세균, 식물, 말라리아 원충과 같은 정단복합체충류 원생동물은 비메발론산 경로를 사용하여 아이소프레노이드 전구체를 생성할 수 있다. 식물과 특정 원생동물의 경우, 아이소펜테닐 피로인산(IPP)과 다이메틸알릴 피로인산(DMAPP) 생합성은 색소체에서 일어난다.[30] 식물은 세포질에서 메발론산 경로를 사용하고, 엽록체에서 비메발론산 경로를 사용하여 아이소프레노이드 전구체를 합성한다. 비메발론산 경로를 사용하는 세균에는 결핵균과 같은 중요한 병원균 등이 있다.[31]
DXP 리덕토아이소머레이스는 비메발론산 경로의 핵심 효소이며, 천연물 포스미도마이신에 의해 저해될 수 있다. 포스미도마이신은 항생제 또는 항말라리아제 후보 약물 개발을 위한 출발점으로 연구되고 있다.[34][35][36]
대사 중간생성물인 (E)-4-하이드록시-3-메틸뷰트-2-엔일 피로인산(HMB-PP)은 사람의 Vγ9/Vδ2 T 세포의 천연 활성인자인데, 이 세포는 말초 혈액에서 주요 γδ T 세포 집단이자 미생물 병원체에 대한 면역 반응에 중요한 역할을 한다.[37]
5. 산업적 응용
참조
[2]
저널
Review Biosynthesis of isoprenoids via the non-mevalonate pathway
[3]
저널
The Non-mevalonate Pathway of Isoprenoid Precursor Biosynthesis
[4]
저널
The 1-Deoxy-D-xylulose-5-phosphate pathway of isoprenoid biosynthesis in plants
[5]
저널
Network Analysis of the MVA and MEP Pathways for Isoprenoid Synthesis
https://www.annualre[...]
2013-04-29
[6]
저널
Isoprenoid Metabolism as a Therapeutic Target in Gram-Negative Pathogens
2010
[7]
저널
Engineering a mevalonate pathway in ''Escherichia coli'' for production of terpenoids
[8]
저널
Metabolic flux ratio analysis by parallel 13C labeling of isoprenoid biosynthesis in ''Rhodobacter sphaeroides''
[9]
저널
Exploring Drug Targets in Isoprenoid Biosynthetic Pathway for Plasmodium falciparum
2014
[10]
저널
Biosynthesis of Isoprenoids Via the Non-mevalonate Pathway
[11]
저널
Feedback Inhibition of Deoxy-d-xylulose-5-phosphate Synthase Regulates the Methylerythritol 4-Phosphate Pathway
2013-06
[12]
저널
MEP pathway products allosterically promote monomerization of deoxy-D-xylulose-5-phosphate synthase to feedback-regulate their supply
2023-05-08
[13]
저널
The MEP pathway and the Development of Inhibitors as Potential Anti-Infective Agents
2012
[14]
저널
Inhibitors of the Nonmevalonate Pathway of Isoprenoid Biosynthesis as Antimalarial Drugs
[15]
저널
Isoprenoid Biosynthesis via the Methylerythritol Phosphate Pathway: Structural Variations around Phosphonate Anchor and Spacer of Fosmidomycin, a Potent Inhibitor of Deoxyxylulose Phosphate Reductoisomerase
[16]
저널
Microbial Isoprenoid Biosynthesis and Human γδ T cell Activation
[17]
뉴스
Research team reports new class of antibiotics active against a wide range of bacteria
https://www.mdlinx.c[...]
2020-12-23
[18]
저널
Elucidation of the Methylerythritol Phosphate Pathway for Isoprenoid Biosynthesis in Bacteria and Plastids. A Metabolic Milestone Achieved through Genomics
2002-11-01
[19]
저널
Systematic overexpression study to find target enzymes enhancing production of terpenes in Synechocystis PCC 6803, using isoprene as a model compound
2018-09-01
[20]
저널
Engineering the methylerythritol phosphate pathway in cyanobacteria for photosynthetic isoprene production from CO2
https://pubs.rsc.org[...]
2016-04-13
[21]
저널
Metabolic engineering of Synechocystis sp. PCC 6803 for improved bisabolene production
2021-06-01
[22]
저널
Enhanced limonene production by optimizing the expression of limonene biosynthesis and MEP pathway genes in E. coli
2014-08-31
[23]
저널
The discovery of a mevalonate-independent pathway for isoprenoid biosynthesis in bacteria, algae and higher plants
[24]
저널
THE 1-DEOXY-D-XYLULOSE-5-PHOSPHATE PATHWAY OF ISOPRENOID BIOSYNTHESIS IN PLANTS
http://www.annualrev[...]
1999-06
[25]
저널
Biosynthesis of isoprenoids via the non-mevalonate pathway
[26]
저널
Inhibitors of the nonmevalonate pathway of isoprenoid biosynthesis as antimalarial drugs
[27]
저널
The discovery of a mevalonate-independent pathway for isoprenoid biosynthesis in bacteria, algae and higher plants
[28]
저널
Review Biosynthesis of isoprenoids via the non-mevalonate pathway
[29]
저널
The Non-mevalonate Pathway of Isoprenoid Precursor Biosynthesis
http://www.jbc.org/c[...]
[30]
저널
The 1-Deoxy-D-xylulose-5-phosphate pathway of isoprenoid biosynthesis in plants
[31]
저널
Isoprenoid Metabolism as a Therapeutic Target in Gram-Negative Pathogens
2010
[32]
저널
Exploring Drug Targets in Isoprenoid Biosynthetic Pathway for Plasmodium falciparum
2014
[33]
저널
Biosynthesis of Isoprenoids Via the Non-mevalonate Pathway
[34]
저널
The MEP pathway and the Development of Inhibitors as Potential Anti-Infective Agents
http://pubs.rsc.org/[...]
2012
[35]
저널
Inhibitors of the Nonmevalonate Pathway of Isoprenoid Biosynthesis as Antimalarial Drugs
[36]
저널
Isoprenoid Biosynthesis via the Methylerythritol Phosphate Pathway: Structural Variations around Phosphonate Anchor and Spacer of Fosmidomycin, a Potent Inhibitor of Deoxyxylulose Phosphate Reductoisomerase
[37]
저널
Microbial Isoprenoid Biosynthesis and Human γδ T cell Activation
본 사이트는 AI가 위키백과와 뉴스 기사,정부 간행물,학술 논문등을 바탕으로 정보를 가공하여 제공하는 백과사전형 서비스입니다.
모든 문서는 AI에 의해 자동 생성되며, CC BY-SA 4.0 라이선스에 따라 이용할 수 있습니다.
하지만, 위키백과나 뉴스 기사 자체에 오류, 부정확한 정보, 또는 가짜 뉴스가 포함될 수 있으며, AI는 이러한 내용을 완벽하게 걸러내지 못할 수 있습니다.
따라서 제공되는 정보에 일부 오류나 편향이 있을 수 있으므로, 중요한 정보는 반드시 다른 출처를 통해 교차 검증하시기 바랍니다.
문의하기 : help@durumis.com