키메라 항원 수용체 T 세포
"오늘의AI위키"의 AI를 통해 더욱 풍부하고 폭넓은 지식 경험을 누리세요.
1. 개요
키메라 항원 수용체 T 세포(CAR-T 세포)는 암세포를 표적으로 공격하도록 유전자 조작된 T 세포를 이용하는 면역 치료법이다. 1980년대에 개념이 제시되었으며, 항체와 T 세포 수용체의 결합을 통해 개발되었다. CAR-T 세포는 외부 도메인, 막 도메인, 내부 도메인으로 구성되며, 외부 도메인은 암세포의 특정 항원을 인식하고, 내부 도메인은 T 세포를 활성화하는 역할을 한다.
CAR-T 세포 치료는 혈액암 치료에 주로 사용되며, 특히 CD19를 표적으로 하는 치료법이 림프종, 백혈병 환자에게 효과를 보였다. 고형암 치료에도 연구가 진행 중이지만, 종양의 이질성, 종양 미세 환경, 면역 억제 환경 등의 한계로 인해 어려움이 있다. CAR-T 세포의 부작용으로는 사이토카인 방출 증후군(CRS), 신경 독성 등이 있으며, 이를 해결하기 위한 자살 유전자, 이중 항원 수용체, ON/OFF 스위치 등의 기술이 개발되고 있다.
CAR-T 세포 치료는 고비용의 치료법이며, 전 세계적으로 사용 가능 지역이 제한적이다.
더 읽어볼만한 페이지
- 백혈병 - 한국백혈병어린이재단
한국백혈병어린이재단은 백혈병, 소아암 및 희귀난치성 질환을 앓는 어린이와 가족을 위해 2000년 설립된 재단법인으로, 치료비 지원, 쉼터 운영, 정서 지원, 정보 제공 등 의료사회복지 서비스를 제공하며 투명한 운영으로 인정받고 이승환, 김종석 등이 홍보대사로 활동한다. - 백혈병 - 급성 백혈병
급성 백혈병은 백혈구 세포의 비정상적 증식으로 발생하는 혈액암으로, 미성숙한 백혈구 세포가 말초혈로 유출되어 빈혈, 발열, 출혈 등의 증상을 동반하며, 골수 검사를 통해 진단하고, 화학 요법, 조혈모세포 이식 등으로 치료한다. - 유전자 치료 - 미토콘드리아 대체요법
미토콘드리아 대체요법은 손상된 미토콘드리아를 건강한 미토콘드리아로 대체하여 세포 기능을 회복시키는 치료법으로, 미토콘드리아 유전 질환 예방과 치료에 활용되며, 전핵 이식, 극체 이식, 세포질 이전 등의 기술을 포함하고 윤리적 쟁점과 안전성 문제가 존재한다. - 유전자 치료 - 오나셈노진아베파르보벡
오나셈노진아베파르보벡은 척수성 근위축증(SMA) 치료를 위해 개발되어 미국, 유럽 연합, 캐나다에서 승인받은 유전자 치료제로서, SMN1 유전자를 대체하는 SMN 유전자를 전달하여 영유아 SMA 환자에게 효과를 나타내지만, 간 기능 이상 등의 부작용과 경제적, 윤리적 이슈가 존재하며 대한민국에는 아직 도입되지 않았다. - T 세포 - CD4
CD4는 보조 T 세포 표면에서 T 세포 수용체의 공동수용체로 작용하여 항원제시세포와 상호작용을 돕고 T 세포 활성화 신호를 증폭시키는 면역계의 당단백질이며, HIV의 숙주 세포 침투 수용체로 작용하여 HIV 감염 및 AIDS 발병에 중요한 역할을 한다. - T 세포 - T세포 수용체
T세포 수용체(TCR)는 T 세포 표면의 이량체 단백질 복합체로, MHC 분자에 결합된 펩타이드를 인식하며, CD3 분자와 복합체를 이루어 신호 전달을 매개하고, V(D)J 재조합을 통해 다양한 항원 특이성을 갖는 T 세포 생성에 기여하여, CAR-T 치료 등 면역 요법 발전에 기여했다.
2. 역사적 배경
키메라 항원 수용체(CAR) 개념은 1987년 일본의 쿠와나 요시히사가 처음 제시하였고,[130] 1989년 이스라엘 바이츠만 연구소의 젤리그 에샤르와 기드온 그로스가 항체의 특정 항원 결합 능력과 TCR-α 또는 TCR-β 단백질의 불변 도메인을 결합한 형태로 발전시켰다.[7][8] 초기에는 "T-바디"라고 불렸다.[10]
키메라 항원 수용체(CAR)는 외부 도메인, 막 도메인, 내부 도메인의 세 부분으로 구성된다.[139] 1989년 이스라엘의 에샤하르(Eshahar) 박사가 처음 고안했으며, 당시에는 T-body로 불렸다. 초기에는 현재와 같은 단일 사슬 구조가 아닌, 면역글로불린 중쇄(VH) 및 경쇄(VL)의 항원 결합 부위를 T 세포 수용체의 α 사슬(Cα) 및 β 사슬(Cβ)의 불변 부위와 결합한 형태였다. 이후 VH와 VL을 링커로 연결하여 현재와 같은 단일 사슬 키메라 수용체가 개발되어 구조가 단순화되고 효율이 높아졌다.[138]
1991년, 아서 와이스는 CD3ζ 세포 내 신호 전달 도메인을 포함하는 키메라 수용체를 개발하여 T 세포 신호 전달 활성화를 입증하였다.[11] 이는 1세대 CAR로 명명되었다.[12][13]
2000년대 초반, CD28 또는 4-1BB와 같은 공동 자극 도메인이 1세대 CAR의 CD3ζ 세포 내 도메인에 추가된 2세대 CAR가 개발되어 전임상 모델에서 더 큰 지속성과 개선된 종양 제거 효과를 보였다.[15] 2010년대 초반, 국립 암 연구소(NCI), 펜실베이니아 대학교, 메모리얼 슬론 케터링 암 센터의 연구자들이 CD19를 표적으로 하는 2세대 CAR를 사용한 임상 시험에서 B 세포 백혈병 및 B 세포 림프종 환자들에게서 완전 관해를 가져오는 등 CAR T 세포 치료의 임상적 효능을 입증하였다.[14]
이러한 시험들을 바탕으로 2017년 미국 식품의약국(FDA)은 노바티스의 티사젠렉류셀(킴리아)과 키트 파마의 악시캅타젠 실로류셀(예스카르타)을 승인하였다.[14] 현재 FDA 승인을 받은 CAR T 치료법은 6개이다.[16]
3. 키메라 항원 수용체의 구조
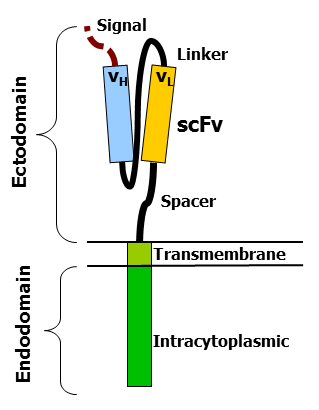
CAR는 세포 외 항원 인식 도메인을 세포 내 신호 전달 도메인에 연결하며, 항원이 결합하면 T 세포를 활성화한다. 일반적인 CAR는 단일 사슬 가변 단편(scFv)과 CD3-ζ 막 횡단 도메인 및 세포내 도메인을 융합한 것이다.[77][78] 예를 들어, 14g2a-ζ는 하이브리도마 14g2a(이는 디시알로강글리오사이드 GD2를 인식한다)에서 유래한 scFv와의 융합 단백질이다.
항체의 가변 부위는 중쇄 및 경쇄로 구성되며, 두 개의 항원 인식 부위를 갖는다. 키메라 항원 수용체에서는 유연한 링커에 의해 중쇄 가변 부위 VH와 경쇄 가변 부위 VL이 결합하여 단일 사슬 가변 부위 단편(scFv)을 형성한다. 막 횡단 도메인은 전형적인 소수성의 α-나선 단백질이다. I형 단백질은 두 개의 단백질 도메인이 막 횡단 α-나선 단백질에 의해 연결되어 있고 세포막의 지질 이중층을 막 횡단 도메인이 관통하며, 세포막이 세포 내부와 세포 외부를 나눈다.
ScFv/CD3-ζ 하이브리드는 scFv가 항원을 인식하고 ζ 신호를 전달한다. 형질도입된 T 세포는 표적 세포에 발현되는 GD2(예: 신경모세포종 세포)를 인식하고 살상한다. 악성 B 세포를 대상으로 B 세포 표면 마커인 CD19 특이적 키메라 항원 수용체가 연구되고 있다.
3. 1. 외부 도메인 (Ecto domain)
Ecto domain영어은 세포 바깥에 위치한 부분으로, 신호 펩타이드, 항원 인지 부위, 그리고 간격 부위로 구성된다.[140]3. 2. 막 도메인 (Transmembrane domain)
막 도메인은 소수성 알파 나선 구조로 이루어져 있으며, 수용체의 안정화에 기여한다.[139] 이 도메인은 CAR을 세포막에 고정시켜 세포 외 힌지와 항원 인식 도메인을 세포 내 신호 영역과 연결하는 역할을 한다.[77] 일반적으로 엔도도메인의 가장 막에 가까운 구성 요소의 세포막 관통 도메인이 사용되지만, 서로 다른 세포막 관통 도메인은 서로 다른 수용체 안정성을 초래한다.[84] CD28 막 도메인이 발현이 높고 안정적인 수용체를 만드는 것으로 알려져 있다.[84]
CD3-제타 세포막 관통 도메인을 사용하는 것은 권장되지 않는데, 이는 인공 TCR가 원래의 TCR에 통합될 수 있기 때문이다.[88]
3. 3. 내부 도메인 (Endo domain)
내부 도메인은 리셉터의 기능적인 역할을 수행하며, 기본적인 요소로는 하위 신호전달 역할을 수행하는 면역세포 활성화를 담당하는 면역수용체 티로신 기반 활성 모티프(ITAM)의 일부분인 CD3-제타이다.[139] 정상적인 T 세포 활성화는 ITAM의 인산화에 의존하며, 이는 CD3-제타의 세포질 도메인에 존재한다. 이 과정을 모방하기 위해 CD3-제타의 세포질 도메인은 일반적으로 주요 CAR 엔도도메인 구성 요소로 사용된다. 다른 ITAM 함유 도메인도 시도되었지만 효과가 떨어졌다.[78]
T 세포는 활성화 후 지속되기 위해 CD3 신호 외에 공동 자극 분자도 필요하다. 이러한 이유로 CAR 수용체의 엔도도메인은 일반적으로 공동 자극 단백질의 하나 이상의 키메라 도메인을 포함한다.[90] CD28, CD27, CD134 (OX40), CD137 (4-1BB)를 포함한 다양한 공동 자극 분자의 신호 도메인이 성공적으로 테스트되었다.[77]
사용된 세포내 신호 도메인은 CAR T 세포의 세대를 정의한다.[3] 1세대 CAR는 CD3-제타 세포질 도메인만 포함한다.[3] 2세대 CAR는 CD28 또는 4-1BB와 같은 공동 자극 도메인을 추가한다. 이러한 세포내 신호 도메인의 참여는 T 세포 증식, 사이토카인 분비, 세포 사멸 저항성 및 생체 내 지속성을 향상시킨다.[3] 3세대 CAR는 CD28-4-1BB 또는 CD28-CD134 (OX40)과 같은 여러 공동 자극 도메인을 결합하여 T 세포 활성을 증강시킨다. 전임상 데이터에 따르면 3세대 CAR는 2세대 CAR에 비해 향상된 이펙터 기능과 더 나은 생체 내 지속성을 나타낸다.[3]
4. CAR-T 세포의 생산 및 적용
CAR-T 세포는 환자 자신의 혈액(자가) 또는 건강한 기증자의 혈액(동종)에서 T 세포를 분리하여 제조된다. 백혈구성분채집술을 통해 T 세포를 분리하고, 의약품제조관리기준(GMP)을 만족하는 시설에서 생산한다.[145]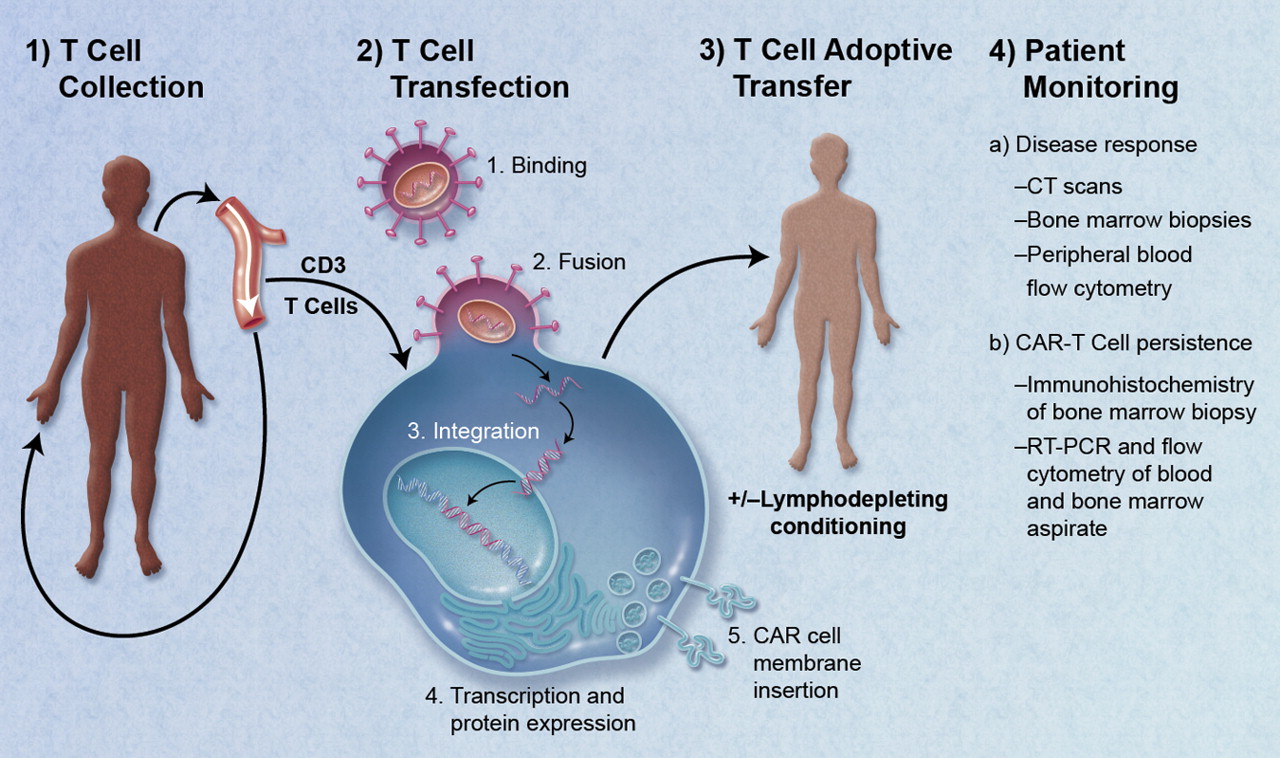
CAR-T 세포 생산 과정은 다음과 같다.
1. T 세포 분리: 환자 또는 건강한 기증자의 혈액에서 백혈구를 분리하고, 그중에서 T 세포를 분리한다.[17][18]
2. T 세포 활성화 및 증식: 분리된 T 세포는 사이토카인의 일종인 인터류킨 2(IL-2) 및 항-CD3 항체 등으로 처리하여 활성화 및 증식을 유도한다.[19]
3. CAR 유전자 형질도입: 활성화된 T 세포에 레트로바이러스 또는 렌티바이러스 벡터를 이용하여 암세포 특이적 CAR 유전자를 형질도입시킨다.[18]
4. CAR-T 세포 증식: CAR 유전자가 도입된 T 세포를 증식시킨다.
5. 림프구 제거 화학요법: CAR-T 세포를 환자에게 주입하기 전에, 환자의 림프구를 제거하는 화학요법을 시행한다. 이는 T 세포 활성을 억제하는 세포와 사이토카인을 제거하여 CAR-T 세포의 효능을 높이기 위함이다.[3][146]
6. CAR-T 세포 주입: 증식된 CAR-T 세포를 환자에게 주입한다.
CAR는 단일 사슬 가변 부위 단편(scFv)과 CD3-ζ 막 횡단 도메인 및 세포내 도메인을 융합한 것이다. scFv는 항체의 가변 부위로, 중쇄 및 경쇄가 결합하여 형성되며, 암세포 표면의 특정 항원을 인식한다. 막 횡단 도메인은 소수성의 α-나선 단백질로 구성되며, 세포막을 관통하여 신호를 전달한다.
4. 1. 임상 적용
CAR-T 세포 치료는 B 림프종 및 림프종 환자에게서 높은 효능을 보이며, 다발골수종 환자를 대상으로 한 임상시험에서도 매우 성공적으로 진행되고 있다. 급성 골수성 백혈병을 대상으로도 치료를 시도하고 있다.[147] 2019년 3월 기준으로 전 세계에서 약 364건의 CAR-T 세포 관련 임상 시험이 진행 중이며, 이 중 대다수는 혈액암을 대상으로 한다.[23] CD19는 여전히 가장 많이 사용되는 항원 표적이며,[24] 그 다음으로는 다발성 골수종에서 흔히 발현되는 BCMA가 뒤를 잇는다.[23][25] 2016년에는 CD20과 같은 다른 항원의 가능성을 알아보는 연구도 시작되었다.[26]하지만 CAR-T 치료는 혈액암에 국한되어 있고, 환자의 90%를 차지하는 고형암에서는 효과적인 임상 결과를 보여주지 못하고 있다. 이는 앞으로 CAR-T 치료제의 효능과 안전성을 높이기 위해 더 많은 연구와 임상 평가가 필요함을 의미한다.[147] 고형 종양에 대한 임상 시험은 CAR-T가 덜 지배적인 양상을 보이며, 세포 치료 기반 임상 시험의 약 절반은 NK 세포와 같은 다른 플랫폼을 포함한다.[23]
CAR-T 치료의 어려운 점은 다음과 같다.[148][149][150]
- 종양의 이질성(heterogeneity): 종양 내 각기 다른 genome instability가 불안정하면서 이와 관련하여 tumor associated antigen(TAA)을 발현하는데, 이는 CAR의 표적 선정에 어려움을 준다.
- 종양이 발현하는 케모카인: 면역세포의 이동을 조절하는 케모카인 중, 종양은 면역세포들의 부적절한 케모카인을 발현시켜 종양 주변으로 접근하지 못하게 막는다.
- 면역세포를 억제시키는 환경: CANCER ASSOCIATED FIBROBLAST(CAF)에 의해 면역세포들의 물리적인 접근을 차단하고, 저산소증 상태를 유지시켜 면역세포들의 활성과 증식을 줄인다. 또한 젖당생성과 포도당결핍으로 면역세포의 증식과 사이토카인 생성을 억제시킨다.
- tumor에서 유래된 soluble factor 또는 사이토카인 그리고 MDSC, TAM, TAN에 의해 분비되는 prostaglandin, TGF-β, IL-10같은 Pro-inflammatory cytokine에 의해 면역을 억제시킨다.
CAR-T 세포 치료 후 가장 흔한 문제는 사이토카인 방출 증후군(CRS)으로, 면역 체계가 활성화되어 염증성 사이토카인의 수가 증가하는 상태이다. 이 증후군의 임상적 증상은 고열, 피로, 근육통, 메스꺼움, 모세 혈관 누출, 빈맥 및 기타 심장 기능 부전, 간부전, 신장 손상으로 패혈증과 유사하다.[68] CRS는 CAR-T 세포 치료를 받는 거의 모든 환자에게서 발생하며, CAR-T 세포가 암세포를 죽이고 있음을 나타내는 진단 지표이기도 하다.[66] 중증 사이토카인 방출 증후군은 면역억제제인 코르티코스테로이드와 토실리주맙 (항-IL-6 단클론 항체)을 사용하여 관리할 수 있다.[69]
5. CAR-T 치료의 한계 및 극복 과제
CAR-T 치료는 혈액암에서 높은 효능을 보였지만, 고형암에서는 효과가 제한적이다.[147] 이는 종양의 이질성, 종양 미세 환경, CAR-T 세포의 고갈 등 여러 요인 때문이다.
- 종양의 이질성(Heterogeneity): 종양 내 유전적 변이가 다양하여 종양 관련 항원(TAA) 발현이 달라지므로, CAR-T 세포가 표적을 선정하기 어렵다.[148]
- 종양 미세 환경(Tumor microenvironment): 종양은 면역 세포의 이동을 조절하는 케모카인을 발현하여 CAR-T 세포의 접근을 막는다. 또한, 암 관련 섬유아세포(CAF)는 면역 세포의 물리적 접근을 차단하고, 저산소 환경을 조성하여 면역 세포의 활성과 증식을 억제한다. 젖산 생성과 포도당 결핍은 면역 세포의 증식과 사이토카인 생성을 억제하며, 종양 유래 용해성 인자, 사이토카인, MDSC, TAM, TAN 등이 분비하는 프로스타글란딘, TGF-β, IL-10 등은 면역 억제 효과를 유발한다.[148][149][150]
5. 1. 안전성 문제
키메라 항원 수용체 T 세포(CAR-T 세포)가 신체에 도입되면 사이토카인 방출 증후군(CRS)과 신경 독성 같은 심각한 부작용이 발생할 수 있다.[3] CAR-T 세포 치료는 비교적 새로운 치료법이기에, 장기적인 영향에 대한 자료는 거의 없다. CAR-T 세포로 치료받은 여성 환자의 장기 생존 및 임신 합병증에 대한 우려도 여전히 존재한다.[66] CAR이 외부 단일클론 항체로 만들어져 면역 반응을 유발하므로 아나필락시스가 부작용으로 나타날 수 있다.온-타겟/오프-종양(On-target/Off-tumor) 인식은 CAR-T 세포가 올바른 항원을 인식하지만, 해당 항원이 건강한 비 병원성 조직에서도 발현될 때 발생한다. 이로 인해 CAR-T 세포가 CD19를 발현하는 건강한 B 세포와 같은 비 종양 조직을 공격하여 B 세포 무형성증을 유발할 수 있다. 이러한 부작용의 심각성은 다양하지만, 이전의 면역 억제, 림프구 감소 화학 요법 및 온-타겟 효과가 저감마글로불린혈증과 지속적인 세포 감소증을 유발하여 환자가 심각한 감염의 위험에 더 많이 노출될 수 있다.[19][67]
또한, 바이러스 벡터가 숙주 T 세포의 게놈 내 종양 억제 유전자 또는 암 유전자에 CAR 유전자를 삽입함으로써, 엔지니어링된 CAR-T 세포 자체가 삽입 돌연변이 유발을 통해 암세포로 변형될 가능성도 낮게나마 존재한다. 일부 레트로바이러스(RV) 벡터는 렌티바이러스(LV) 벡터보다 낮은 위험을 갖지만, 둘 다 종양 유발 가능성이 있다. T 세포 내 CAR 삽입 부위의 유전체 염기서열 분석은 생체 내 CAR-T 세포 기능 및 지속성을 더 잘 이해하기 위해 확립되었다.[82]
CAR-T 세포 치료 후 가장 흔한 문제는 사이토카인 방출 증후군(CRS)인데, 이는 면역 체계가 활성화되어 염증성 사이토카인의 수가 증가하는 상태이다. 이 증후군의 임상적 증상은 고열, 피로, 근육통, 메스꺼움, 모세 혈관 누출, 빈맥 및 기타 심장 기능 부전, 간부전, 신장 손상으로 패혈증과 유사하다.[68] CRS는 CAR-T 세포 치료를 받는 거의 모든 환자에게서 발생한다. 실제로 CRS의 존재는 CAR-T 세포가 의도한 대로 암세포를 죽이고 있음을 나타내는 진단 지표이다.[66] CRS의 심각성은 치료에 대한 반응 증가와 상관관계가 없으며, 오히려 높은 질병 부담과 관련이 있다.[66] 중증 사이토카인 방출 증후군은 면역억제제인 코르티코스테로이드와 토실리주맙(항-IL-6 단클론 항체)을 사용하여 관리할 수 있다.[69] 토실리주맙을 사용한 조기 개입은 여러 연구에서 치료 효과에 영향을 미치지 않으면서 심각한 CRS의 빈도를 감소시키는 것으로 나타났다.[70][71]
신경 독성은 CAR-T 세포 치료와 종종 관련이 있다.[73] 근본적인 기전은 잘 알려져 있지 않으며, CRS와 관련이 있을 수도 있고 없을 수도 있다. 임상 증상으로는 헛소리, 언어를 해석할 수 있는 능력을 유지하면서 조리 있게 말하는 능력의 부분적인 상실(표현성 실어증), 경계 저하(둔화), 발작 등이 있다.[66] 일부 임상 시험에서 신경 독성으로 인한 사망이 발생했으며, 주요 원인은 뇌부종이다. Juno Therapeutics, Inc.가 실시한 연구에서, 시험에 등록된 환자 5명이 뇌부종으로 사망했다. 환자 2명은 사이클로포스파미드 단독으로, 나머지 3명은 사이클로포스파미드와 플루다라빈의 병용 요법으로 치료받았다.[74] 프레드 허친슨 암 연구 센터가 후원하는 또 다른 임상 시험에서는 CAR-T 세포 투여 후 122일 만에 돌이킬 수 없는 치명적인 신경 독성 사례가 1건 보고되었다.[75]
다발성 골수종에 대한 BCMA-키메라 항원 수용체(CAR) T 세포 치료법을 사용한 경우 운동 저하 장애(파킨슨증, 또는 운동 및 신경인지 치료 발생 이상 반응)가 관찰되었다.[76]
CAR-T 세포 치료는 독특하고 유망한 암 치료법이지만, 심각한 안전상의 우려가 남아있다. 건강한 조직에서 종양 세포와 동일한 항원을 가진 경우 공격 대상이 되어, 이식편대숙주병(GVHD)과 유사한 결과를 초래한다. 이 문제는 자살 유전자를 CAR-T 세포에 도입함으로써 해결할 수 있다. 프로드럭 투여에 의해 자살 유전자가 활동하도록 설계하여, GVHD가 발생하면 CAR-T 세포가 아폽토시스에 의해 사멸하도록 할 수 있다.
6. CAR-T 디자인의 진화
CAR(키메라 항원 수용체) 디자인은 T 세포의 활성, 증식, 지속성 및 항종양 효과를 향상시키기 위해 여러 세대에 걸쳐 발전해왔다.
- 1세대 CAR: T 세포 활성화 신호를 전달하는 CD3ζ 세포질 도메인만을 포함한다.[3]
- 2세대 CAR: CD28 또는 4-1BB와 같은 공동 자극 도메인을 추가하여 T 세포 증식, 사이토카인 분비, 세포 사멸 저항성 및 생체 내 지속성을 향상시켰다.[3]
- 3세대 CAR: CD28-4-1BB 또는 CD28-CD134(OX40)과 같이 여러 공동 자극 도메인을 결합하여 T 세포 활성을 더욱 증강시켰다. 전임상 데이터에 따르면 3세대 CAR는 2세대 CAR에 비해 향상된 이펙터 기능과 더 나은 생체 내 지속성을 나타낸다.[3]
- 4세대 CAR (TRUCK): T 세포 증식, 지속성 및 항종양 활성을 향상시키는 사이토카인(IL-2, IL-15, IL-12 등) 또는 보조 자극 리간드를 추가로 발현한다.
이 외에도, 다음과 같은 새로운 기술들이 개발되고 있다.
- Prime CAR-T 세포: IL-7과 CCL19를 동시에 생성하여 고형암에 대한 숙주의 면역 반응을 활성화한다.[135][136]
- SMDC 어댑터 기술: FITC 등의 소분자에 대한 친화성을 높여 다양한 종류의 암에 사용될 수 있도록 한다.[94][95]
- 기타: 톨 유사 수용체 4(TLR4) 신호 구성 요소를 CAR 구조에 통합하거나, Src 계열 키나제의 일원인 FYN 키나제를 통합하여 CAR-T 세포 내 신호 전달 연쇄 반응을 개선하는 등 대체 활성 도메인에 초점을 맞춘 발전이 이루어지고 있다. KIR 기반 CAR (KIR-CAR)는 T 세포 증식 및 항종양 활성이 향상된 것으로 나타났다.
이러한 CAR 디자인의 발전은 CAR-T 세포 치료법의 효능을 높이고, 부작용을 줄이며, 더 넓은 범위의 암에 적용할 수 있도록 하는 데 기여하고 있다.
6. 1. 제어 메커니즘
CAR-T 세포 치료의 부작용을 줄이기 위해, 공학적으로 조작된 T 세포에 합성 제어 기전을 추가하여 의사가 환자 체내에서 T 세포의 지속성 또는 활성을 정밀하게 제어할 수 있다.[98] 주요 제어 기술에는 T 세포 사멸을 유발하거나 T 세포 활성화를 제한하는 방법이 있으며, 필요에 따라 투여하거나 보류할 수 있는 별도의 약물을 통해 T 세포를 조절한다.- '''자살 유전자''': 유전자 변형된 T 세포에 세포 외 분자에 의해 활성화될 때 세포 사멸을 유도하는 유전자를 삽입한다. 헤르페스 단순 바이러스 티미딘 키나아제(HSV-TK)와 유도성 카스파제 9(iCasp9)가 CAR-T 세포에 통합되는 대표적인 자살 유전자이다.[98][99][100] iCasp9 시스템은 작은 분자 rimiducid/AP1903에 대한 높은 특이성을 가진 변이된 FK506 결합 단백질과 프로-도메인이 제거된 인간 카스파제 9을 암호화하는 유전자로 구성된다. 환자에게 rimiducid를 투여하면 자살 시스템이 활성화되어 유전자 변형된 T 세포가 빠르게 사멸한다. HSV-TK와 iCasp9 시스템 모두 임상 시험에서 안전 스위치로서의 기능을 보였지만, HSV-TK는 바이러스 유래이므로 인간에게 면역원성이 있을 수 있다는 한계가 있다.[98][101]
- '''이중 항원 수용체''': CAR-T 세포가 두 개의 종양 관련 항원 수용체를 동시에 발현하도록 조작하여, T 세포가 비종양 세포를 공격할 가능성을 줄인다. 이중 항원 수용체 CAR-T 세포는 부작용의 강도가 덜한 것으로 보고되었다.[102]
7. 경제성
키메라 항원 수용체 T 세포 (CAR-T) 치료는 복잡한 제조 과정과 높은 수준의 병원 치료가 필요하여 비용이 매우 높다. 티사젠렉류셀 (킴리아)과 악시캅타젠 실로류셀 (예스카타)의 초기 비용은 각각 475000USD와 375000USD였다.[123] 미국에서는 CAR-T 세포 치료가 메디케어 및 일부 민간 보험사에 의해 보장된다.[124][125] CAR-T 세포 제조업체는 치료 후 특정 시점까지 완전 관해를 유도하는 경우에만 지불을 요구하는 등 대체 지불 프로그램을 개발했다.[126]
8. 한국의 현황 및 전망
한국에서는 키메라 항원 수용체 T 세포(CAR-T) 치료제 개발 및 임상 연구가 활발하게 진행되고 있으며, 식품의약품안전처의 허가를 받은 치료제도 출시되고 있다. 더불어민주당은 CAR-T 세포 치료와 같은 첨단 바이오 의약품에 대한 환자 접근성 확대를 위해 건강보험 적용 범위를 넓히고, 관련 연구 개발을 지원하는 정책을 추진하고 있다.
국내 제약 회사 및 바이오 벤처 기업들은 차세대 CAR-T 세포 치료제 개발에 주력하고 있으며, 고형암, 자가면역질환 등 다양한 질환으로 적응증을 확대하기 위한 연구를 진행하고 있다. CAR-T 세포 치료가 널리 보급되기 위해서는 높은 치료 비용, 생산 과정의 복잡성, 부작용 관리 등의 문제를 해결해야 하며, 이를 위해 정부, 의료계, 산업계의 협력이 필요하다.
참조
[1]
웹사이트
New Gene Therapy for Cancer Offers Hope to Those With No Options Left
https://www.nbcnews.[...]
2017-07-12
[2]
논문
Engineering CAR-T cells: Design concepts
2015-08
[3]
논문
Clinical development of CAR T cells-challenges and opportunities in translating innovative treatment concepts
2017-09
[4]
논문
Therapeutic potential of CAR-T cell-derived exosomes: a cell-free modality for targeted cancer therapy
2015-12
[5]
논문
Engineering better chimeric antigen receptor T cells
2020-12
[6]
논문
Expression of chimeric receptor composed of immunoglobulin-derived V regions and T-cell receptor-derived C regions
1987-12
[7]
논문
Generation of effector T cells expressing chimeric T cell receptor with antibody type-specificity
1989-02
[8]
논문
Tragedy, Perseverance, and Chance - The Story of CAR-T Therapy
2017-10
[9]
논문
Expression of immunoglobulin-T-cell receptor chimeric molecules as functional receptors with antibody-type specificity
1989-12
[10]
논문
The T-body approach: potential for cancer immunotherapy
1996
[11]
논문
The cytoplasmic domain of the T cell receptor zeta chain is sufficient to couple to receptor-associated signal transduction pathways
1991-03
[12]
논문
T-cell gene therapy
1996-12
[13]
논문
Chimeric Antigen Receptor Therapy
2018-07
[14]
논문
The long road to the first FDA-approved gene therapy: chimeric antigen receptor T cells targeting CD19
2020-02
[15]
논문
Targeting tumours with genetically enhanced T lymphocytes
2003-01
[16]
논문
Approved Cellular and Gene Therapy Products
https://www.fda.gov/[...]
2022-03-01
[17]
논문
Allogeneic lymphocyte-licensed DCs expand T cells with improved antitumor activity and resistance to oxidative stress and immunosuppressive factors
2014-03-05
[18]
서적
Single-Domain Antibodies
2022
[19]
논문
Clinical development of anti-CD19 chimeric antigen receptor T-cell therapy for B-cell non-Hodgkin lymphoma
2017-06
[20]
논문
Safe engineering of CAR T cells for adoptive cell therapy of cancer using long-term episomal gene transfer
2016-07
[21]
논문
Therapeutic gene editing in haematological disorders with CRISPR/Cas9
2019-06
[22]
논문
Increased intensity lymphodepletion and adoptive immunotherapy--how far can we go?
2006-12
[23]
논문
The global pipeline of cell therapies for cancer
2019-10
[24]
논문
Chimeric antigen receptor T cell therapies for lymphoma
Nature Reviews Clinical Oncology
2018
[25]
논문
Chimeric antigen receptor T-cell therapies for multiple myeloma
Blood
2017
[26]
논문
CAR T Cell Therapy: A Game Changer in Cancer Treatment
2016
[27]
논문
Time to put the CAR-T before the horse
2011-11
[28]
논문
Advances in immunotherapeutic targets for childhood cancers: A focus on glypican-2 and B7-H3
2021-07
[29]
논문
Immunotherapy for hepatobiliary cancers: Emerging targets and translational advances
https://pubmed.ncbi.[...]
2022
[30]
논문
Eradication of B-lineage cells and regression of lymphoma in a patient treated with autologous T cells genetically engineered to recognize CD19
2010-11
[31]
논문
Chemotherapy-refractory diffuse large B-cell lymphoma and indolent B-cell malignancies can be effectively treated with autologous T cells expressing an anti-CD19 chimeric antigen receptor
2015-02
[32]
논문
Driving CAR T cell translation forward
2019-02
[33]
논문
Intraventricular CARv3-TEAM-E T Cells in Recurrent Glioblastoma
http://www.nejm.org/[...]
2024-04-11
[34]
논문
The Principles of Engineering Immune Cells to Treat Cancer
2017-02
[35]
논문
Therapeutically targeting glypican-2 via single-domain antibody-based chimeric antigen receptors and immunotoxins in neuroblastoma
2017-08-08
[36]
논문
CAR T cells targeting tumor-associated exons of glypican 2 regress neuroblastoma in mice
2021-06-15
[37]
논문
Regulatory T cells and immune tolerance
2008-05
[38]
논문
Chimeric Antigen Receptor (CAR) Treg: A Promising Approach to Inducing Immunological Tolerance
[39]
논문
CD19-Targeted CAR T Cells in Refractory Systemic Lupus Erythematosus
2021-08
[40]
웹사이트
Novartis receives first ever FDA approval for a CAR-T cell therapy, Kymriah(TM) (CTL019), for children and young adults with B-cell ALL that is refractory or has relapsed at least twice
https://www.novartis[...]
2017-08-30
[41]
웹사이트
Novartis receives European Commission approval of its CAR-T cell therapy, Kymriah® (tisagenlecleucel)
https://www.novartis[...]
2023-11-18
[42]
웹사이트
Novartis gets approval to sell Kymriah in Japan for $306,000
https://www.reuters.[...]
2019-05-15
[43]
웹사이트
KYMRIAH (tisagenlecleucel)
https://www.fda.gov/[...]
2019-04-05
[44]
웹사이트
FDA approves Novartis Kymriah® CAR-T cell therapy for adult patients with relapsed or refractory follicular lymphoma
https://www.novartis[...]
2022-06-05
[45]
웹사이트
Novartis Kymriah® receives EC approval as first CAR-T cell therapy for adults with relapsed or refractory follicular lymphoma
https://www.novartis[...]
2023-11-18
[46]
논문
FDA approves CAR-T cell therapy to treat adults with certain types of large B-cell lymphoma
https://www.fda.gov/[...]
2017-10-18
[47]
웹사이트
Yescarta® (Axicabtagene Ciloleucel) Receives European Marketing Authorization for the Treatment of Relapsed or Refractory DLBCL and PMBCL, After Two or More Lines of Systemic Therapy
https://www.gilead.c[...]
2023-11-18
[48]
웹사이트
Kite Joint Venture - Fosun Kite - Gains the First CAR T-cell Therapy Approval in China
https://www.gilead.c[...]
2023-11-13
[49]
웹사이트
Yescarta® Now Approved in Japan for Initial Treatment of Relapsed/Refractory Large B-Cell Lymphoma
https://www.gilead.c[...]
2022-12-22
[50]
논문
YESCARTA (axicabtagene ciloleucel)
https://www.fda.gov/[...]
2020-05-28
[51]
웹사이트
Kite's CAR T-cell Therapy Yescarta® First in Europe to Receive Positive CHMP Opinion for Use in Second-line Diffuse Large B-cell Lymphoma and High-grade B-cell Lymphoma
https://www.gilead.c[...]
2023-11-18
[52]
웹사이트
U.S. FDA Approves Yescarta® for Relapsed or Refractory Follicular Lymphoma After Two or More Lines of Systemic Therapy
https://www.gilead.c[...]
2021-03-15
[53]
웹사이트
Kite's CAR T-cell Therapy Yescarta® Granted European Marketing Authorization for the Treatment of Relapsed or Refractory Follicular Lymphoma
https://www.gilead.c[...]
2023-11-18
[54]
논문
TECARTUS (brexucabtagene autoleucel)
https://www.fda.gov/[...]
2021-03-04
[55]
논문
TECARTUS (brexucabtagene autoleucel)
https://www.ema.euro[...]
2023-01-30
[56]
논문
TECARTUS (brexucabtagene autoleucel)
https://www.fda.gov/[...]
2021-03-04
[57]
웹사이트
U.S. Food and Drug Administration Approves Bristol Myers Squibb's Breyanzi (lisocabtagene maraleucel), a New CAR T Cell Therapy for Adults with Relapsed or Refractory Large B-cell Lymphoma
https://news.bms.com[...]
2023-11-21
[58]
논문
Breyanzi
https://www.ema.euro[...]
2023-11-10
[59]
웹사이트
CAR T Cell Therapy Breyanzi® Approved as Relapsed or Refractory Large B-cell Lymphoma Second-Line Therapy in Japan
https://news.bms.com[...]
[60]
논문
FDA D.I.S.C.O. Burst Edition: FDA approval of Breyanzi (lisocabtagene maraleucel) for second-line treatment of large B-cell lymphoma
https://www.fda.gov/[...]
2022-06-24
[61]
논문
Abecma
https://www.ema.euro[...]
2023-07-27
[62]
논문
ABECMA (idecabtagene vicleucel)
https://www.fda.gov/[...]
2021-03-27
[63]
논문
Carvykti
https://www.ema.euro[...]
2023-07-27
[64]
논문
CARVYKTI
https://www.fda.gov/[...]
2022-03-21
[65]
논문
FDA approves obecabtagene autoleucel for adults with relapsed or refractory B-cell precursor acute lymphoblastic leukemia
https://www.fda.gov/[...]
2024-11-08
[66]
논문
Toxicity and management in CAR T-cell therapy
2016
[67]
논문
CAR-T cell therapy and infection: a review
2021-06
[68]
논문
Cytokine-release syndrome: overview and nursing implications
2007-02
[69]
논문
Current concepts in the diagnosis and management of cytokine release syndrome
2014-07
[70]
논문
Regulatory Measures to Improve the Safety of CAR-T-Cell Treatment
2022-11-29
[71]
논문
Preemptive mitigation of CD19 CAR T-cell cytokine release syndrome without attenuation of antileukemic efficacy
2019-12
[72]
논문
Chimeric antigen receptor-T cells with cytokine neutralizing capacity
2020-04
[73]
논문
Toxicities of chimeric antigen receptor T cells: recognition and management
2016-06
[74]
뉴스
Study Evaluating the Efficacy and Safety of JCAR015 in Adult B-cell Acute Lymphoblastic Leukemia (B-ALL)
https://clinicaltria[...]
2018-02-21
[75]
논문
CD19 CAR-T cells of defined CD4+:CD8+ composition in adult B cell ALL patients
2016-06
[76]
논문
BCMA-CAR T-cell treatment–associated parkinsonism
https://ashpublicati[...]
2023-10-05
[77]
논문
T cell receptor-based cancer immunotherapy: Emerging efficacy and pathways of resistance
2019-07
[78]
논문
Design and development of therapies using chimeric antigen receptor-expressing T cells
2014-01
[79]
논문
Engineering CAR-T cells
2017-06-24
[80]
논문
Chimeric fusion proteins used for therapy: indications, mechanisms, and safety
2015-05
[81]
논문
Therapeutically targeting glypican-2 via single-domain antibody-based chimeric antigen receptors and immunotoxins in neuroblastoma
2017-08
[82]
논문
Persistent Polyfunctional Chimeric Antigen Receptor T Cells That Target Glypican 3 Eliminate Orthotopic Hepatocellular Carcinomas in Mice
2020-06
[83]
논문
The IgG4 hinge with CD28 transmembrane domain improves VHH-based CAR T cells targeting a membrane-distal epitope of GPC1 in pancreatic cancer
2023-04-08
[84]
논문
Human VH-based chimeric antigen receptor T cells targeting glypican 3 eliminate tumors in preclinical models of HCC
2023-02-01
[85]
논문
A novel PD-L1-targeted shark VNAR single-domain-based CAR-T cell strategy for treating breast cancer and liver cancer
2022-03-17
[86]
논문
The nonsignaling extracellular spacer domain of chimeric antigen receptors is decisive for in vivo antitumor activity
2015-02
[87]
논문
Incorporation of a hinge domain improves the expansion of chimeric antigen receptor T cells
2017-03
[88]
논문
The optimal antigen response of chimeric antigen receptors harboring the CD3zeta transmembrane domain is dependent upon incorporation of the receptor into the endogenous TCR/CD3 complex
2010-06
[89]
논문
Suicide gene therapy to increase the safety of chimeric antigen receptor-redirected T lymphocytes
[90]
논문
The basic principles of chimeric antigen receptor design
2013-04
[91]
간행물
A Cure for Cancer? How CAR-T Therapy is Revolutionizing Oncology.
https://labiotech.eu[...]
labiotech
2018-03-08
[92]
논문
Engineering T Cells to Treat Cancer: The Convergence of Immuno-Oncology and Synthetic Biology
[93]
논문
Universal Chimeric Antigen Receptors for Multiplexed and Logical Control of T Cell Responses
2018-05
[94]
웹사이트
SMDC technology
http://endocyte.com/[...]
2016-03-27
[95]
간행물
Endocyte announces promising preclinical data for application of SMDC technology in CAR T cell therapy in late-breaking abstract at American Association for Cancer Research (AACR) annual meeting 2016
http://investor.endo[...]
Endocyte
2016-04-19
[96]
논문
CD19 CAR T Cells Expressing IL-12 Eradicate Lymphoma in Fully Lymphoreplete Mice through Induction of Host Immunity
2018-03
[97]
논문
TRUCKs: the fourth generation of CARs
2015
[98]
논문
A new insight in chimeric antigen receptor-engineered T cells for cancer immunotherapy
2017-01
[99]
논문
HSV-TK gene transfer into donor lymphocytes for control of allogeneic graft-versus-leukemia
1997-06
[100]
논문
Co-expression of cytokine and suicide genes to enhance the activity and safety of tumor-specific cytotoxic T lymphocytes
2007-10
[101]
논문
T-cell mediated rejection of gene-modified HIV-specific cytotoxic T lymphocytes in HIV-infected patients
1996-02
[102]
논문
Human T-lymphocyte cytotoxicity and proliferation directed by a single chimeric TCRzeta /CD28 receptor
2002-01
[103]
논문
Dual targeting of ErbB2 and MUC1 in breast cancer using chimeric antigen receptors engineered to provide complementary signaling
2012-10
[104]
논문
Remote control of therapeutic T cells through a small molecule-gated chimeric receptor
2015-10
[105]
논문
Targeting T cells to tumor cells using bispecific antibodies
2013-06
[106]
논문
Anti-CD20/CD3 T cell-dependent bispecific antibody for the treatment of B cell malignancies
2015-05
[107]
논문
Bispecific small molecule-antibody conjugate targeting prostate cancer
2013-10
[108]
논문
In situ programming of leukaemia-specific T cells using synthetic DNA nanocarriers
http://dx.doi.org/10[...]
2017-04-17
[109]
논문
"In vivo" generated human CAR T cells eradicate tumor cells
http://dx.doi.org/10[...]
2019-10-10
[110]
논문
Bioinstructive implantable scaffolds for rapid in vivo manufacture and release of CAR-T cells
http://dx.doi.org/10[...]
2022-03-24
[111]
논문
Rapid manufacturing of non-activated potent CAR T cells
2022-02
[112]
논문
Cancer-fighting CAR-T cells could be made inside body with viral injection
https://www.nature.c[...]
2023-12-20
[113]
논문
Application of toll-like receptors (TLRs) and their agonists in cancer vaccines and immunotherapy
2023-10-23
[114]
논문
Toll-like receptor 4 signaling activation domains promote CAR T cell function against solid tumors
https://doi.org/10.1[...]
2024-06
[115]
논문
The critical role of Toll-like receptor-mediated signaling in cancer immunotherapy
2022-06-01
[116]
논문
CD28-CAR-T cell activation through FYN kinase signaling rather than LCK enhances therapeutic performance
2023-02-21
[117]
논문
Generation of Potent T-cell Immunotherapy for Cancer using DAP12-based, Multichain, Chimeric Immunoreceptors
2015-07
[118]
웹사이트
First-in-Human Trial to Assess KIR-CAR T-Cell Therapy in MSLN+ Solid Tumors
https://www.cgtlive.[...]
2024-06-05
[119]
논문
152. A Chimeric Antigen Receptor (CARs) Based Upon a Killer Immunoglobulin-Like Receptor (KIR) Triggers Robust Cytotoxic Activity in Solid Tumors
2014-05
[120]
논문
Abstract 6332: Evaluating the relationship of affinity, functional avidity, and in vivo potency in KIR-CAR T cells
https://aacrjournals[...]
2024-03-22
[121]
논문
MyD88/CD40 signaling retains CAR T cells in a less differentiated state
2020-11-05
[122]
논문
Constitutively active MyD88/CD40 costimulation enhances expansion and efficacy of chimeric antigen receptor T cells targeting hematological malignancies
2019-09
[123]
논문
Economic Evaluation of Chimeric Antigen Receptor T-Cell Therapy by Site of Care Among Patients With Relapsed or Refractory Large B-Cell Lymphoma
2020-04
[124]
웹사이트
Decision Memo for Chimeric Antigen Receptor (CAR) T-cell Therapy for Cancers (CAG-00451N)
https://www.cms.gov/[...]
2021-03-22
[125]
웹사이트
CAR T-cell Therapy: An Update on Coverage and Reimbursement - Hematology.org
https://www.hematolo[...]
2021-03-22
[126]
논문
Value and affordability of CAR T-cell therapy in the United States
2020-09
[127]
웹사이트
Which countries is CAR T-cell therapy available in? {{!}} SingleUseSupport
https://www.susuppor[...]
SingleUseSupport
2022-05-13
[128]
웹사이트
Anvisa aprova produto de terapia avançada para tratamento de câncer
https://www.gov.br/a[...]
2022-06-07
[129]
웹사이트
키메라항원수용체(CAR)를 이용한 유전자 개변T세포 요법
http://s-igaku.umin.[...]
信州医学会
2018-02-10
[130]
논문
Expression of chimeric receptor composed of immunoglobulin-derived V regions and T-cell receptor-derived C regions
1987-12
[131]
웹사이트
Historic 'living drug' gets go-ahead
http://www.bbc.co.uk[...]
BBC
2017-08-30
[132]
웹사이트
genome-editing-save-girl
https://gigazine.net[...]
[133]
논문
Artificial T-cell receptors
[134]
웹사이트
DGXMZO18653040Z00C17A7X11000
https://www.nikkei.c[...]
[135]
웹사이트
release_20180306-02
https://www.amed.go.[...]
[136]
간행물
IL-7 and CCL19 expression in CAR-T cells improves immune cell infiltration and CAR-T cell survival in the tumor.
2018-04
[137]
논문
Therapeutic gene editing in haematological disorders with CRISPR/Cas9
2019-06
[138]
웹인용
광범위큰B세포림프종에 대한 키메릭항원수용체T세포 (Chimeric Antigen Receptor T-cells) 치료
http://ekjm.org/jour[...]
[139]
논문
Engineering CAR-T cells
https://doi.org/10.1[...]
2017
[140]
웹사이트
The Transmembrane Spacer Domain CAR Design
https://www.creative[...]
[141]
논문
Signals through T cell receptor-zeta chain alone are insufficient to prime resting T lymphocytes.
J Exp Med
1995-05-01
[142]
논문
Chimeric Fv-zeta or Fv-epsilon receptors are not sufficient to induce activation or cytokine production in peripheral T cells.
Blood
2000
[143]
논문
Cytokine-induced killer cells for cell therapy of acute myeloid leukemia:improvement of their immune activity by expression of CD33-specificchimeric receptors.
Haematologica
2010
[144]
논문
TRUCKs: the fourth generation o어려운ㅇㅇf CARs.
ExpertOpin Biol Ther
2015
[145]
웹인용
광범위큰B세포림프종에 대한 키메릭항원수용체T세포 (Chimeric Antigen Receptor T-cells) 치료
http://ekjm.org/jour[...]
[146]
논문
Adaptive cell transfer as personalized immunotherapy for human cancer
[147]
웹인용
키메라 항원 수용체(Chimeric Antigen Receptor, CAR)기반 항암면역 T세포치료제
http://nov.ncc.re.kr[...]
2020-07-19
[148]
저널
An introduction to chimeric antigen receptor (CAR) T-cell immunotherapy for human cancer
[149]
저널
Chimeric antigen receptor (CAR)-modified NK cells against cancer: Opportunities and challenges
[150]
저널
Chimeric Antigen Receptor T-Cell Therapy: Reach to Solid Tumor Experience
본 사이트는 AI가 위키백과와 뉴스 기사,정부 간행물,학술 논문등을 바탕으로 정보를 가공하여 제공하는 백과사전형 서비스입니다.
모든 문서는 AI에 의해 자동 생성되며, CC BY-SA 4.0 라이선스에 따라 이용할 수 있습니다.
하지만, 위키백과나 뉴스 기사 자체에 오류, 부정확한 정보, 또는 가짜 뉴스가 포함될 수 있으며, AI는 이러한 내용을 완벽하게 걸러내지 못할 수 있습니다.
따라서 제공되는 정보에 일부 오류나 편향이 있을 수 있으므로, 중요한 정보는 반드시 다른 출처를 통해 교차 검증하시기 바랍니다.
문의하기 : help@durumis.com