레트로트랜스포존
"오늘의AI위키"의 AI를 통해 더욱 풍부하고 폭넓은 지식 경험을 누리세요.
1. 개요
레트로트랜스포존은 레트로바이러스와 유사하게 역전사 효소를 사용하여 RNA를 DNA로 전사하고, 숙주 게놈에 삽입하는 이동성 유전 요소이다. LTR 레트로트랜스포존과 Non-LTR 레트로트랜스포존으로 나뉘며, LTR 레트로트랜스포존은 긴 말단 반복 서열을, Non-LTR 레트로트랜스포존은 LINE, SINE, SVA 요소 등으로 구성된다. 레트로트랜스포존은 유전자 발현 변화, 파괴 등을 유발하여 암, 신경 질환 등 다양한 질병과 관련 있으며, 유전체 진화에 중요한 역할을 한다. 레트로트랜스포존은 RNA 간섭에 의해 조절되며, 유전자 비활성화, 조절 변경, DNA 복구 부위 역할 등의 돌연변이를 유발한다.
더 읽어볼만한 페이지
- 비부호화 DNA - 텔로미어
텔로미어는 진핵세포 염색체 말단에서 염색체 안정성을 유지하고 DNA 손상을 방지하는 반복적인 DNA 서열과 단백질 복합체로, 세포 분열 시 짧아져 노화와 관련되며 텔로머레이스 효소에 의해 유지될 수 있다는 연구로 노벨상을 수상했다. - 비부호화 DNA - 인트론
진핵생물 유전자에서 엑손 사이에 존재하는 비코딩 DNA 서열인 인트론은 스플라이싱 과정을 거쳐 제거되며 유전자 발현 조절, 선택적 스플라이싱 등 다양한 기능에 관여하는 것으로 여겨진다. - 분자생물학 - 단백질
단백질은 아미노산 중합체로 생체 구조 유지와 기능에 필수적이며, 아미노산 서열에 따라 고유한 3차원 구조를 형성하여 효소, 구조, 수송, 저장, 수축, 방어, 조절 단백질 등 다양한 기능을 수행하고, 인체 내에서 건강 유지와 질병 예방에 중요한 역할을 하는 필수 영양소이다. - 분자생물학 - 의학
의학은 질병의 진단, 예후, 치료, 예방을 연구하는 과학 및 실천 분야이며, 고대부터 발전하여 현대에는 다양한 전문 분야로 세분화되고 첨단 기술 발전에 따라 혁신적인 변화를 겪고 있다.
2. 레트로트랜스포존의 종류
레트로트랜스포존은 구조적 특징, 특히 긴 말단 반복 서열(Long Terminal Repeat, LTR)의 유무에 따라 크게 두 가지 주요 유형으로 나뉜다.
- LTR 레트로트랜스포존: 서열의 양쪽 끝에 LTR이라는 긴 반복 서열을 가진다. 이들은 레트로바이러스와 유사한 방식으로 작동하는 경우가 많다.
- Non-LTR 레트로트랜스포존: LTR 서열이 없다. 대신 다른 종류의 반복 서열을 가질 수 있으며, 전위 메커니즘도 LTR 레트로트랜스포존과 다르다.[12] Non-LTR 레트로트랜스포존은 주로 LINE(Long Interspersed Nuclear Element)과 SINE(Short Interspersed Nuclear Element)으로 나뉜다. SVA 요소는 LINE과 SINE의 특징을 일부 공유하는 또 다른 유형이다.
2. 1. LTR 레트로트랜스포존
LTR 레트로트랜스포존은 양쪽 말단에 긴 말단 반복 서열 (Long Terminal Repeat, LTR)이라는 특징적인 서열을 가진다. 이 LTR 서열의 길이는 보통 `100bp`에서 `5kb` 정도이며, 때로는 `1000bp`를 넘기도 한다.[9] LTR에는 전이성 요소(TE)의 전사를 조절하는 프로모터가 포함되어 있으며, 요소가 게놈에 삽입되는 과정에 필수적이다. LTR 레트로트랜스포존 전체의 크기는 평균적으로 수천 염기쌍(kb)에 달하며, 큰 것은 `30kb`에 이르기도 한다.LTR 레트로트랜스포존은 서열 유사성과 암호화하는 유전자의 순서에 따라 크게 Ty1-copia 유사 그룹(Pseudoviridae), Ty3-gypsy 유사 그룹(Metaviridae), 그리고 BEL-Pao 유사 그룹으로 분류된다.[8][9] 특히 식물 게놈, 그중에서도 게놈 크기가 큰 식물에서는 Ty1-copia군과 Ty3-gypsy군 레트로트랜스포존이 매우 많은 수(수백만 복제본까지)로 발견된다. Ty1-copia군은 단세포 조류부터 선태식물, 겉씨식물, 피자식물까지 다양한 식물 종에서 흔하게 발견되며, Ty3-gypsy군 역시 겉씨식물과 피자식물을 포함하여 넓게 분포한다. 인간 게놈의 약 8%는 LTR 레트로트랜스포존으로 구성되어 있다.
LTR 레트로트랜스포존은 비 LTR 레트로트랜스포존과 역전사 및 게놈 통합 메커니즘에서 차이를 보인다. 비 LTR 레트로트랜스포존이 표적-프라이밍 역전사(TPRT) 방식을 사용하는 반면, LTR 레트로트랜스포존은 세포질에서 먼저 역전사를 거쳐 이중 가닥 DNA를 만든다. 이 DNA는 인테그라제 단백질과 함께 사전 통합 복합체(pre-integration complex, PIC)를 형성한 후, 세포핵 안으로 이동하여 새로운 게놈 위치에 삽입된다.
LTR 레트로트랜스포존은 일반적으로 레트로바이러스와 유사하게 gag 단백질과 pol 단백질을 암호화한다. gag 단백질은 바이러스 입자(캡시드) 조립과 RNA 및 관련 단백질 패키징에 관여한다. pol 단백질은 역전사에 필요한 여러 효소 활성(프로테아제(PR), 역전사 효소(RT), RNase H(RH), 인테그라제(INT))을 가진다. 일부 LTR 레트로트랜스포존은 추가적으로 외피 단백질을 암호화하는 env 유전자를 가지기도 하는데, 이는 세포 표면 부착을 돕고 내생 레트로바이러스와 관련이 있다.[10] env 유전자의 존재 여부는 레트로바이러스와 레트로트랜스포존을 구분하는 중요한 특징 중 하나이다.
2. 1. 1. 내생 레트로바이러스
내생 레트로바이러스는 레트로바이러스가 숙주 게놈에 통합되어 다음 세대로 유전될 수 있는 형태로, 바이러스로서의 병원성 효과는 없다.[9] 이 때문에 내생 레트로바이러스는 레트로바이러스와 레트로트랜스포존의 특징을 모두 공유한다. 레트로바이러스의 DNA가 숙주 게놈에 통합되면, 시간이 지나면서 내생 레트로바이러스로 진화하여 진핵생물 게놈의 일부가 된다. 많은 내생 레트로바이러스가 진핵생물 게놈에 삽입되어 있으며, 이는 바이러스-숙주 상호작용, 진화 과정, 그리고 질병 발생 메커니즘에서 레트로트랜스포존의 역할을 이해하는 데 중요한 통찰력을 제공한다.많은 레트로트랜스포존 역시 숙주 게놈을 인식하고 융합하는 특성을 가지므로 내생 레트로바이러스와 유사한 특징을 보인다. 그러나 레트로바이러스와 레트로트랜스포존 사이에는 결정적인 차이가 있는데, 바로 env 유전자의 존재 여부이다. 이 유전자는 레트로바이러스가 숙주 세포로 침투하는 데 필요한 외피 당단백질을 암호화한다. env 유전자를 가진 레트로바이러스는 세포 간 이동이 가능하지만, 대부분의 LTR 레트로트랜스포존은 env 유전자가 없어 동일한 세포 내의 게놈으로만 이동할 수 있다.[10] 어떤 요소가 레트로바이러스인지 레트로트랜스포존인지는 주로 env 유전자의 유무와 pol 유전자의 서열 순서 차이로 구분된다. 일부 LTR 레트로트랜스포존 유형, 예를 들어 Ty1-copia (Pseudoviridae), Ty3-gypsy (Metaviridae), BEL/Pao 등에서는 env 유전자가 발견되기도 한다.[8][9]
척추동물의 많은 유전자는 과거 레트로바이러스나 LTR 레트로트랜스포존으로부터 유래된 것으로 여겨진다. 특정 내생 레트로바이러스나 LTR 레트로트랜스포존이 서로 다른 종에서 동일한 기능과 게놈 상의 위치를 가지는 경우가 있는데, 이는 이들이 생명체의 진화 과정에서 중요한 역할을 했음을 시사한다.[11]
2. 2. Non-LTR 레트로트랜스포존
Non-LTR 레트로트랜스포존은 이름 그대로 LTR(long terminal repeat) 서열이 없는 레트로트랜스포존이다. 이들은 주로 LINE(Long Interspersed Nuclear Element)과 SINE(Short Interspersed Nuclear Element)의 두 종류로 나뉜다. Non-LTR 레트로트랜스포존은 진핵생물의 게놈에 널리 퍼져 있으며, 특히 식물 게놈에서 많은 복사본이 발견된다.Non-LTR 레트로트랜스포존은 구조적으로 역전사 효소, RNA 결합 단백질, 뉴클레이스, 때로는 리보뉴클레아제 H 도메인에 대한 유전자를 포함하지만, LTR 서열은 없다.[12] LTR 대신 짧은 반복 서열을 가지며, 이는 LTR 레트로트랜스포존에서 발견되는 직접 반복과는 다르다.
LINE은 전위에 필요한 역전사 효소, 엔도뉴클레이스 등의 단백질과 리보핵산단백질 형성을 위한 핵산 결합 단백질을 암호화하는 두 개의 ORF(Open Reading Frame)를 가지고 있다. 반면, SINE은 자체적으로 전위 효소를 만들지 못하고 LINE이 만든 효소와 기능들에 의존하여 게놈 내에서 이동한다.
또한, SVA 요소는 LINE과 SINE의 특징을 모두 가지는 예외적인 형태로 존재한다. 길이는 LINE보다 짧지만 SINE보다는 길다.
Non-LTR 레트로트랜스포존은 LTR 레트로트랜스포존과 마찬가지로 RNA 중간체를 통해 전위하지만, tRNA에 결합하는 서열이 없기 때문에 역전사 과정의 세부 메커니즘은 다르다.
과거에는 이들 서열이 기능이 없는 "정크 DNA"로 여겨지기도 했으나, 최근 연구에 따르면 일부 LINE과 SINE 요소가 새로운 유전자에 통합되어 새로운 기능을 형성하는 데 기여했을 가능성이 제기되었다.[13]
2. 2. 1. LINE (Long Interspersed Nuclear Element)
Non-LTR 레트로트랜스포존은 긴 산재 핵 요소(LINE, Long Interspersed Nuclear Element)와 짧은 산재 핵 요소(SINE, Short Interspersed Nuclear Element)로 나뉜다. LINE은 전위에 필요한 단백질을 암호화하는 두 개의 오픈 리딩 프레임(ORF)를 가지며, 이들은 역전사 효소, 엔도뉴클레이스 활성을 가지거나 리보핵산단백질(RNP) 형성을 위한 핵산 결합 단백질 등을 포함한다. 반면 SINE은 자체 전위 능력이 없어 LINE이 만든 효소에 의존한다.LINE이 전사될 때 만들어지는 전사체는 RNA 중합효소 II 프로모터를 포함한다. 전사체의 3' 말단에는 폴리A 꼬리처럼 아데닌(A) 염기가 다수 추가되어[14] 안정성을 높이며, 이는 RNA 전위 중간체 역할을 한다. 이 RNA 중간체는 핵 밖 세포질로 이동하여 번역 과정을 거쳐 ORF1, ORF2 단백질을 만든다. 생성된 단백질은 다시 RNA 중간체와 결합하여 복합체를 형성한 뒤, 게놈에 삽입되기 위해 핵 안으로 이동한다.
LINE은 주로 AT 염기쌍이 풍부한 게놈 영역에 삽입된다. 삽입 과정에서 LINE이 암호화한 엔도뉴클레이스는 표적 DNA의 한 가닥을 절단한다. LINE RNA의 아데닌 풍부 꼬리가 절단된 DNA 가닥의 상보적인 티민(T) 염기와 결합하고, 노출된 수산기(-OH)를 시작점으로 역전사 효소가 RNA를 주형으로 사용하여 LINE 서열을 DNA로 합성해 삽입한다. 새로 삽입된 LINE은 다른 게놈 영역으로 다시 복사되어 삽입될 수 있으며, 이 과정에서 인접한 숙주 게놈 서열이 함께 이동하기도 한다. LINE 서열은 LTR 레트로트랜스포존보다 길고 가변적이다.
역전사 과정이 중간에 멈추는 경우가 많아, 삽입된 LINE 복사본들은 종종 5' 말단이 잘린 불완전한 형태를 가지며 길이가 다양하다. 이로 인해 전사에 필요한 프로모터 영역이 소실되면 해당 LINE은 더 이상 전위 능력을 잃게 된다.[15]
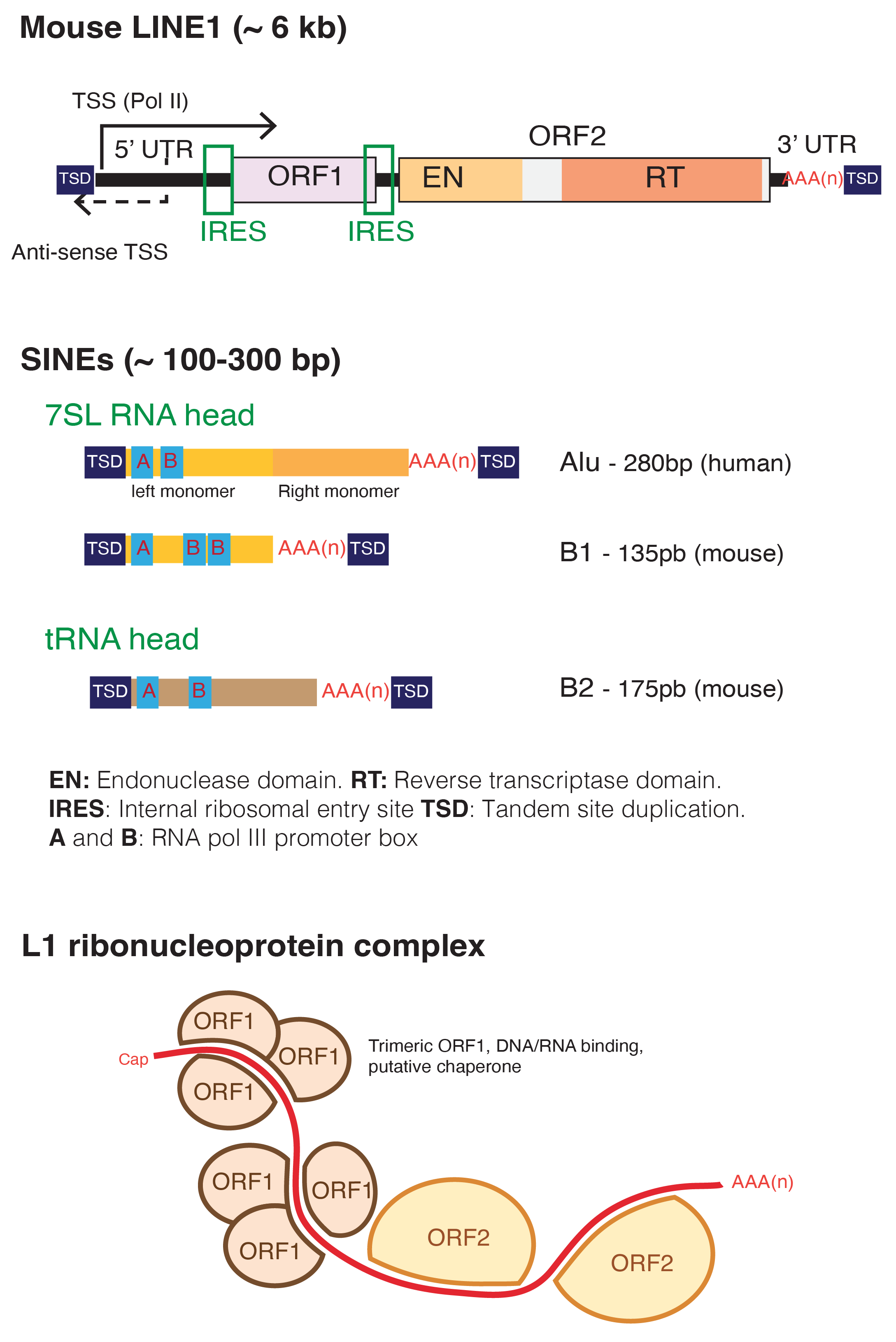
LINE-1(L1) 레트로트랜스포존은 인간 게놈의 상당 부분을 차지하며, 게놈당 약 50만 개의 복사본이 있는 것으로 추정된다. 인간 L1 유전자의 전사는 일반적으로 DNA 메틸화(DNA 메틸전달효소에 의해 메틸기가 DNA에 결합) 및 PIWI 단백질 등에 의해 억제된다. L1이 유전자 내부나 근처에 삽입되면 해당 유전자의 기능을 파괴하여 유전 질환이나 암과 같은 질병을 유발할 수 있다. L1의 전위는 개인 간의 유전적 다양성에 기여하기도 하며, 때로는 염색체 구조 변화를 일으키기도 한다.[17] 인간 참조 게놈에는 약 80~100개의 전위 능력이 있는 활성 L1이 존재하지만, 이 중 실제로 활발하게 전위를 일으키는 L1의 수는 더 적다. L1 삽입은 암유전자를 활성화하거나 종양 억제 유전자의 기능을 방해하여 종양 형성과 관련이 있는 것으로 알려져 있다.
각 인간 L1은 유전자 산물을 암호화할 수 있는 두 개의 영역(ORF1, ORF2)을 포함한다. ORF1에는 단백질-단백질 상호작용에 관여하는 류신 지퍼 모티프를 포함하며 RNA 결합 능력과 핵산 샤페론(chaperone) 활성을 가지는 단백질(ORF1p)을 암호화한다. ORF2에는 엔도뉴클레이스와 역전사 효소 활성을 모두 가진 단백질(ORF2p)을 암호화하며, 이 단백질은 아미노산 시스테인과 히스티딘이 풍부하다. 다른 레트로트랜스포존과 마찬가지로 인간 L1의 끝은 아데닌이 풍부하다.[18][19][20]
인간 L1은 인간 게놈에서 활발하게 레트로트랜스포지션한다. 최근 연구에서는 1,708개의 체세포 L1 레트로트랜스포지션 사건을 확인했으며, 특히 대장암과 같은 종양 조직 및 대장 상피 세포에서 많이 발생했다. 이러한 사건은 초기 배아 발생부터 발생하며 대장 종양 발생 과정에서 레트로트랜스포지션 속도가 실질적으로 증가한다.[21]
2. 2. 2. SINE (Short Interspersed Nuclear Element)
SINE(Short Interspersed Nuclear Element, 짧은 산재 핵 요소)는 LINE과 함께 Non-LTR 레트로트랜스포존의 한 종류이다. 이름에서 알 수 있듯이 LINE보다 훨씬 짧아서 길이는 약 300bp 정도이다.[22] SINE 서열은 유전자를 mRNA 전사체로 전사하는 RNA 중합효소 II에 의해 전사되는 유전자, 그리고 리보솜 RNA, tRNA, 기타 작은 RNA 분자로 전사하는 RNA 중합효소 III의 시작 서열과 유사성을 가진다.[23] 포유류의 MIR 요소와 같은 일부 SINE는 시작 부분에 tRNA 유전자와 유사한 서열을 가지고 있으며, 끝 부분에는 LINE과 유사하게 아데닌이 풍부한 서열을 가진다.SINE은 자체적으로 기능적인 역전사 효소 단백질을 암호화하지 않기 때문에 스스로 전위(transposition)할 수 없다. 대신, 다른 이동성 요소인 LINE이 만들어내는 효소와 단백질(전위 구성 요소)을 이용하여 게놈 내 다른 위치로 이동한다.[24] LINE 결합 단백질은 기본적으로 LINE RNA에 결합하는 것을 선호하지만, SINE의 특정 부분(LINE 유래 부분)을 인식하여 결합할 수 있다. SINE은 일반적으로 tRNA 유래 부분과 LINE 유래 부분으로 구성되는데, tRNA 유래 부분에는 RNA 중합효소 III 프로모터가 포함되어 있어 SINE RNA가 전사될 수 있도록 한다. 이렇게 전사된 SINE RNA는 LINE 구성 요소 덕분에 LINE 결합 단백질에 의해 인식되어 LINE의 전위 시스템을 이용하게 된다.
영장류에서 가장 흔하게 발견되는 SINE은 Alu 요소이다. Alu 요소는 약 350bp 길이이며 단백질을 암호화하지 않는다. 이름은 제한 효소 AluI에 의해 인식되는 특정 서열을 가지고 있기 때문에 붙여졌다. Alu 요소의 분포는 일부 유전 질환이나 암 발생과 관련이 있을 수 있다. Alu 요소가 복제되어 다른 위치에 삽입되는 과정(복사 및 붙여넣기)은 Alu RNA의 아데닌이 풍부한 말단 서열과 신호 인식 서열에 의존한다. 신호가 인식된 Alu RNA는 리보솜에 결합할 수 있으며, 이때 LINE RNA도 같은 리보솜에 결합하게 된다. 이러한 동시 결합을 통해 Alu 요소는 LINE의 전위 기구를 이용하여 복제되고 게놈 내 다른 위치로 삽입될 수 있다.
2. 2. 3. SVA 요소
SVA 요소는 SINE과 LINE의 특징을 모두 가지는 레트로트랜스포존의 한 종류이다. 이는 Alu 요소, VNTR(가변 수 탄뎀 반복 서열), LTR 조각의 융합을 통해 생성되었다.[25] SVA 요소의 시작 부분은 Alu 요소와 유사하며, 반복 서열과 내생 레트로바이러스와 유사한 종결부를 가진다. 전이 과정에서는 LINE이 SVA 요소의 측면에 결합하여 이를 이동시킨다.인간 게놈 내에서는 SINE이나 LINE 요소보다 적은 수로 존재한다. SVA는 유인원 게놈에서 가장 최근에 나타난 전이 인자 중 하나로 여겨지며, 특히 인간 집단 내에서는 가장 활발하게 활동하고 높은 다형성을 보이는 전이 인자 중 하나이다.[25]
3. 레트로트랜스포존의 생물학적 역할
레트로트랜스포존은 복제적 전이를 통해 게놈 내에서 자신의 복제 수를 늘려 게놈 크기 증가에 기여한다. 이 과정에서 유전자 근처나 내부에 삽입되어 돌연변이를 유발할 수 있으며, 이러한 돌연변이는 비교적 안정적으로 유지되는 경향이 있다.
레트로트랜스포존과 숙주 게놈은 수천만 년에 걸쳐 서로 영향을 주고받으며 함께 진화해 온 것으로 보인다. 이들은 서로에게 해로운 영향을 줄이면서 생존 기회를 높이는 방향으로 전이 및 삽입 특성, 돌연변이 형질 등을 조절하는 메커니즘을 발전시켜 왔을 것으로 추정되며, 이에 대한 구체적인 연구가 진행 중이다.
3. 1. 인간 질병과의 관련성
LINE1(L1)과 같은 레트로트랜스포존은 인간 게놈 내에서 이동하며 유전자의 기능에 영향을 미칠 수 있다. L1 레트로트랜스포지션은 유전자 내부나 그 근처에 자신을 삽입하여 원래 유전자의 기능을 파괴함으로써 결과적으로 인간의 질병을 유발할 가능성이 있다.[17]특히 L1 삽입은 암과 관련된 유전자에 영향을 미쳐 종양 형성과 연관될 수 있다. 예를 들어, 발암 유전자를 활성화하거나 종양 억제 유전자의 기능을 감소시키는 방식으로 작용할 수 있다.[17] 최근 연구에서는 1,708개의 체세포 L1 레트로트랜스포지션 사례가 확인되었는데, 특히 대장 상피 세포에서 이러한 현상이 두드러졌다. 이는 초기 배아 발생 단계부터 나타나며, 대장 종양 발생 과정에서는 레트로트랜스포지션 속도가 상당히 증가하는 것으로 관찰되었다.[21]
또한, LINE 레트로트랜스포존은 신경계로 발달하는 인간 배아 세포로 전이될 수도 있어, 이것이 뇌 기능에 미치는 영향에 대한 연구가 진행 중이다. LINE 레트로트랜스포지션은 여러 종류의 암에서 나타나는 특징이기도 하지만, 이것이 단순히 암의 결과인지 아니면 직접적인 원인인지는 아직 명확하게 밝혀지지 않았다.
레트로트랜스포존의 복제적 전이는 게놈 크기를 크게 늘릴 수 있으며, DNA 서열이 유전자 근처나 내부에 삽입되면서 돌연변이를 일으킬 수 있다. 이렇게 발생한 돌연변이는 삽입된 서열이 복제 과정에서 유지되기 때문에 비교적 안정적인 특징을 가진다.
통제되지 않는 레트로트랜스포지션은 숙주 생물과 레트로트랜스포존 자체 모두에게 해로울 수 있으므로, 그 활동은 숙주 게놈 내에서 조절된다. 대표적인 조절 기작으로 RNA 간섭이 있으며, 이는 여러 종류의 짧은 비암호화 RNA가 단백질 아고노트(Argonaute)와 상호작용하여 레트로트랜스포존 전사체를 분해하거나, DNA 히스톤 구조를 변경하여 전사를 억제하는 방식으로 작동한다.
3. 2. 진화에서의 역할
내생 레트로바이러스(ERV)는 레트로트랜스포존과 유사하게 다음 세대로 전달될 수 있는 방식으로 숙주 게놈에 유전 정보를 삽입하여 통합된 레트로바이러스이다. 이들은 바이러스로서의 병원성 효과는 없으며,[9] 레트로바이러스와 레트로트랜스포존의 특징을 공유한다. 레트로바이러스 DNA가 숙주 게놈에 통합되면, 이는 진핵생물 게놈에 영향을 미치는 내생 레트로바이러스로 진화할 수 있다. 많은 내생 레트로바이러스가 진핵생물 게놈에 삽입되어 있으며, 이는 바이러스-숙주 상호작용과 진화 및 질병에서 레트로트랜스포존의 역할에 대한 이해를 돕는다.많은 레트로트랜스포존은 숙주 게놈을 인식하고 융합하는 내생 레트로바이러스의 특징을 공유한다. 그러나 레트로바이러스의 ''env'' 유전자는 중요한 차이점을 형성한다. 이 유전자는 레트로바이러스 외피의 당단백질을 암호화하여 숙주 세포로 들어가는 데 필요하며, 해당 유전 요소가 레트로바이러스인지 레트로트랜스포존인지를 결정하는 기준으로 사용된다.[8][9] ''Env'' 유전자는 LTR 레트로트랜스포존 유형인 Ty1-copia (Pseudoviridae), Ty3-gypsy (Metaviridae) 및 BEL/Pao에서도 발견된다.[8][9] 레트로바이러스는 세포 간 이동이 가능하지만, LTR 레트로트랜스포존은 동일 세포 내의 게놈으로만 이동할 수 있다.[10] 그럼에도 불구하고, 많은 척추동물의 유전자는 레트로바이러스 및 LTR 레트로트랜스포존으로부터 형성되었다. 특정 내생 레트로바이러스나 LTR 레트로트랜스포존이 서로 다른 종에서 동일한 기능과 게놈 위치를 가지는 경우가 있는데, 이는 이들이 진화 과정에서 중요한 역할을 했음을 시사한다.[11] LTR 레트로트랜스포존은 비-LTR 레트로트랜스포존보다 나중에 나타났으며, 조상 격인 비-LTR 레트로트랜스포존이 DNA 트랜스포존으로부터 인테그라제를 획득하면서 생겨난 것으로 추정된다.
레트로트랜스포존은 복제적 전이(retrotransposition) 메커니즘을 통해 빠르게 수를 늘릴 수 있으며, 이로 인해 인간 게놈의 약 40%를 차지하게 되었다. LINE1, Alu, SVA 요소의 삽입률은 각각 1/200–1/20, 1/20, 1/900 정도로 추정되며, 특히 LINE1의 삽입률은 지난 3,500만 년 동안 크게 변동하여 게놈 진화의 특정 시점을 나타내기도 한다.
식물의 경우, 특히 옥수수 게놈의 상당 부분(예: 특정 100킬로베이스 영역)은 레트로트랜스포존의 존재 여부에 따라 다양성을 보인다. 그러나 옥수수는 다른 식물에 비해 유전적으로 독특한 측면이 있어, 옥수수의 사례를 다른 식물의 레트로트랜스포지션 양상을 예측하는 데 직접 사용하기는 어렵다.
레트로트랜스포존은 돌연변이를 유발하여 진화에 영향을 미치는데, 주요 방식은 다음과 같다.
- 유전자 비활성화
- 유전자 조절 변경
- 유전자 산물 변경
- DNA 복구 부위 역할
레트로트랜스포존의 복제적 전이는 요소의 수를 급격히 증가시켜 게놈 크기를 상당히 증대시킨다. 또한, 유전자 근처나 내부에 DNA 서열이 삽입되면서 돌연변이가 발생할 수 있다. 이러한 돌연변이는 삽입 부위의 서열이 복제 및 전이 과정에서 유지되므로 비교적 안정적인 편이다.
레트로트랜스포존의 전이와 숙주 게놈 내에서의 잔류는 수천만 년에 걸쳐 이루어진 레트로트랜스포존-숙주 게놈 간의 상호작용 결과로 보인다. 레트로트랜스포존과 숙주 게놈 모두에게 해로운 영향을 피하기 위해, 전이 과정은 레트로트랜스포존과 숙주 게놈 내의 인자들에 의해 제어되는 것으로 여겨진다. 레트로트랜스포존과 숙주 게놈이 서로의 생존 가능성을 높이기 위해 전이, 삽입 특이성, 돌연변이 형질 등을 조절하는 기구를 어떻게 공진화시켜 왔는지에 대한 연구는 이제 막 시작 단계에 있다.
참조
[1]
논문
An in vivo assay for the reverse transcriptase of human retrotransposon L1 in Saccharomyces cerevisiae
1994-07
[2]
서적
Mobile DNA III
ASM press
2015
[3]
논문
Evidence that a recent increase in maize genome size was caused by the massive amplification of intergene retrotranposons
[4]
논문
Initial sequencing and analysis of the human genome
2001-02
[5]
논문
High-frequency recombination between members of an LTR retrotransposon family during transposition bursts
2017-11
[6]
논문
Becoming a Selfish Clan: Recombination Associated to Reverse-Transcription in LTR Retrotransposons
2019-12
[7]
논문
Origin and evolution of retroelements based upon their reverse transcriptase sequences
1990-10
[8]
논문
The Sinbad retrotransposon from the genome of the human blood fluke, Schistosoma mansoni, and the distribution of related Pao-like elements
2005-02
[9]
논문
A unified classification system for eukaryotic transposable elements
2007-12
[10]
논문
The diversity of LTR retrotransposons
2004-05-18
[11]
논문
Not so bad after all: retroviruses and long terminal repeat retrotransposons as a source of new genes in vertebrates
2016-02-17
[12]
논문
Characterization of the restriction enzyme-like endonuclease encoded by the Entamoeba histolytica non-long terminal repeat retrotransposon EhLINE1
2009-12
[13]
논문
Ancient exaptation of a CORE-SINE retroposon into a highly conserved mammalian neuronal enhancer of the proopiomelanocortin gene
2007-10
[14]
논문
A gene expression restriction network mediated by sense and antisense Alu sequences located on protein-coding messenger RNAs
2013-05
[15]
논문
SINEs and LINEs: highly repeated short and long interspersed sequences in mammalian genomes
1982-03
[16]
논문
Transposon regulation upon dynamic loss of DNA methylation (PDF Download Available)
[17]
논문
LINE retrotransposon RNA is an essential structural and functional epigenetic component of a core neocentromeric chromatin
2009-01
[18]
논문
Characterization of LINE-1 ribonucleoprotein particles
2010-10
[19]
논문
Primate-specific ORF0 contributes to retrotransposon-mediated diversity
2015-10
[20]
논문
SINEs and LINEs: symbionts of eukaryotic genomes with a common tail
[21]
논문
Widespread somatic L1 retrotransposition in normal colorectal epithelium
2023-05-18
[22]
서적
A dictionary of genetics
Oxford University Press
[23]
서적
Short retroposons in eukaryotic genomes
[24]
논문
LINE-mediated retrotransposition of marked Alu sequences
2003-09
[25]
논문
A Field Guide to Eukaryotic Transposable Elements.
2020-11-23
본 사이트는 AI가 위키백과와 뉴스 기사,정부 간행물,학술 논문등을 바탕으로 정보를 가공하여 제공하는 백과사전형 서비스입니다.
모든 문서는 AI에 의해 자동 생성되며, CC BY-SA 4.0 라이선스에 따라 이용할 수 있습니다.
하지만, 위키백과나 뉴스 기사 자체에 오류, 부정확한 정보, 또는 가짜 뉴스가 포함될 수 있으며, AI는 이러한 내용을 완벽하게 걸러내지 못할 수 있습니다.
따라서 제공되는 정보에 일부 오류나 편향이 있을 수 있으므로, 중요한 정보는 반드시 다른 출처를 통해 교차 검증하시기 바랍니다.
문의하기 : help@durumis.com
