후성유전학
"오늘의AI위키"의 AI를 통해 더욱 풍부하고 폭넓은 지식 경험을 누리세요.
1. 개요
후성유전학은 DNA 염기 서열의 변화 없이 유전자 발현이 변화하는 현상을 연구하는 학문 분야이다. 1942년 C.H. 와딩턴에 의해 명명되었으며, DNA 메틸화, 히스톤 변형, 비암호화 RNA 간섭 등 다양한 메커니즘을 통해 유전자 발현을 조절한다. 후성유전학은 발생 및 분화, 질병 연구, 세대 간 유전 등 다양한 분야에서 연구되고 있으며, 암, 기억 형성, 뇌 노화, 중독 등 질병의 진단과 치료에 활용될 수 있는 잠재력을 지닌다.
코이네 그리스어 ἐπιγέννησις에서 유래한 "후성설"이라는 용어는 17세기부터 영어에서 "추가 성장"이라는 일반적인 의미로 사용되었다.[320] 이와 관련된 "후성유전학"은 C. H. 와딩턴에 의해 만들어졌으며, 동시에 Valentin Haecker의 ‘형질유전학(phenogenetics)’에서도 후성설이 존재했다.[321]
DNA 메틸화와 히스톤의 화학적 변형은 후성유전학의 주요 메커니즘으로 자주 거론되지만, 이 두 가지 외에도 다양한 기작들이 존재한다(표 1). 많은 생물에서 RNA 간섭과 같은 비번역 RNA에 의한 조절이 알려져 있으며(표 2), 히스톤 변이체의 관여나 염색질 리모델링 인자 등 히스톤 이외의 단백질 관여도 알려져 있다. DNA 메틸화, 히스톤 변형, 비번역 RNA는 각각 별개의 사건으로 발견되었지만, 이들 세 가지 종류의 사건이 서로 연계하여 염색질 구조 변화와 유전자 발현 조절에 관여하는 예도 많으며, 그 전형적인 예로 X 염색체 불활성화를 들 수 있다.
2. 역사
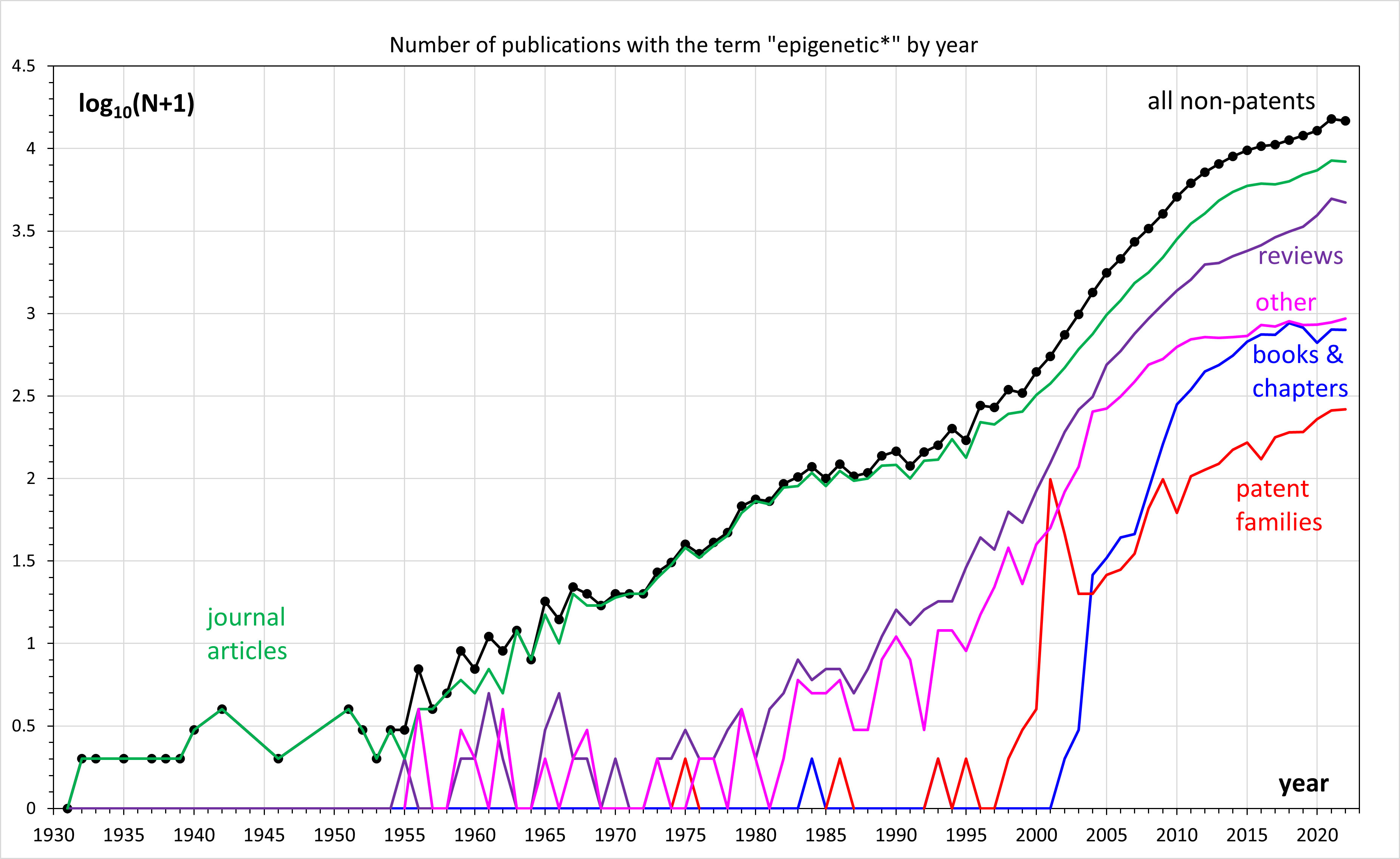
과학 출판물에서 "후성유전학"이라는 용어는 1930년대에 나타나기 시작했지만, 현대적인 의미는 1990년대에 들어서야 나타났다.[11] 염색체의 발현에 영향을 미치는 후성적 변화에 대한 가설은 러시아 생물학자 니콜라이 콜초프에 의해 제시되었다.[13] 영국 발생학자 C. H. 와딩턴은 1942년에 '후성유전학(epigenetics)'이라는 용어를 발생과 관련하여 발렌틴 헤커의 '현상유전학(Phänogenetik)'에 맞춰 만들었다.[14] 당시 생물학의 맥락에서 '발생'은 배아 발생 동안 초기 전능성 상태로부터 세포의 세포 분화를 의미했다.[15]
"DNA 염기서열의 변화 없이 염색체의 변화로 인한 안정적으로 유전 가능한 표현형"이라는 의미의 "후성유전적 형질" 개념에 대한 정의는 2008년 콜드 스프링 하버 회의에서 공식화되었지만,[24] 유전되지 않는 형질을 포함하는 대체 정의가 여전히 널리 사용되고 있다.[12]
로빈 홀리데이는 1990년에 후성유전학을 "복잡한 유기체의 발달 과정에서 유전자 활동의 시간적 및 공간적 조절 메커니즘 연구"로 정의했다.[20] 아서 리그스와 동료들은 후성유전학을 "DNA 염기서열 변화로는 설명할 수 없는 유전자 기능의 체세포 분열 및/또는 감수 분열을 통해 유전되는 변화"를 연구하는 것이라고 정의했다.[21] 에이드리언 버드는 후성유전학을 "변형된 활동 상태를 등록, 신호 또는 영속시키기 위한 염색체 영역의 구조적 적응"으로 정의했다.[7]
2008년, 콜드 스프링 하버 회의에서 "DNA 염기서열의 변경 없이 염색체의 변화로 인한 안정적으로 유전되는 표현형"인 후성유전적 형질에 대한 합의된 정의가 이루어졌다.[24] "후성유전체"는 세포의 전반적인 후성유전적 상태를 나타내는 "게놈"과 유사하며, 후성유전체학은 전체 게놈에 걸쳐 후성유전적 변화를 전반적으로 분석하는 것을 의미한다.[12] "유전 암호"라는 문구도 채택되었으며, "후성유전 암호"는 동일한 기본 DNA 염기서열에서 서로 다른 세포에서 서로 다른 표현형을 생성하는 후성유전적 특징 집합을 설명하는 데 사용되었다.
2. 1. 초기 개념
코이네 그리스어 ἐπιγέννησις에서 유래한 "후성설"이라는 용어는 17세기부터 영어에서 "추가 성장"이라는 일반적인 의미로 사용되었다.[320] 이와 관련된 "후성유전학"은 C. H. Waddington에 의해 만들어졌으며, 동시에 Valentin Haecker의 ‘형질유전학(phenogenetics)’에서도 후성설이 존재했다.[321] 생물학의 맥락에서 후성은 배아 발달 초기 전능 상태에서 세포의 분화를 의미한다.[322]
Waddington이 용어를 만들 당시에는 유전자와 유전적인 역할의 기질은 알려지지 않았다. 그는 유전자 형질을 생산하는 주변 환경과 상호 작용하는 방법의 개념적 모형으로 "후성유전학적 지형(epigenetic landscape)"을 사용했다. 그는 세포의 운명이 결정되는 것이 낮은 고도의 지점으로 구슬이 떨어지는 것과 매우 비슷하다고 여겼다.[323] Waddington은 구슬이 능선을 상승하며 골짜기 사이를 이동하는 것을 세포 분화의 비가역적인 증가로 시각화했다.[324]
최근의 후성유전학적 지형에 대한 Waddington의 개념은 엄격하게 세포 운명 연구에 시스템의 역학적 상태 접근의 맥락에서 공식화되었다.[325][326] 세포 운명의 결정은 어트랙터(attractor) 수렴이나 진동 등의 특정 역학을 나타낼 것으로 예상된다.[326]
"후성적"이라는 용어는 유전과 환경의 지속적인 양방향 교환의 결과로서 심리적 현상을 설명하기 위해 발달 심리학에 이용되고있다.[327] 개발 아이디어는 19세기와 20세기에 걸쳐 다양한 형태와 다양한 이름에서 논의되고 있다. 초기 버전은 칼 에른스트 폰 배어에 의해 제안되었고, 에른스트 헤켈에 의해 대중화되었다.
"DNA 염기서열의 변화 없이 염색체의 변화로 인한 안정적으로 유전 가능한 표현형"이라는 의미의 "후성유전적 형질" 개념에 대한 정의는 2008년 콜드 스프링 하버 연구소 회의에서 공식화되었지만,[24] 유전되지 않는 형질을 포함하는 대체 정의가 여전히 널리 사용되고 있다.[12]
염색체의 발현에 영향을 미치는 후성적 변화에 대한 가설은 러시아 생물학자 니콜라이 콜초프에 의해 제시되었다.[13] 영국 발생학자 C. H. 와딩턴은 1942년에 '후성유전학(epigenetics)'이라는 용어를 발생과 관련하여 발렌틴 헤커의 '현상유전학(Phänogenetik)'에 맞춰 만들었다.[14]
1942년, 워딩턴은 '후성설(epigenesis)'과 '유전학(genetics)'의 혼성어로서 '후성유전학'이라는 단어를 만들었다. 후성설은 수정란으로부터 생물의 형태가 만들어지는 것을 설명하는 오래된 학설 중 하나이다[249] (역사적 배경에 대해서는 전성설도 참조).
2. 2. 현대적 정의
로빈 홀리데이는 1990년에 후성유전학을 "복잡한 유기체의 발달 과정에서 유전자 활동의 시간적 및 공간적 조절 메커니즘 연구"로 정의했다.[20]
아서 리그스와 동료들은 후성유전학을 "DNA 염기서열 변화로는 설명할 수 없는 유전자 기능의 체세포 분열 및/또는 감수 분열을 통해 유전되는 변화"를 연구하는 것이라고 정의했다.[21]
그러나 이 용어는 히스톤 변형의 일부 형태와 같이 유전성이 입증되지 않은 과정을 설명하는 데에도 사용되었다. 에이드리언 버드는 후성유전학을 "변형된 활동 상태를 등록, 신호 또는 영속시키기 위한 염색체 영역의 구조적 적응"으로 정의했다.[7] 이 정의는 DNA 복구 또는 세포 주기 단계와 관련된 일시적인 변형뿐만 아니라 여러 세포 세대에 걸쳐 유지되는 안정적인 변화를 포함하지만, 막 구조의 템플릿화 및 프리온과 같이 염색체 기능에 영향을 미치지 않는 다른 것들은 제외한다.
2008년, 콜드 스프링 하버 회의에서 "DNA 염기서열의 변경 없이 염색체의 변화로 인한 안정적으로 유전되는 표현형"인 후성유전적 형질에 대한 합의된 정의가 이루어졌다.[24]
"후성유전체"는 세포의 전반적인 후성유전적 상태를 나타내는 "게놈"과 유사하며, 후성유전체학은 전체 게놈에 걸쳐 후성유전적 변화를 전반적으로 분석하는 것을 의미한다.[12] "유전 암호"라는 문구도 채택되었으며, "후성유전 암호"는 동일한 기본 DNA 염기서열에서 서로 다른 세포에서 서로 다른 표현형을 생성하는 후성유전적 특징 집합을 설명하는 데 사용되었다.
3. 주요 메커니즘
DNA 메틸화 사이토신 잔기에 메틸기(-CH3)가 결합하는 화학 반응 히스톤 변형 히스톤 단백질의 아미노산 잔기, 특히 N말단(히스톤 테일)에 일어나는 다양한 화학적 변형 (예: 아세틸화, 메틸화, 인산화, 유비퀴틴화) 비번역 RNA (ncRNA)에 의한 조절 RNA 간섭 등 비번역 RNA에 의한 유전자 침묵을 포함한 유전자 발현 조절 히스톤 변이체 뉴클레오솜을 구성하는 히스톤 단백질의 다양한 변이체 염색질 리모델링 염색질 리모델링 인자 등 히스톤 이외의 단백질에 의한 염색질 구조 변화
후성유전학적 유전자 발현 조절은 크게 촉진과 억제로 나눌 수 있으며, 억제는 유전자 침묵과 거의 같은 의미이다. 유전자 침묵은 전사형 유전자 침묵 (transcriptional gene silencing)과 전사후 유전자 침묵 (post-transcriptional gene silencing)으로 더 세분화된다. 일반적으로 DNA 메틸화는 전사 억제(탈메틸화는 전사 촉진)에, 히스톤의 화학적 변형을 중심으로 한 염색질 구조 변화는 전사 촉진과 전사형 유전자 침묵에, 비번역 RNA에 의한 조절은 전사형 유전자 침묵 및 전사후 유전자 침묵과 관련되어 있다.RNA 간섭 (RNAi) Dicer 효소에 의해 생성된 저분자 간섭 RNA (siRNA)가 상동성 mRNA를 분해하는 현상 (좁은 의미의 RNAi) RNA 지령형 DNA 메틸화 (RdDM) 식물에서 관찰되는 siRNA에 의한 전사후 유전자 침묵으로, siRNA와 상동인 DNA 염색 서열의 시토신 잔기가 메틸화되는 현상 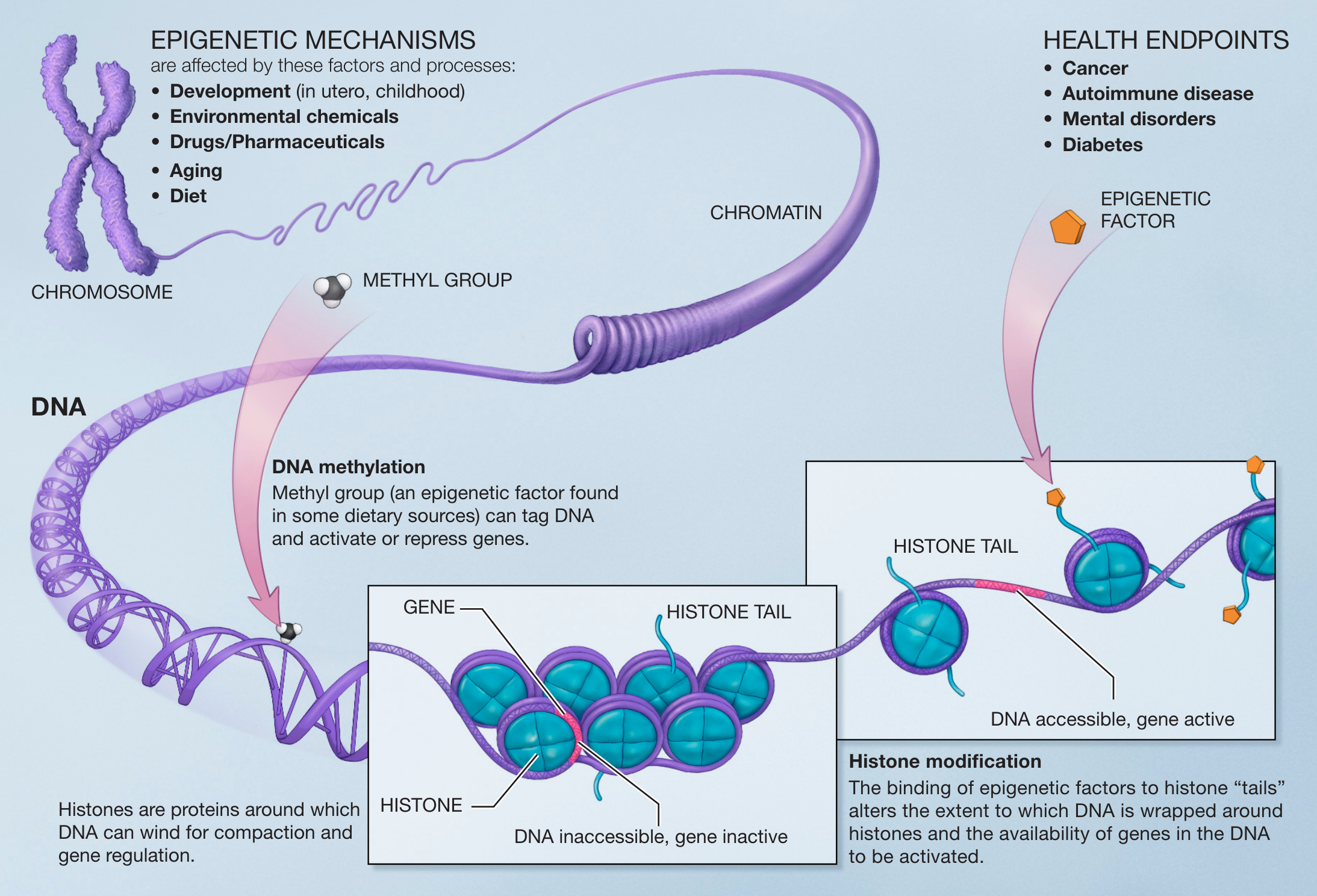
DNA에서의 공유결합 변경 (예: 사이토신 메틸화 및 하이드록시메틸화) 또는 히스톤 단백질에서의 공유결합 변경 (예: 라이신의 아세틸화, 라이신과 아르기닌의 메틸화, 세린 및 트레오닌 인산화, 라이신 유비퀴틴화 및 수모화)이 후성유전학적 유전의 여러 종류 중에서 중심적인 역할을 한다.[331]
세포나 개체의 표현형은 어떠한 유전자가 전사되는지에 영향을 받기 때문에, 유전 가능한 전사 상태는 후성유전학적 영향을 야기할 수 있다. 유전자 발현 조절에는 여러 단계가 있는데, 그중 한 가지 방법은 염색질의 리모델링을 통해서이다. 염색질은 히스톤 단백질이 연관되어 있는 DNA 복합체이다. 만약 DNA가 히스톤을 감싸는 방식이 바뀌는 경우, 유전자 발현 또한 변경될 수 있다. 염색질 리모델링은 아래의 두 가지 메커니즘을 통해 이루어진다.
1. 히스톤 단백질을 구성하는 아미노산의 번역 후 변형. 히스톤 단백질은 아미노산의 긴 사슬로 구성되며, 아미노산 사슬이 변경되는 경우 히스톤의 형상이 변형될 수 있다. DNA는 완전히 복제하는 동안 풀리지 않으며, 수정된 히스톤은 DNA의 새 복사본으로 옮겨갈 수 있다. 이러한 히스톤은 새로운 방식으로 형성될 수 있는 주변의 새로운 히스톤의 주형으로 작용할 수 있다.
2. DNA에 메틸기를 첨가하는 과정. 이 과정은 대부분 CpG 부위에 있는 사이토신을 5-메틸사이토신으로 변환하며 일어난다. 5-메틸사이토신은 이중 가닥 DNA의 구아닌과 결합하여 일반 사이토신과 같이 작동한다. 그러나 게놈의 일부 영역이 다른 것보다 더 많이 메틸화되고, 메틸화가 많이 일어난 부분은 전사가 억제되는데, 이러한 메커니즘은 아직 연구가 더 필요하다.
로빈 홀리데이는 1990년에 후성유전학을 "복잡한 유기체의 발달 과정에서 유전자 활동의 시간적 및 공간적 조절 메커니즘 연구"로 정의했다.[20] 아서 리그스와 동료들은 "DNA 염기서열 변화로는 설명할 수 없는 유전자 기능의 체세포 분열 및/또는 감수 분열을 통해 유전되는 변화"를 연구하는 것이라고 정의했다.[21]
3. 1. DNA 메틸화
DNA 메틸화는 진정세균을 포함한 광범위한 생물에서 발견되는 현상이다.[261] 진핵생물의 메틸화는 사이토신에 메틸기를 5번 위치에 부착하는 반응이다. 메틸화된 5-메틸시토신은 구아닌과 쌍을 이룰 때 일반적인 사이토신과 거의 동일하게 행동한다. 사이토신과 구아닌이 인접해 있는 CpG 부위[290]에서의 메틸화는 포유류와 피자식물의 반복 서열에서 잘 관찰되며, 트랜스포존의 전이 억제와 강력하게 관련되어 있다. 또한, 포유류와 마찬가지로 피자식물에서도 DNA 메틸화에 의한 게놈 각인이 일어난다.[289] 한편, 피자식물의 DNA 메틸화에는 동물에는 없는 CpG 부위 이외의 메틸화도 있으며, 이에 관여하는 효소도 동정되었다.
인간의 경우 인간 유전체에는 'CpG'라는 이중 염기서열이 다량으로 존재하고 있고, 이 중 약 70%에 이르는 CpG의 사이토신 염기에는 메틸기(-CH3)가 결합되어 있는데, 이를 ‘DNA 메틸화’라고 부른다. 이러한 DNA 메틸화 현상은 유전체의 각종 반복 서열 등에서 흔히 관찰되며, 이는 유전체의 안정성 유지 등에 중요한 역할을 하고 있는 것으로 보고 있다. 한편, 각종 유전자의 상단 5’ 조절 부위에 CpG가 밀집된 독특한 영역이 존재하는데 이를 'CpG 섬'이라고 하며, 이 경우 CpG의 사이토신은 대부분 메틸기가 결합되어 있지 않다. 그러나 경우에 따라서 시토신 메틸화가 발생하며, 이 부위 뉴클레오솜의 히스톤 분자들과의 상호작용을 통해 크로마틴의 구조에 변화를 일으켜 결국 유전자 발현에 영향을 주게 된다. 따라서 유전자의 발현은 DNA 메틸화 및 히스톤 변형 등과 같은 화학적 가역반응에 의해 조절된다고 할 수 있는데, 이와 같이 DNA 염기서열의 변화 없이 크로마틴의 구조적 변화, 즉 ‘크로마틴 리모델링’에 영향을 주어 유전자 발현이 조절되는 기전에 관한 연구 분야를 ‘후성유전학’(Epigenetics)이라고 한다.[319]
포유류나 피자식물 등 CpG 부위에서의 DNA 메틸화 상태를 변경하는 공통적인 방식에는 다음 세 가지가 있다.
# 미수정 CpG 부위에 대한 새로운 메틸화인 '신규 메틸화'(''de novo'' 메틸화)
# 헤미메틸화 DNA[290]를 메틸화하는 '유지 메틸화'
# 기존 메틸기의 '탈메틸화'
일반적으로 1)은 유전자 발현 억제, 2)는 메틸화 상태의 세포 분열 후 계승, 3)은 유전자 발현의 활성화에 작용한다. DNA 메틸화가 유전자 침묵에 작용하는 원리로는, 메틸화된 것 자체가 전사 인자가 DNA에 접근하는 것을 방해하고, 메틸화된 DNA에 단백질이 결합하여 간접적으로 전사 인자의 접근을 방해하며, DNA 메틸화가 히스톤 변형을 유도한다는 점 등이 보고되었다.
CpG 부위 DNA 메틸화는 게놈 전체에 존재하지만 분포는 균일하지 않다. 포유류에서는 전체 CpG 중 70% 정도가 메틸화되어 있으며, 트랜스포존, 위성 DNA, 엑손 등이 고도로 메틸화되어 있다. 한편, 프로모터 및 그 주변 영역에 존재하는 CpG 아일랜드는 기본적으로 거의 메틸화되지 않는다. 예외적인 CpG 아일랜드의 메틸화는 X 염색체 비활성화에서의 이질염색질로의 구조 변화, 발암 과정에서의 암 억제 유전자의 발현 억제 등에서 관찰된다. 이러한 CpG 아일랜드의 메틸화는 조직 특이적인 유전자의 비활성화에서도 관찰되며, 각 세포 기능과 관련되어 있는 것으로 생각된다.
포유류에서의 DNA 메틸화는 적어도 세 개의 독립적인 DNA 메틸기 전이 효소(DNMT1, DNMT3A, DNMT3B)의 상호작용에 의해 부착 또는 유지된다. 체세포에서 가장 많은 메틸기 전이 효소인 DNMT1은[291] DNA 복제 부위에 국재하여[292] 헤미메틸화 DNA를 우선적으로 수정함으로써, 복제 후의 신규 DNA 가닥에 메틸화 패턴을 기록한다.[293][290] 이 효소는 적절한 배 발생, 각인 및 X 염색체 비활성화를 위해 필수적이다.[294] 애기장대에서도 동일한 유지 메틸화 기능을 가진 효소 MET1이 존재하며, 포유류 DNMT1과 같은 기원을 가진 유전자(오쏘로그)인 것으로 밝혀졌다. 또한, 애기장대의 ''de novo''형 DNA 메틸화 효소는 포유류 DMNT3의 오쏘로그에 해당하는 DRM2이다. 식물에서 알려진 RNA 지령형 DNA 메틸화(RNA-directed DNA methylation: RdDM)에 대해서는 비번역성 RNA에 의한 제어#RdDM에서 후술한다. 또한, 식물 종자에 대기압 플라즈마를 조사함으로써 DNA의 탈메틸화가 일어난다는 것이 보고되었다.[295]
3. 2. 히스톤 변형
'''염색질'''은 '''히스톤'''에 DNA가 감긴 '''뉴클레오솜''' 구조를 가진 복합체이다. DNA가 히스톤에 감겨 있는 상태가 변하면, 염색질 리모델링(재구축·재구성)이 일어나 유전자 발현도 변화한다. 히스톤의 메틸화는 1964년에 발견되었지만, 그 생리적 의의는 오랫동안 불명이었다.[319] 이후 연구를 통해 수많은 화학적 변형이 발견되었으며, 그 번역 후 변형의 역할은 효모, 동물, 식물에서 공통적인 경우가 많다는 것이 밝혀지고 있다.[319] 히스톤 변형은 아미노산 서열 전체에 걸쳐 발생하지만, 히스톤의 N말단(히스톤 테일)이 특히 고빈도로 변형된다. 이러한 변형에는 '''아세틸화''', '''메틸화''', '''유비퀴틴''', '''인산화''', '''SUMO화'''가 포함된다.
아세틸화는 잘 연구된 화학적 변형이다. 예를 들어, 히스톤 아세틸기 전이 효소(histone acetyltransferase, HAT)에 의한 히스톤 H3 테일의 K9와 K14 라이신[296]의 아세틸화는 일반적으로 높은 전사 능력과 관련되어 있다(표3). 히스톤의 라이신 잔기는 양전하를 띤 질소 원자를 포함하는 아미노기를 측쇄에 가지며, DNA 골격의 음전하를 띤 인산기와 결합하기 쉽다. 라이신 잔기의 아세틸화는 아미노기의 양전하를 중화시켜 히스톤과 DNA 간의 상호 작용을 약화시킴으로써 전사 인자가 DNA에 접근하는 것을 가능하게 한다.[319] 이처럼 히스톤 변형이 뉴클레오솜의 구조를 변화시켜 전사에 영향을 미친다는 설명을 '''"시스" 모델'''이라고 한다.
| 변형 종류 | 히스톤 / 피변형 아미노산 잔기[296] | ||||||
|---|---|---|---|---|---|---|---|
| H3 | H4 | H2B | |||||
| H3K4 | H3K9 | H3K14 | H3K27 | H3K79 | H4K20 | H2BK5 | |
| 모노메틸화 | 활성화[297] | 활성화[298] | 활성화[298] | 활성화[298][299] | 활성화[298] | 활성화[298] | |
| 디메틸화 | 억제[300] | 억제[300] | 활성화[299] | ||||
| 트리메틸화 | 활성화[301] | 억제[298] | 억제[298] | 활성화[299] 억제[298] | 억제[300] | ||
| 아세틸화 | 활성화[301] | 활성화[301] | |||||
히스톤 변형에 의한 기능의 또 다른 모델은 '''"트랜스" 모델'''이다. 히스톤 변형 효소가 작용하여 다른 단백질과의 결합 부위를 만들고, 그 단백질이 염색질에 회합함으로써 전사를 제어한다.[319] 예를 들어, 트랜스 모델은 H3K9[296] 메틸화에 의해 뒷받침된다. H3K9의 메틸화는 항존적인 전사 불활성 염색질(구조적 헤테로크로마틴)과 관련되어 왔으며, 메틸화된 H3K9는 크로모도메인(메틸리신 특이적 결합 도메인)을 가진 전사 억제 단백질 HP1을 리크루트한다.[319]
라이신 잔기 메틸화는 변형을 받는 잔기, 동일 잔기가 받는 메틸화 상태(모노, 디, 트리)의 종류가 많고, 작용도 전사의 활성화와 억제 모두에 관여하여 다른 히스톤 변형에 비해 복잡하다. H3K9 메틸화와 HP1의 관계는 초파리의 위치 효과에 의한 얼룩무늬(PEV)에서 헤테로크로마틴 영역의 확대와도 관련이 있다고 여겨진다. 한편, H3K4의 메틸화는 유크로마틴에서의 유전자 발현 활성화와 관련되어 있으며, 여러 인자가 H3K4 트리메틸화를 유도하는 것으로 알려져 있다.[319]
히스톤 라이신 메틸기 전이 효소(lysine methyltransferase, KMT)는 히스톤 H3 및 H4에 대해 메틸화 활성을 담당한다. 이 효소는 SET 도메인(Suppressor of variegation, Enhancer of zeste, Trithorax)이라고 불리는 촉매 활성 부위를 이용한다. SET 도메인은 유전자 활성 조절에 관여하는 130 아미노산 서열이다. 이 도메인은 히스톤 테일에 결합하여 히스톤의 메틸화를 일으키는 것으로 나타났다.[302] 히스톤 H3와 H4는 히스톤 라이신 탈메틸화 효소 (lysine demethylase [KDM])에 의해 탈메틸화되기도 한다. 이 효소는 십자 도메인(JmjC)이라고 불리는 촉매 활성 부위를 가지고 있다. 십자 도메인이 여러 보조 인자를 사용하여 메틸기를 히드록실화하여 제거하면 탈메틸화가 일어난다. 십자 도메인은 메틸기를 1-3개 가진 기질을 탈메틸화할 수 있다.[303]
; 히스톤 코드
복수이며 동적인 히스톤의 화학적 변형에 의한 유전자 제어 개념은 히스톤 코드 가설이라고 불린다.[304] 이 가설은 "히스톤 화학적 변형의 특정 조합이 마치 암호(코드)처럼 작용함으로써 다종다양한 반응을 유도하여 염색질 기능을 제어한다"는 것이다. 개별 히스톤 변형의 영향이 밝혀지고 있지만, 여러 변형이 협조적 또는 대립적인 영향을 가지면서 공존하는 예나, 동일한 변형이 존재하는 조건에 따라 다른 영향을 초래하는 예가 알려져 있다.[319] 따라서, 여러 종류의 히스톤 변형에 의해 제어되는 에피제네틱한 과정의 복잡성을 이해하기 위해서는 히스톤 코드 가설이 유효하다고 인정하는 견해도 있다.[319]
; 염색질 리모델링
염색질 리모델링은 DNA와 히스톤 사이의 위치 관계가 변화하고, 그에 따라 유전자 발현이 촉진 또는 억제되는 것이다.[319] 히스톤 변형과 ATP 의존성 리모델링 인자(SWI/SNF 등)에 의한 염색질 변화를 가리킨다.[305]
3. 3. 비암호화 RNA(ncRNA) 간섭
비번역 RNA(ncRNA)는 단백질로 번역되지 않고 기능하는 RNA를 말하며, 염기 수나 가닥 형태가 다른 여러 종류를 통칭한다. 비번역 RNA는 RNA 간섭 (RNAi), 헤테로크로마틴 형성, 그리고 식물의 RNA 지령형 DNA 메틸화(RdDM) 등 다양한 과정을 통해 후성유전적 유전자 조절에 관여한다.[306]RNA 간섭(RNAi)은 비번역 RNA에 의한 전사 후 유전자 침묵 현상이다. 어떤 이유로 이중 가닥 RNA(dsRNA)가 존재하면, Dicer라는 효소에 의해 dsRNA가 절단되어 20여 염기 이하의 짧은 이중 가닥 RNA (저분자 간섭 RNA, siRNA)가 된다. 이 siRNA와 동일한 염기 서열을 가진 mRNA가 분해되는 현상을 좁은 의미의 RNAi라고 한다.[306] 그러나 siRNA가 관여하는 유전자 침묵 전반을 RNAi라고 하거나, RNA 침묵이라는 용어를 RNAi와 동의어로 사용하기도 한다. 좁은 의미의 RNAi는 식물, 선충, 포유류를 포함한 다양한 생물에서 보존되는 현상이므로, 현재는 유전자 녹다운 기술로 널리 이용된다. RNAi를 발견한 앤드루 파이어와 크레이그 멜로는 그 공로로 2006년 노벨 생리학·의학상을 수상했다.[307]
RNA 지령형 DNA 메틸화(RdDM)는 식물에서 관찰되는 siRNA에 의한 전사 후 유전자 침묵이며, 넓은 의미의 RNAi에 포함되기도 한다. 동물에서 RdDM과 동일한 기능이 있는지는 밝혀지지 않았다. RdDM은 siRNA와 상동인 DNA 염기 서열의 시토신 잔기가 메틸화되는 현상이며, siRNA의 근원이 되는 RNA가 핵 내 DNA의 전사 산물이든 외부에서 유래한 RNA이든 발생한다. 벼에 유전자 도입 실험에서 도입한 유전자의 프로모터를 RdDM으로 불활성화한 결과, 히스톤에서 H3K9의 디메틸화 및 H3와 H4의 탈아세틸화가 동시에 일어나는 것이 보고되었다. RdDM에 의한 유전자 발현 불활성화는 외부 유전자가 게놈에 침입했을 때 게놈 내 이동을 억제하는 방어 작용으로 추정된다.
3. 4. 기타 메커니즘
후성유전학에는 DNA 메틸화와 히스톤 변형 외에도 다양한 기작들이 존재한다. 이러한 기작들은 유전자 발현 조절에 중요한 역할을 하며, 세포 분화 및 발생 과정에서 핵심적인 기능을 수행한다.주요 후성유전학적 기작:
- 비번역 RNA (ncRNA)에 의한 조절: RNA 간섭 등 비번역 RNA는 유전자 침묵을 포함한 유전자 발현 조절에 관여한다. 특히, 전사형 유전자 침묵 (transcriptional gene silencing) 및 전사후 유전자 침묵 (post-transcriptional gene silencing)에 모두 작용한다.[284]
- 히스톤 변이체: 뉴클레오솜을 구성하는 히스톤 단백질에는 다양한 변이체가 존재하며, 이들은 게놈의 특정 영역에 무작위적이지 않게 통합된다.[127] 히스톤 변이체의 생화학적 특성은 유전자 조절 및 염색체 구조 유지에 영향을 미친다.[128]
- 염색질 리모델링: 염색질 리모델링 인자 등 히스톤 이외의 단백질도 염색질 구조 변화에 관여한다.
- DNA 메틸화, 히스톤 변형, 비번역 RNA의 상호 연계: 이 세 가지 기작은 서로 독립적으로 작용하는 것이 아니라, 상호 연관되어 복합적인 조절을 수행한다. 예를 들어, X 염색체 불활성화는 DNA 메틸화, 히스톤 변형, 비번역 RNA가 모두 관여하는 대표적인 후성유전학적 현상이다.
- 3차원 게놈 구조: 게놈의 3차원 구조(3D 게놈)는 복잡하고 역동적이며, DNA 복제, 전사, DNA 손상 복구와 같은 게놈 기능 및 핵 과정을 조절하는 데 매우 중요하다.[129]
- 뉴클레오솜 위치: 뉴클레오솜의 위치는 무작위적이지 않으며 조절 단백질에 대한 DNA 접근성을 결정한다. 서로 다른 조직에서 활성화되는 프로모터는 서로 다른 뉴클레오솜 위치 특징을 갖는 것으로 확인되었다.[125]
- 구조적 유전: 섬모충류(예: ''Tetrahymena''와 ''Paramecium'')에서는 유전적으로 동일한 세포들이 세포 표면의 섬모 열 패턴에서 유전 가능한 차이를 보인다.[122] 기존의 구조가 새로운 구조의 템플릿 역할을 하는 것으로 보인다.[123]
프리온:프라이온은 감염성을 가진 단백질 형태로, 일반적으로 전달성 해면상 뇌병증과 같은 질병과 관련되어 알려져 있다. 그러나 프리온은 동일한 단백질의 다른 형태를 감염성 형태로 전환시키는 능력을 가진 단백질로 정의되기도 한다. 이러한 관점에서 프리온은 유전체의 변형 없이 표현형 변화를 유도하는 후성유전학적 인자로 간주될 수 있다.[69]
곰팡이 프라이온은 프라이온에 의해 유발된 감염성 표현형이 유전체의 변형 없이 상속될 수 있기 때문에 후성유전학적 현상으로 여겨진다. 효모에서 발견된 PSI+와 URE3는 이러한 유형의 프라이온 중 가장 잘 연구된 예시이다.[70][71]
세균의 DNA 메틸화:진정세균은 DNA 메틸화를 후성유전학적 제어에 사용하지만, 시토신이 아닌 아데닌을 메틸화 대상으로 한다. DNA 아데닌 메틸화는 대장균, 살모넬라속, 비브리오속, 예르시니아속, 헤모필루스속, 브루셀라속 등의 생물체 내 세균의 병원성에서 중요해진다.[283]
진핵생물 후성유전학적 기작 비교:
4. 연구 분야
후성유전학은 발생 과정이 끝난 성체에서 발생하는 유전자 발현 조절의 변화와 유전체 변화를 연구하는 분야이다. 특히 암과 같은 질병 연구가 활발하게 이루어지고 있다.[330]
DNA (예: 시토신 메틸화 및 하이드록시메틸화) 또는 히스톤 단백질 (예: 라이신 아세틸화, 라이신 및 아르기닌 메틸화, 세린 및 트레오닌 인산화, 라이신 유비퀴틴화 및 수모화)의 공유 결합 변형은 여러 유형의 후성 유전적 유전에서 중심적인 역할을 한다. 염색질 리모델링은 항상 유전되는 것은 아니며, 모든 후성 유전적 유전이 염색질 리모델링을 포함하는 것은 아니다.[25]
세포 또는 개체의 표현형은 어떤 유전자가 전사되는지에 의해 영향을 받기 때문에, 유전 가능한 전사 상태는 후성 유전적 영향을 일으킬 수 있다. 유전자 발현에는 여러 층의 조절이 존재하며, 유전자가 조절되는 한 가지 방법은 염색질 리모델링을 통한다. 염색질은 DNA와 DNA가 결합하는 히스톤 단백질의 복합체이다. DNA가 히스톤 주변에 감기는 방식이 변경되면 유전자 발현도 변경될 수 있다. 염색질 리모델링은 두 가지 주요 메커니즘을 통해 수행된다.
# 히스톤 단백질을 구성하는 아미노산의 번역 후 변형. 히스톤 단백질은 긴 아미노산 사슬로 구성되어 있으며, 사슬 내의 아미노산이 변경되면 히스톤의 모양이 수정될 수 있다. DNA는 복제 과정에서 완전히 풀리지 않으므로 수정된 히스톤이 DNA의 각 새로운 복사본으로 전달될 수 있다. 이러한 변형된 히스톤은 주변의 히스톤 모양을 변경하여 세포 분열 후 계통 특이적 전사 프로그램을 유지하도록 돕는다.
# DNA에 메틸기를 첨가하는 것. 대부분 CpG 부위에 위치하여 시토신을 5-메틸시토신으로 변환한다. 5-메틸시토신은 이중 가닥 DNA에서 구아닌과 쌍을 이루면서 일반적인 시토신과 거의 동일하게 작용한다. 그러나 메틸화된 시토신이 유전자의 프로모터 및 인핸서 영역의 CpG 부위에 존재하면 해당 유전자는 종종 억제된다.[27][28] 메틸화된 시토신이 유전자 몸체의 CpG 부위에 존재하면 유전자 발현이 종종 증가한다. 유전자 전사는 일반적으로 해당 유전자의 프로모터 영역과 상호 작용하는 인핸서의 인식 서열에 결합하는 전사 인자에 의존한다.[29] 인식 서열에 메틸화된 시토신이 있으면 전사 인자의 약 22%가 결합을 억제받는다. 또한, 프로모터 영역에 메틸화된 시토신이 존재하면 메틸-CpG 결합 도메인 (MBD) 단백질을 끌어들일 수 있다. 모든 MBD는 뉴클레오솜 리모델링 및 히스톤 탈아세틸화 효소 복합체와 상호 작용하여 유전자 침묵을 유도한다. 또한, 메틸화된 시토신과 관련된 또 다른 공유 결합 변형은 TET 효소에 의한 탈메틸화이다. 이러한 탈메틸화는, 예를 들어 뉴런에서 학습과 기억 형성 과정에서 수백 번 발생한다.[30][31]
DNA 메틸화와 히스톤 라이신 메틸화 사이에는 빈번하게 상호 관계가 존재하며,[32] DNMT3A와 DNMT3B에 의해 수행되는 DNA 메틸화와 히스톤 메틸화 사이에는 더 많은 상호작용이 있어, DNA 메틸화와 히스톤 메틸화의 게놈 전체 분포 사이에 상관관계가 존재한다.[33]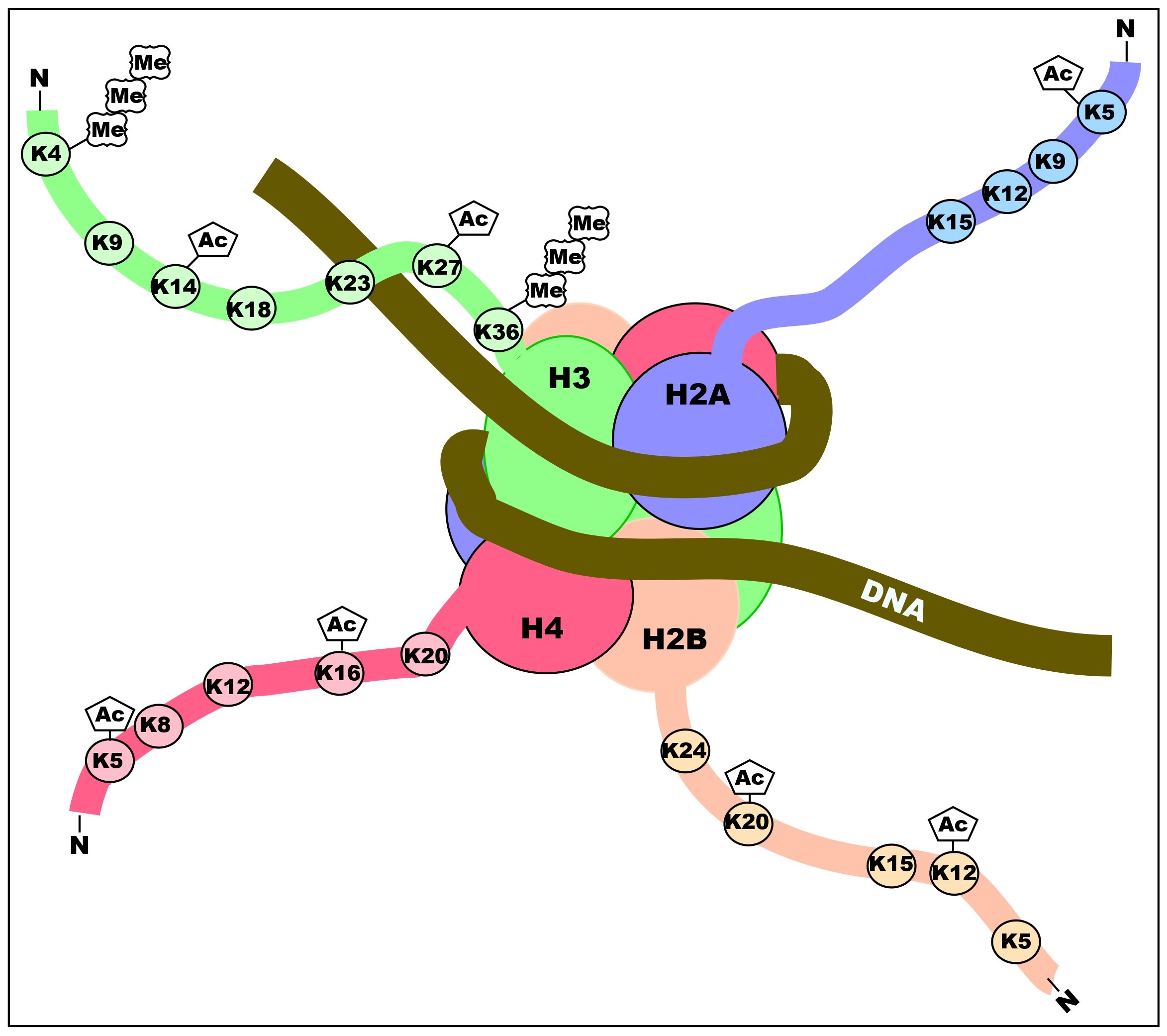
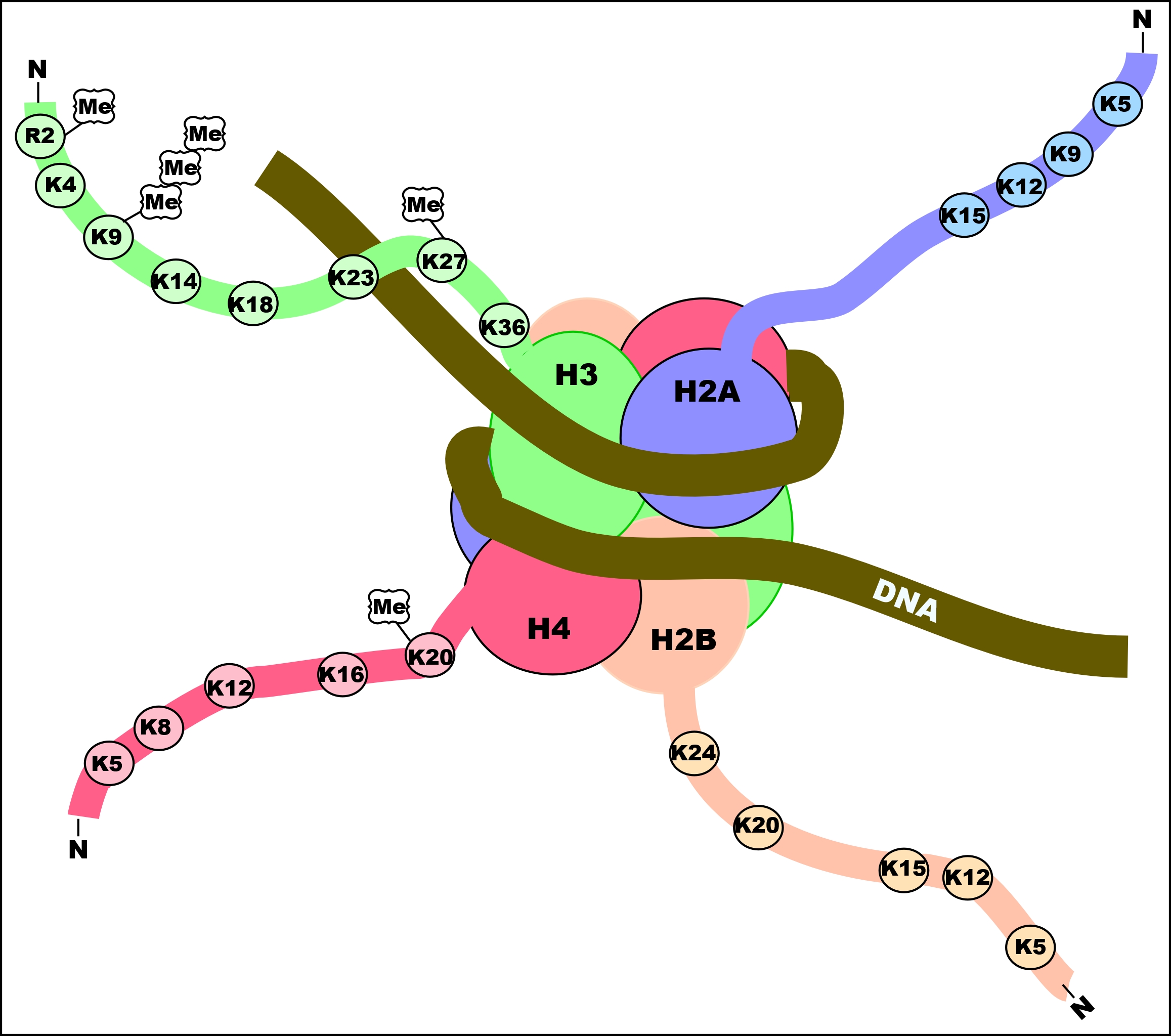
히스톤 변형은 전체 서열에서 발생하지만, 히스톤의 비구조적 N-말단 (히스톤 꼬리)이 특히 높은 변형을 보인다. 이러한 변형에는 아세틸화, 메틸화, 유비퀴틴화, 인산화, 수모화, 리보실화 및 시트룰린화가 포함된다. 아세틸화는 이러한 변형 중에서 가장 많이 연구되었다. 예를 들어, 히스톤 아세틸전달효소 (HAT) 효소에 의한 히스톤 H3 꼬리의 K14 및 K9 라이신의 아세틸화는 일반적으로 전사 능력과 관련이 있다[35] (그림 참조).
히스톤 라이신 메틸전달효소 (KMT)가 히스톤 H3 & H4 패턴에서 이러한 메틸화 활성에 책임이 있는 것으로 나타났다. 이 효소는 SET 도메인이라는 촉매 활성 부위를 사용한다. SET 도메인은 유전자 활성을 조절하는 데 관여하는 130개의 아미노산 서열이다. 이 도메인은 히스톤 꼬리에 결합하여 히스톤의 메틸화를 유발하는 것으로 입증되었다.[37]
서로 다른 히스톤 변형은 서로 다른 방식으로 기능할 가능성이 높다. 한 위치에서의 아세틸화는 다른 위치에서의 아세틸화와 다르게 기능할 가능성이 높다. 또한, 여러 변형이 동시에 발생할 수 있으며, 이러한 변형은 함께 작용하여 뉴클레오솜의 동작을 변경할 수 있다.
DNA 메틸화는 반복 서열에서 자주 발생하며, '이동성 유전자'의 발현과 이동성을 억제하는 데 도움이 된다.[38] 5-메틸시토신은 자발적으로 탈아미노화(질소를 산소로 치환)되어 티미딘으로 변환될 수 있기 때문에 CpG 부위는 빈번하게 돌연변이를 일으키며, CpG 섬을 제외하고는 유전체에서 희귀해진다. CpG 섬에서는 메틸화되지 않은 상태로 유지된다.
히스톤 H3와 H4는 히스톤 리신 탈메틸화 효소(KDM)를 사용하여 탈메틸화를 통해 조작될 수 있다. 이 효소는 주몬지 도메인(JmjC)이라고 불리는 촉매 활성 부위를 가지고 있다. 탈메틸화는 JmjC가 여러 보조 인자를 사용하여 메틸기를 수산화하여 제거될 때 발생한다. JmjC는 모노-, 디-, 및 트리-메틸화된 기질을 탈메틸화할 수 있다.[48]
염색체 영역은 DNA 서열의 변화 없이 이중 안정적인 유전자 발현을 초래하는 안정적이고 유전 가능한 대체 상태를 채택할 수 있다. 후성 유전적 제어는 종종 히스톤의 대체 공유 결합 변형과 관련이 있다.[49]
작은 RNA의 효과에 의해 크로마틴 기반 전사 조절이 매개될 수 있다는 주장이 제기되었다. 작은 간섭 RNA는 표적 프로모터의 후성 유전적 조절을 통해 전사적 유전자 발현을 조절할 수 있다.[53]
마이크로 RNA(miRNA)는 길이가 17~25 뉴클레오타이드인 비암호 RNA의 일종으로, 식물과 동물에서 다양한 생물학적 기능을 조절한다.[56] 세포에서 발현되는 각 miRNA는 약 100~200개의 메신저 RNA(mRNA)를 표적으로 하여 하향 조절한다.[58] mRNA의 하향 조절은 대부분 표적 mRNA의 분해를 유발하여 발생하며, 일부 하향 조절은 단백질로의 번역 수준에서 발생한다.[59] 인간 단백질 암호 유전자의 약 60%가 miRNA에 의해 조절되는 것으로 보이며,[60] 많은 miRNA는 후생 유전학적으로 조절된다. miRNA 유전자 중 약 50%는 CpG 섬과 관련이 있으며,[56] 이는 후생 유전적 메틸화에 의해 억제될 수 있다.
sRNA는 세균에서 발견되는 작고(50–250 뉴클레오티드), 구조가 복잡하며, 비번역 RNA 조각이다. 이들은 병원체의 독성 유전자를 포함한 유전자 발현을 조절하며, 약물 내성 세균과의 싸움에서 새로운 표적으로 간주된다.[64]
수많은 연구에서 장비 부호화 RNA(lncRNA)가 유전자 발현 조절과 염색체 변형에 중추적인 역할을 하여 세포 분화에 중요한 영향을 미친다는 것을 보여주었다.
프라이온은 감염성 단백질 형태이다. 일반적으로 단백질은 독특한 세포 기능을 수행하는 개별 단위로 접히지만, 일부 단백질은 프라이온이라고 알려진 감염성 컨포메이션 상태를 형성할 수도 있다. 곰팡이 프라이온은 프라이온에 의해 유발된 감염성 표현형이 유전체의 변형 없이 상속될 수 있기 때문에 일부 사람들은 이를 후성 유전적이라고 간주한다.
DNA 손상은 후성 유전적 변화를 일으킬 수 있다.[83][84][85] DNA 손상은 인체 세포 하나당 하루 평균 약 60,000번 정도 발생하며, 대부분 복구되지만 DNA 복구 부위에 후성 유전적 변화가 남을 수 있다.[86] 특히, DNA 이중 가닥 절단은 DNA 메틸화를 유발하고, 침묵 유형의 히스톤 변형(크로마틴 리모델링)을 촉진하여 계획되지 않은 후성 유전적 유전자 침묵을 시작할 수 있다.[87]
DNA 메틸화는 유전자 전사의 중요한 조절 인자이며, 사람의 많은 악성 종양에서는 정상 조직과 다른 과잉 메틸화 또는 저메틸화가 발견된다.
후성유전학 연구는 후성유전학적 현상에 대한 이해를 높이기 위해 광범위한 분자 생물학 기법을 사용한다. 이러한 기법에는 염색질 면역침강법 (대규모 변형인 칩온칩 및 칩-시퀀싱과 함께), 형광 현미경 면역 염색법, 메틸화에 민감한 제한 효소, DNA 아데닌 메틸전달효소 식별 (DamID) 및 바이설파이트 시퀀싱이 포함된다.[114] 또한, 생물정보학 방법의 사용은 계산 후성유전학에서 역할을 한다.[114]
4. 1. 발생 및 분화
인간의 인간 유전체에는 'CpG'라는 이중 염기서열이 다량으로 존재하며, 이중 약 70%에 이르는 CpG의 사이토신 염기에는 메틸기(-CH3)가 결합되어 있는데, 이를 ‘DNA 메틸화’라고 부른다. 이러한 DNA 메틸화 현상은 유전체의 각종 반복 서열 등에서 흔히 관찰되며, 이는 유전체의 안정성 유지 등에 중요한 역할을 하고 있는 것으로 보고 있다. 한편 각종 유전자의 상단 5’ 조절부위에 CpG가 밀집된 독특한 영역이 존재하는데 이를 'CpG 섬'이라고 하며, 이 경우 CpG의 사이토신은 대부분 메틸기가 결합되어 있지 않다. 그러나 경우에 따라서 시토신 메틸화가 발생하며 이 부위 뉴클레오솜의 히스톤 분자들과의 상호작용을 통해 크로마틴의 구조에 변화를 일으켜 결국 유전자 발현에 영향을 주게 된다. 따라서 유전자의 발현은 DNA 메틸화 및 히스톤 변형 등과 같은 화학적 가역반응에 의해 조절된다고 할 수 있는데, 이와 같이 DNA 염기서열의 변화 없이 크로마틴의 구조적 변화, ‘크로마틴 리모델링’에 영향을 주어 유전자 발현이 조절되는 기전에 관한 연구 분야를 ‘후성유전학’(Epigenetics)이라고 한다.[319]
후성유전적 변화는 DNA의 유전자 암호 서열이 아닌 특정 유전자의 활성을 수정한다.[78] DNA 자체의 미세 구조(암호가 아님) 또는 관련된 크로마틴 단백질이 수정되어 활성화 또는 침묵을 유발할 수 있다. 이러한 메커니즘을 통해 다세포 생물의 분화된 세포는 자체 활동에 필요한 유전자만 발현할 수 있다. 후성유전적 변화는 세포 분열 시 보존된다. 대부분의 후성유전적 변화는 한 개체 유기체의 평생 동안에만 발생하지만, 이러한 후성유전적 변화는 세대 간 후성유전적 유전이라는 과정을 통해 유기체의 자손에게 전달될 수 있다. 게다가, 수정으로 이어지는 정자 또는 난세포에서 유전자 비활성화가 발생하면, 이러한 후성유전적 수정이 다음 세대로 전달될 수도 있다.[79]
특정 후성유전적 과정에는 파라뮤테이션, 북마킹, 각인, 유전자 침묵, X 염색체 불활성화, 위치 효과, DNA 메틸화 재프로그래밍, 전위, 모성 효과, 발암의 진행, 많은 기형유발물질의 영향, 히스톤 변형 및 이질염색질의 조절, 그리고 처녀생식 및 복제에 영향을 미치는 기술적 제한이 포함된다.[80][81][82]
배아 발생을 포함한 초기 사건은 후성유전학적 기전을 통해 발달, 인지 및 건강 결과에 영향을 미칠 수 있다.[148]
발달 후생유전학은 미리 결정된 후생 발생과 확률적 후생 발생으로 나눌 수 있다. 미리 결정된 후생 발생은 DNA의 구조적 발달에서 단백질의 기능적 성숙으로의 단방향적인 움직임이다. 여기서 "미리 결정된"은 발달이 각본화되고 예측 가능하다는 것을 의미한다. 반면에 확률적 후생 발생은 경험과 외부의 형성 발달을 동반하는 양방향적인 구조-기능 발달이다.[156]
체세포 후생 유전적 유전, 특히 DNA와 히스톤 공유 결합 변형 및 뉴클레오솜 재배치를 통해, 다세포 진핵생물의 발달에 매우 중요하다.[126] 게놈 서열은 정적이지만 (몇 가지 주목할 만한 예외가 있음), 세포는 여러 다른 유형으로 분화되어 서로 다른 기능을 수행하고 환경 및 세포 간 신호에 다르게 반응한다. 따라서 개체가 발달함에 따라 형태 형성 물질은 후생 유전적으로 유전 가능한 방식으로 유전자를 활성화하거나 침묵시켜 세포에 기억을 부여한다. 포유류에서는 대부분의 세포가 최종적으로 분화되어, 몇 가지 세포 유형("전능성" 및 "다능성")으로 분화할 수 있는 능력을 가진 줄기 세포만 남는다. 포유류에서는 일부 줄기 세포가 평생 동안 새로 분화된 세포를 계속 생성하는데, 예를 들어 신경 발생이 이에 해당하지만, 포유류는 일부 조직의 손실에 반응할 수 없으며, 예를 들어 다른 동물은 가능한 사지 재생 능력이 없다. 후생 유전적 변형은 신경 줄기 세포에서 신경 교세포 전구 세포로의 전환을 조절한다(예: 올리고덴드로사이트로의 분화는 히스톤의 탈아세틸화 및 메틸화에 의해 조절된다).[157] 동물과 달리 식물 세포는 최종적으로 분화되지 않고, 새로운 개체 식물을 생성할 수 있는 능력을 가진 전능성을 유지한다. 식물은 크로마틴 리모델링과 같이 동물과 동일한 후생 유전적 메커니즘을 많이 사용하지만, 일부 종류의 식물 세포는 "세포 기억"을 사용하거나 필요로 하지 않고, 환경과 주변 세포의 위치 정보를 사용하여 유전자 발현 패턴을 재설정하여 운명을 결정한다고 가정되어 왔다.[158]
후생 유전적 변화는 환경 노출에 반응하여 발생할 수 있다. 예를 들어, 제니스테인 (250mg/kg)으로 보충된 어미의 식이 요법은 아구티 유전자의 발현에 영향을 미치는 후생 유전적 변화를 일으켜 털 색깔, 체중, 암 발생 경향에 영향을 미친다.[159][160][161] 진행 중인 연구는 당뇨병성 배아병증과 같은 다른 알려진 기형 유발 물질의 메틸화 지표에 미치는 영향을 탐구하는 데 중점을 두고 있다.[162]
다세포 생물의 발생에서, 몇몇 예외를 제외하고 DNA 염기 서열 자체는 변하지 않지만, 세포는 서로 다른 종류로 분화하며, 환경 또는 세포 간 신호에 대해 서로 다른 반응을 한다. 개체가 발생할 때, 형태 형성 인자는, 후성 유전적인 방법으로 세포에 "기억"을 부여하면서, 유전자를 활성화 또는 비활성화한다.[244]
플라나리아나 불가사리류처럼 단편에서 개체를 재생할 수 있는 동물도 있는 반면, 포유류처럼 분화 후의 세포는 분화능을 잃는 동물도 있다. 분화능의 소실은 세포의 경력을 반영한 후성 유전적인 변화이다. 식물은 동물과 마찬가지로 후성 유전적인 메커니즘을 많이 이용하고 있다. 그러나, 식물 세포는 포유류 등과는 달리, 분화 후의 조직도 전능성을 유지하고 있다. 이로부터, 어떤 종류의 식물 세포는, 주변 환경 및 위치 정보를 이용하여, 지금까지의 세포 기억을 사용하지 않도록 전환할 수 있다는 가설을 제시하는 연구자도 있다.[262]
포유류의 발생과 관련된 후성 유전적인 기구의 대표적인 예로, X 염색체 비활성화, 게놈 임프린팅, 리프로그래밍 (초기화·재프로그램)에 의한 분화능의 재획득이 꼽힌다.
포유류에서는 성염색체인 X 염색체의 수가 암수에서 다르다(암컷 2개, 수컷 1개). 수컷은 1개의 X 염색체만으로 생존에 필요한 유전자 발현을 유지한다. 이에 비해 암컷은 2개의 X 염색체가 모두 활성을 유지하면 유전자 발현이 과도해져 배아 발생 초기(착상 직후)에 사망한다. 이를 피하기 위한 유전자량 보상으로, 2개 이상의 X 염색체를 가진 개체는, 1개의 X 염색체의 활성을 남기고 다른 X 염색체의 유전자 발현을 억제한다. 이때 불활성화되는 염색체는 조건적 헤테로크로마틴이 되어, 분열기가 아니더라도 현미경 관찰이 가능한 형태를 취한다(바 소체). X 염색체 불활성화에서는, 후생 유전적 기작으로 DNA 메틸화, 히스톤 변형(H3K27 트리메틸화 외), 특이적인 비번역 RNA (''Xist'')의 전사 및 염색체 결합이 동시에 관여한다.
포유류에서는 배우자 형성 과정에서 수컷과 암컷의 성별에 따른 특이적인 DNA 메틸화가 일어난다. 이 DNA 메틸화는 배우자 게놈에서 수정란으로 이어져, 수정 후 개체에서 부계 유전자와 모계 유전자의 사용이 구분된다. 수컷과 암컷 각각의 임프린팅을 받는 유전자(임프린트 유전자)는 동일한 염색체 영역에 집중되어 편재하며, 클러스터를 형성하고 있다. 유전자가 임프린트되는 의미에 대해서는 아직 밝혀지지 않았지만, 배아 발생 시에 수컷과 암컷 양쪽의 유전자가 필요하다. 따라서 포유류에서는 자연 조건에서의 단성 생식이 불가능하다. 한편, 임프린팅 상태를 인위적으로 조작하여 암컷 게놈만으로 단성 발생한 생쥐가 만들어졌다.
다세포 생물의 세포는 후성 유전적 상태의 계승에 의해 특이적인 기능을 유지하지만, 다른 종류의 세포가 되는 분화능이 제한되는 경우가 있다. 세포(세포핵)가 그 동안 계승·축적해 온 후성 유전적 표식을 소거·재구성하고, 분화능을 되찾는 것을 리프로그래밍(재 프로그래밍화·초기화)이라고 부른다.
양서류의 경우, 1950년대에는 배아 세포의 핵을, 1960년대에는 체세포의 핵을 제거한 난자에 이식하여 발생시켜 복제 개체를 얻을 수 있었다. 이러한 연구들은 이식을 통해 세포핵이 리프로그래밍된다는 것을 보여준다. 한편, 포유류에서도 핵 이식 복제 연구가 시도되었지만, 1980년대에 수행된 생식세포 핵 이식에서는 발생이 멈추고, 수컷 게놈 또는 암컷 게놈 단독으로는 발생이 불가능하다는 것이 시사되었다. 이로 인해 포유류에서의 게놈 임프린팅 기전이 발견되었다.
1997년에는 체세포 핵 이식에 의한 복제 양 돌리의 탄생이 보고되었고, 이후 다른 포유류에서도 체세포 복제 개체 제작이 잇따랐다. 하지만, 체세포 복제는 개체 제작 효율이 수 퍼센트 이하로 낮고, 탄생한 복제 개체에서 이상이 관찰되는 것이 문제시되고 있다. 또한, 배아줄기세포 (ES 세포) 유래의 ES 복제에서도 표현형 이상이 관찰되고 있다. 이러한 복제 개체의 표현형 이상은 대부분 유성 생식에 의해 후대에 전달되지 않으며, 즉 생식세포에서의 리프로그래밍이 일어나기 때문에, 주로 후성 유전적 요인에 의한 것으로 생각되고 있다. 체세포 복제에서는 임프린팅 부분을 제외한 리프로그래밍 불완전이 개체 이상을 일으키고, ES 복제의 경우에는 게놈 임프린팅의 불량으로 인해 개체 이상이 일어나는 것으로 생각된다.
재생 의학에서 인공 다능성 줄기 세포(iPS 세포)·배아 줄기 세포 등을 이용한 기관 회복 연구가 진행되고 있다. 체세포 유래 iPS 세포는 후성 유전학적으로 볼 때, 수 종류의 유전자 도입에 의한 인위적인 리프로그래밍을 통해 만능성을 복원시킨 세포이다.
4. 2. 질병 연구
인간의 인간 유전체에는 'CpG'라는 이중 염기서열이 다량으로 존재하며, 이중 약 70%에 이르는 CpG의 사이토신 염기에는 메틸기(-CH3)가 결합되어 있는데, 이를 ‘DNA 메틸화’라고 부른다. 이러한 DNA 메틸화 현상은 유전체의 각종 반복 서열 등에서 흔히 관찰되며, 이는 유전체의 안정성 유지 등에 중요한 역할을 한다.[319] 유전자 상단 5’ 조절 부위에 CpG가 밀집된 독특한 영역은 'CpG 섬'이라고 하며, 이 경우 CpG의 사이토신은 대부분 메틸기가 결합되어 있지 않다. 그러나 시토신 메틸화가 발생하면 이 부위 뉴클레오솜의 히스톤 분자들과의 교감을 통해 크로마틴 구조에 변화를 이끌어 결국 유전자 발현에 영향을 준다.[319]후성유전학은 발생 과정이 끝난 성체에서 발생하는 유전자 발현 조절의 변화와 유전체 변화를 연구하며, 특히 암과 같은 질병 연구가 활발히 이루어지고 있다.[330]
DNA 손상은 후성 유전적 변화를 일으킬 수 있다.[83][84][85] DNA 손상은 인체 세포 하나당 하루 평균 약 60,000번 정도 발생하며(자연 발생 DNA 손상 참조), 대부분 복구되지만 DNA 복구 부위에 후성 유전적 변화가 남을 수 있다.[86] 특히, DNA 이중 가닥 절단은 DNA 메틸화를 유발하고, 침묵 유형의 히스톤 변형(크로마틴 리모델링)을 촉진하여 계획되지 않은 후성 유전적 유전자 침묵을 시작할 수 있다.[87]
DNA 메틸화는 유전자 전사의 중요한 조절 인자이며, 사람의 많은 악성 종양에서는 정상 조직과 다른 과잉 메틸화 또는 저메틸화가 발견된다. 저메틸화는 게놈의 넓은 범위에서 관찰되며, 게놈·염색체의 불안정화를 통해 발암에 영향을 미치는 것으로 생각된다. 임프린팅에 의한 불활성 상태 유전자에 대한 DNA 탈메틸화는 해당 유전자를 활성화시켜 대장암 발생에 관여한다.
과잉 메틸화는 주로 암 억제 유전자프로모터 영역의 CpG 아일랜드 메틸화를 통해 발암에 관여한다. 이 과잉 메틸화 패턴은 세포 분열에서 높은 정확도로 딸 세포에 계승되며, 메틸화된 프로모터 영역은 암 억제 유전자의 전사 수준에서 유전자 침묵을 초래한다.
4. 3. 세대 간 후성유전
후성 유전학적 기작은 세포 분화의 진화적 기원의 필수적인 부분이었다.[168] 다세포 생물에서 후성 유전학은 일반적으로 분화와 관련된 기작으로 여겨지며, 유기체가 번식할 때 후성 유전적 패턴이 "재설정"되지만, 세대 간 후성 유전적 유전의 몇 가지 관찰이 있었다(예: 옥수수에서 관찰된 파라뮤테이션 현상). 이러한 다세대 후성 유전적 형질의 대부분은 여러 세대에 걸쳐 점차적으로 소실되지만, 다세대 후성 유전학이 진화와 적응의 또 다른 측면이 될 가능성은 남아있다.일부 학자들은 후성 유전학을 유전 가능한 것으로 정의한다.
격리된 생식 계열 또는 바이스만 장벽은 동물에게 특유하며, 후성 유전적 유전은 식물과 미생물에서 더 흔하다. 에바 야블론카, 마리온 J. 램과 에티엔 단친은 이러한 효과가 현대 종합의 표준 개념적 틀에 대한 개선을 필요로 할 수 있으며 확장된 진화 종합을 요구해왔다.[169][170][171] 존 메이너드 스미스와 같은 다른 진화 생물학자들은 후성 유전적 유전을 집단 유전학 모델에 통합했거나,[172] 확장된 진화 종합에 대해 공개적으로 회의적이다(마이클 린치).[173] 토마스 디킨스와 카지 라흐만은 DNA 메틸화 및 히스톤 변형과 같은 후성 유전학적 기작이 자연 선택의 통제하에 유전적으로 유전되며 따라서 이전의 "현대 종합"에 부합한다고 말한다.[174]
후성 유전적 유전이 전통적인 유전적 유전과 다를 수 있으며 진화에 중요한 결과를 가져오는 두 가지 중요한 방식은 다음과 같다.
식물에서, 유전 가능한 DNA 메틸화 돌연변이는 DNA 돌연변이가 발생할 가능성보다 100,000배 더 높다.[177] PSI+ 시스템과 같은 후성 유전적으로 유전된 요소는 "대체 수단" 역할을 할 수 있으며, 돌연변이 및/또는 재조합이 적응적 표현형 변화를 유전자 동화할 수 있을 정도로 오랫동안 계통이 생존할 수 있도록 단기 적응에 충분하다.[178] 이러한 가능성의 존재는 종의 진화 가능성을 증가시킨다.
원핵생물, 식물 및 동물을 포함한 광범위한 유기체에서 100개 이상의 세대 간 후성 유전 현상이 보고되었다.[179] 예를 들어, 애도 나비는 다양한 온도의 실험에 반응하여 호르몬 변화를 통해 색상을 변경한다.[180]
사상균인 ''Neurospora crassa''는 시토신 메틸화의 제어 및 기능을 이해하기 위한 주요 모델 시스템이다. 이 유기체에서 DNA 메틸화는 RIP(반복 유도 점 돌연변이)라고 하는 유전자 방어 시스템의 유물과 관련이 있으며, 전사 신장을 억제하여 유전자 발현을 침묵시킨다.[181]
효모 프리온 PSI는 번역 종결 인자의 컨포메이션 변화에 의해 생성되며, 이는 딸 세포에 의해 유전된다. 이것은 불리한 조건에서 생존 이점을 제공할 수 있으며, 단세포 유기체가 환경 스트레스에 신속하게 반응할 수 있도록 하는 후성 유전적 조절의 예를 보여준다. 프리온은 유전체 변형 없이 표현형 변화를 유도할 수 있는 후성 유전학적 작용제로 볼 수 있다.[182]
미생물에서 후성 유전학적 표지의 직접적인 감지는 단일 분자 실시간 시퀀싱을 통해 가능하며, 여기서 중합 효소 민감성은 DNA 분자가 시퀀싱되는 동안 메틸화 및 기타 변형을 측정할 수 있게 해준다.[183] 여러 프로젝트에서 박테리아에서 유전체 전체 후성 유전학적 데이터를 수집하는 능력을 입증했다.[184][185][186][187]
5. 의학적 응용
후성유전학은 의학적으로 다양하게 응용될 수 있다.[192] 환경 후성유전학 연구에는 일란성 쌍둥이를 직접 비교하는 것이 적합한 모델이다. 어린 일란성 쌍둥이는 후성유전학적으로 구별하기 어렵지만, 나이가 들면서 5-메틸시토신 DNA와 히스톤 아세틸화 함량 및 분포에서 큰 차이를 보인다.[11] 특히 평생을 함께 보낸 시간이 적거나 건강 기록에 큰 차이가 있는 쌍둥이에게서 5-메틸시토신 DNA와 히스톤 H3 및 H4의 아세틸화 수준 차이가 가장 컸다.[193]
고속 처리량 스크리닝 연구는 40쌍의 일란성 쌍둥이를 대상으로 DNA 메틸화와 히스톤 변형의 전반적, 특정 위치 변화를 비교하여 후성유전학적 차이에 주목했다.[193] 3세에서 74세까지 다양한 연령대의 건강한 쌍둥이를 대상으로 한 이 연구에서는 쌍둥이 형제 간에 연령에 따른 후성유전학적 차이가 축적되는 "후성유전학적 표류" 현상이 나타났다. 이는 나이가 들면서 후성유전학적 변형이 발생함을 의미한다. 노화는 질병의 위험 요소이지만, 연령 관련 메틸화는 유전체의 특정 부위에서 다르게 발생하여 시간이 지나면서 생물학적 연령과 생활 연령 사이에 차이가 생길 수 있다. 후성유전학적 변화는 생활 방식 (사회 과학)을 반영하며, 임상 참고 범위에 도달하기 전에 질병의 기능적 바이오마커로 작용할 수 있다.[197]
최근 연구에서는 114쌍의 일란성 쌍둥이와 80쌍의 이란성 쌍둥이에게서 약 6000개 유전체 영역의 DNA 메틸화 상태를 분석했다. 그 결과, 배반포 분열 시점의 후성유전학적 유사성이 일란성 쌍둥이의 표현형 유사성에 영향을 줄 수 있다는 결론을 내렸다. 이는 초기 배아 발달 단계의 미세 환경 (생물학)이 후성유전학적 표지 형성에 중요할 수 있음을 보여준다.[194]
오버칼릭스 연구에 따르면, 19세기에 기아를 경험한 스웨덴 남성의 아버지 쪽(어머니 쪽이 아닌) 손자들은[201] 심혈관 질환으로 사망할 확률이 낮았다. 반면 음식이 풍족한 경우에는 손자들의 당뇨병 사망률이 증가했는데, 이는 세대 간 후성 유전적 유전 현상으로 해석된다.[202] 여성의 경우, 자궁에 있을 때(난자 형성 시기) 기아를 겪은 여성의 아버지 쪽(어머니 쪽이 아닌) 손녀들은 평균 수명이 짧았다.[203]
중독은 전사 및 신경후성유전학적 기전을 통해 발생하는 뇌의 보상 시스템 질환이며, 모르핀, 코카인, 성관계, 도박과 같은 중독성 자극에 만성적으로 높은 수준으로 노출되어 시간이 지남에 따라 발생한다.[209][210][211] 전임상 연구에서는 중독 표현형의 세대 간 후성유전적 유전이 나타났다.[212][213]
후성유전학적 과정은 DNA, RNA, 단백질의 각 단계에서 작용하기 때문에 의학적 응용에 있어 많은 잠재적 가능성을 가지고 있다.[266] 1989년에는 게놈 임프린팅이 단친성 이염색체증에 의해 선천성 유전 질환에 영향을 미치는 예가 보고되면서, 후성유전학적 과정과 질환이 처음으로 직접 관련지어졌다. 이후, 크로마틴의 유전자 제어 이상을 통해 영향을 받는 레트 증후군과 같은 유전 질환에 대한 연구도 진행되고 있다. 한편, 후천적 요인도 영향을 미치는 암, 알레르기 질환, 비만[267] 등과의 관련성에 대해서도 연구가 이루어지고 있다.
5. 1. 진단 및 치료
후성유전학은 다양하고 잠재적인 의학적 응용 분야를 가지고 있다.[192]베타-락탐 항생제는 글루탐산 수용체 활성 및 사이클로스포린의 여러 전사 인자에 대한 작용을 변경할 수 있다. 리튬은 비정상적인 단백질의 자가소멸에 영향을 미칠 수 있으며, 아편유사제는 만성적인 사용을 통해 중독성 표현형과 관련된 유전자 발현을 증가시킬 수 있다.[204]
중독은 전사 및 신경후성유전학적 기전을 통해 발생하는 뇌의 보상 시스템 질환으로, 중독성 자극(예: 모르핀, 코카인, 성관계, 도박)에 만성적으로 높은 수준으로 노출됨으로써 시간이 지남에 따라 발생한다.[209][210][211]
플루오로퀴놀론 항생제는 철 킬레이션을 통해 포유류 세포에서 후성 유전적 변화를 유도하는데, 이는 철을 보조 인자로 요구하는 α-케토글루타르산 의존적 디옥시게나제의 억제를 통해 후성 유전적 효과를 유발한다.[215]
다양한 약리학적 제제가 유도만능줄기세포(iPSC)를 생성하거나 후성 유전적 접근 방식을 통해 배아줄기세포(ESC) 표현형을 유지하는 데 사용된다. 골수 줄기 세포와 같은 성체 줄기 세포는 G9a 히스톤 메틸전달효소 억제제 BIX01294로 처리하면 심장 적합 세포로 분화할 가능성을 보여주었다.[216][217]
세포 가소성은 후성 유전적 변화를 필요로 한다. 이는 상피-간엽 변환 동안 암세포의 세포 가소성[218]과 대식세포와 같은 면역 세포에서 관찰되었다.[219]
후성유전학적 의약품은 방사선 치료나 화학 요법 등 현재 받아들여지고 있는 치료법을 대체하거나 보조하는 치료법일 수 있으며, 최근 연구는 현재 치료법의 효과를 높일 수 있다는 것을 보여준다.[279]
주로 히스톤 아세틸기 전이 효소(HAT)와 히스톤 탈아세틸화 효소(HDAC)에 초점을 맞춰 의약품 개발이 진행되고 있다.[281] HDAC 억제제인 의약품 보리노스타트는 이미 실용화되었다.[282]
5. 2. 유전체 각인 관련 질환
유전체 각인은 포유류에서 부모가 생식 세포의 특정 유전체 위치에 대해 서로 다른 후성 유전적 패턴을 기여하는 현상이다.[199] 인간 질환에서 각인의 가장 잘 알려진 사례는 안젤만 증후군과 프래더-윌리 증후군인데, 이 두 가지 모두 동일한 유전자 돌연변이인 염색체 15q 부분 결실에 의해 발생할 수 있으며, 어떤 증후군이 발병하는지는 돌연변이가 아이의 어머니 또는 아버지로부터 유전되었는지에 따라 달라진다.[200]이 두 증후군과 관련된 염색체 영역은 15번 염색체 장완(15q)으로 동일하다. 이 위치에 게놈 임프린팅 영역이 존재하기 때문에, 그곳에 있는 유전자는 기능적으로 헤미접합형[272]이다. 따라서, 한쪽 부모의 염색체가 존재하지 않는 염색체 변이(염색체 결실 또는 단일 부모 염색체 이수성)가 발생하면, 부계 또는 모계 유전자가 전혀 발현되지 않는 상태가 되어 두 증후군 중 하나가 발병하게 된다.[273][274]
이 외에도 게놈 임프린팅의 이상과 관련이 지적되는 벡위드-비데만 증후군 (11번 염색체 영역, 11p15.5)이나 실버-러셀 증후군 등의 질환이 있으며, 3번 및 19번 염색체를 제외한 상염색체에서의 단일 부모 염색체 이수성이 알려져 있다.
5. 3. 후성유전체 편집(Epigenome editing)
mRNA/lncRNA 변형, DNA 메틸화 변형 및 히스톤 변형은 후성유전체 편집에서 변경되거나 사용될 수 있는 유전자 발현의 후성 유전적 조절에 포함된다.[220][221][222]재생 의학에서는 인공 다능성 줄기 세포(iPS 세포)·배아 줄기 세포 등을 이용한 기관 회복 연구가 진행 중이다. 체세포 유래 iPS 세포는 후성 유전학적으로 볼 때, 몇 가지 유전자 도입을 통해 인위적인 리프로그래밍을 거쳐 만능성을 회복시킨 세포이다.
참조
[1]
논문
Epigenetics: definition, mechanisms and clinical perspective
2009-09
[2]
뉴스
Beware the pseudo gene genies
https://www.theguard[...]
2015-07-19
[3]
논문
What do you mean, "epigenetic"?
2015-04
[4]
논문
Epigenetics in cancer
2010-01
[5]
논문
Epigenetic modifications in cancer
2012-04
[6]
논문
The Importance of ncRNAs as Epigenetic Mechanisms in Phenotypic Variation and Organic Evolution
2017
[7]
논문
Perceptions of epigenetics
2007-05
[8]
웹사이트
What genes remember
https://www.prospect[...]
2012-07-26
[9]
논문
Stability and flexibility of epigenetic gene regulation in mammalian development
2007-05
[10]
문서
Oxford English Dictionary
[11]
서적
The Developing Genome: An Introduction to Behavioral Epigenetics
Oxford University Press
2015
[12]
웹사이트
Overview
http://www.roadmapep[...]
2013-12-07
[13]
문서
Morange M. La tentative de Nikolai Koltzoff (Koltsov) de lier génétique, embryologie et chimie physique, J. Biosciences. 2011. V. 36. P. 211-214
[14]
논문
The epigenotype
[15]
문서
See preformationism for historical background. Oxford English Dictionary
[16]
서적
The Epigenetics of Birds
Cambridge University Press
2014
[17]
논문
In search of evolutionary developmental mechanisms: the 30-year gap between 1944 and 1974
2004-01
[18]
논문
Floral morphogenesis: stochastic explorations of a gene network epigenetic landscape
2008-11-03
[19]
논문
Branching and oscillations in the epigenetic landscape of cell-fate determination
2015-03
[20]
논문
DNA methylation and epigenetic inheritance
1990-01
[21]
서적
Epigenetic mechanisms of gene regulation
Cold Spring Harbor Laboratory Press
[22]
논문
Language: Disputed definitions
2008-10
[23]
논문
Epigenetics and gene expression
2010-07
[24]
논문
An operational definition of epigenetics
2009-04
[25]
논문
On the use of the word 'epigenetic'
2007-04
[26]
논문
Metabolic regulation of gene expression by histone lactylation
2019-10
[27]
논문
Epigenetics of Modified DNA Bases: 5-Methylcytosine and Beyond
2018
[28]
논문
The diverse roles of DNA methylation in mammalian development and disease
2019-10
[29]
논문
Transcription factors: from enhancer binding to developmental control
2012-09
[30]
논문
Experience-dependent epigenomic reorganization in the hippocampus
2017-07
[31]
논문
DNA Methylation and Establishing Memory
2022
[32]
논문
Understanding the relationship between DNA methylation and histone lysine methylation
2014-12
[33]
논문
The interplay between DNA and histone methylation: molecular mechanisms and disease implications
2021-05
[34]
논문
The role of histone tails in nucleosome stability: An electrostatic perspective
2020
[35]
논문
Relationship between histone H3 lysine 9 methylation, transcription repression, and heterochromatin protein 1 recruitment
2005-04
[36]
서적
Biotechnology in Medical Sciences
2014
[37]
논문
SET domain proteins modulate chromatin domains in eu- and heterochromatin
1998-01
[38]
논문
Transposable elements and the epigenetic regulation of the genome
2007-04
[39]
논문
Targeted mutation of the DNA methyltransferase gene results in embryonic lethality
1992-06
[40]
논문
The human DNA methyltransferases (DNMTs) 1, 3a and 3b: coordinate mRNA expression in normal tissues and overexpression in tumors
1999-06
[41]
논문
A targeting sequence directs DNA methyltransferase to sites of DNA replication in mammalian nuclei
https://epub.ub.uni-[...]
1992-11
[42]
논문
Human DNA-(cytosine-5) methyltransferase-PCNA complex as a target for p21WAF1
1997-09
[43]
논문
DNA methylation in health and disease
2000-10
[44]
논문
Role for DNA methylation in genomic imprinting
1993-11
[45]
논문
Analysis of human histone H2AZ deposition in vivo argues against its direct role in epigenetic templating mechanisms
2006-07
[46]
논문
Erwin Schroedinger, Francis Crick and epigenetic stability
2008-04
[47]
논문
Role of RNA modifications in cancer
2020-06
[48]
논문
Developmental roles of the histone lysine demethylases
2009-03
[49]
논문
Determination of enriched histone modifications in non-genic portions of the human genome
2009-03
[50]
논문
Ultrasensitive gene regulation by positive feedback loops in nucleosome modification
2008-04-15
[51]
웹사이트
Epigenetic cell memory
http://cmol.nbi.dk/m[...]
Cmol.nbi.dk
2012-07-26
[52]
논문
Theoretical analysis of epigenetic cell memory by nucleosome modification
2007-05
[53]
서적
RNA and the Regulation of Gene Expression: A Hidden Layer of Complexity
Caister Academic Press
[54]
논문
RNA regulation of epigenetic processes
2009-01
[55]
웹사이트
RNA can be hereditary molecule
http://www.the-scien[...]
2006-05-25
[56]
논문
Transcriptional and epigenetic regulation of human microRNAs
2013-04
[57]
웹사이트
Browse miRBase by species
http://www.mirbase.o[...]
[58]
논문
Microarray analysis shows that some microRNAs downregulate large numbers of target mRNAs
2005-02
[59]
논문
MicroRNA-target interactions: new insights from genome-wide approaches
2012-10
[60]
논문
Most mammalian mRNAs are conserved targets of microRNAs
2009-01
[61]
논문
Eukaryotic cytosine methyltransferases
[62]
논문
N6-methyladenosine in nuclear RNA is a major substrate of the obesity-associated FTO
2011-10
[63]
웹사이트
New research links common RNA modification to obesity
http://www.physorg.c[...]
Physorg.com
2012-07-26
[64]
논문
Analysis of the small RNA transcriptional response in multidrug-resistant Staphylococcus aureus after antimicrobial exposure
2013-08
[65]
웹사이트
sRNATarBase 2.0 A comprehensive database of bacterial SRNA targets verified by experiments
http://ccb.bmi.ac.cn[...]
[66]
웹사이트
Genomics maps for small non-coding RNA's and their targets in microbial genomes
http://srnamap.mbc.n[...]
2013-08-13
[67]
논문
Long-noncoding RNAs as epigenetic regulators in neurodegenerative diseases
[68]
논문
Examining parent-of-origin effects on transcription and RNA methylation in mediating aggressive behavior in honey bees (Apis mellifera)
2023-06
[69]
논문
Epigenetic inheritance and prions
[70]
논문
"[PSI], a cytoplasmic suppressor of super-suppression in yeast"
[71]
논문
Non-Mendelian mutation allowing ureidosuccinic acid uptake in yeast
1971-05
[72]
논문
Extrachromosomal psi+ determinant suppresses nonsense mutations in yeast
1979-09
[73]
논문
A yeast prion provides a mechanism for genetic variation and phenotypic diversity
2000-09
[74]
논문
Prions as adaptive conduits of memory and inheritance
2005-06
[75]
논문
The conversion of 3' UTRs into coding regions
2007-02
[76]
논문
The spontaneous appearance rate of the yeast prion [PSI+] and its implications for the evolution of the evolvability properties of the [PSI+] system
2010-02
[77]
논문
A prion accelerates proliferation at the expense of lifespan
2021-09
[78]
논문
Wandering along the epigenetic timeline
2020-07
[79]
논문
Paramutation: from maize to mice
2007-02
[80]
서적
RUNX Proteins in Development and Cancer
[81]
논문
Paramutation: the tip of an epigenetic iceberg?
2010-01
[82]
논문
Genomic imprinting: the emergence of an epigenetic paradigm
2011-07
[83]
논문
Epigenetic changes and nontargeted radiation effects--is there a link?
2008-01
[84]
논문
Non-targeted radiation effects-an epigenetic connection
2011-09
[85]
논문
Radiation-induced alterations in histone modification patterns and their potential impact on short-term radiation effects
[86]
논문
DNA damage, homology-directed repair, and DNA methylation
2007-07
[87]
논문
Double strand breaks can initiate gene silencing and SIRT1-dependent onset of DNA methylation in an exogenous promoter CpG island
2008-08
[88]
논문
The role of poly(ADP-ribose) in the DNA damage signaling network
https://www.zora.uzh[...]
2005-06
[89]
논문
Poly(ADP-ribosyl)ation directs recruitment and activation of an ATP-dependent chromatin remodeler
2009-08
[90]
논문
Role of nucleosomal occupancy in the epigenetic silencing of the MLH1 CpG island
2007-11
[91]
논문
Epigenetic factors in cancer risk: effect of chemical carcinogens on global DNA methylation pattern in human TK6 cells
[92]
논문
Progressive, transgenerational changes in offspring phenotype and epigenotype following nutritional transition
[93]
논문
Dietary polyphenols may affect DNA methylation
2007-01
[94]
논문
The flavoring agent dihydrocoumarin reverses epigenetic silencing and inhibits sirtuin deacetylases
2005-12
[95]
논문
Effect of soy isoflavone supplementation on markers of oxidative stress in men and women
2001-10
[96]
논문
Modulation of Nrf2-dependent gene transcription by bilberry anthocyanins in vivo
2013-03
[97]
논문
Endogenous versus exogenous DNA adducts: their role in carcinogenesis, epidemiology, and risk assessment
2011-03
[98]
논문
A reliable assessment of 8-oxo-2-deoxyguanosine levels in nuclear and mitochondrial DNA using the sodium iodide method to isolate DNA
2001-05
[99]
논문
Mapping structurally defined guanine oxidation products along DNA duplexes: influence of local sequence context and endogenous cytosine methylation
2014-03
[100]
논문
OGG1 is essential in oxidative stress-induced DNA demethylation
2016-09
[101]
논문
The genomics of oxidative DNA damage, repair, and resulting mutagenesis
2020
[102]
논문
Lost in the Crowd: How Does Human 8-Oxoguanine DNA Glycosylase 1 (OGG1) Find 8-Oxoguanine in the Genome?
2020-11
[103]
논문
In situ analysis of repair processes for oxidative DNA damage in mammalian cells
2004-09
[104]
논문
Targeted DNA demethylation and activation of endogenous genes using programmable TALE-TET1 fusion proteins
2013-12
[105]
논문
Mismatch repair proteins recruit DNA methyltransferase 1 to sites of oxidative DNA damage
2016-06
[106]
논문
Oxidative DNA Damage Modulates DNA Methylation Pattern in Human Breast Cancer 1 (BRCA1) Gene via the Crosstalk between DNA Polymerase β and a de novo DNA Methyltransferase
2020-01
[107]
논문
Recruitment of DNA methyltransferase I to DNA repair sites
2005-06
[108]
논문
DNA damage, homology-directed repair, and DNA methylation
2007-07
[109]
논문
Double strand breaks can initiate gene silencing and SIRT1-dependent onset of DNA methylation in an exogenous promoter CpG island
2008-08
[110]
논문
Rapid and transient recruitment of DNMT1 to DNA double-strand breaks is mediated by its interaction with multiple components of the DNA damage response machinery
2011-01
[111]
논문
DNA damage and Repair Modify DNA methylation and Chromatin Domain of the Targeted Locus: Mechanism of allele methylation polymorphism
2016-09
[112]
논문
Detection of CRISPR-mediated genome modifications through altered methylation patterns of CpG islands
2020-12
[113]
논문
Non-homologous end joining induced alterations in DNA methylation: A source of permanent epigenetic change
2017-06
[114]
논문
Epigenetic research in cancer epidemiology: trends, opportunities, and challenges
2014-02
[115]
웹사이트
Studying epigenetics using ChIP
https://www.abcam.co[...]
[116]
서적
The Nucleus
Springer
2008
[117]
논문
Fluorescence in situ hybridization (FISH).
https://www.nature.c[...]
2008
[118]
논문
Improved quantification of DNA methylation using methylation-sensitive restriction enzymes and real-time PCR
[119]
논문
Transcriptomic and Epigenomic Dynamics of Honey Bees in Response to Lethal Viral Infection
2020-09-24
[120]
논문
RNA interference knockdown of DNA methyl-transferase 3 affects gene alternative splicing in the honey bee
2013-07
[121]
논문
Detecting DNA cytosine methylation using nanopore sequencing
2017-04
[122]
서적
A Conceptual History of Modern Embryology
[123]
서적
Genesis: the evolution of biology
https://archive.org/[...]
Oxford University Press
[124]
서적
Cycles of Contingency: Developmental Systems and Evolution (Life and Mind: Philosophical Issues in Biology and Psychology)
The MIT Press
[125]
논문
Tissue-specific profiling reveals distinctive regulatory architectures for ubiquitous, germline and somatic genes
2020-02-20
[126]
논문
Nucleosome repositioning links DNA (de)methylation and differential CTCF binding during stem cell development
2014-08
[127]
논문
Variants of core histones and their roles in cell fate decisions, development and cancer
https://www.nature.c[...]
2017-05
[128]
논문
Histone H3.3 maintains genome integrity during mammalian development
2015-07
[129]
웹사이트
The 3D genome
https://www.nature.c[...]
2021-09-26
[130]
논문
Engrams and circuits crucial for systems consolidation of a memory
2017-04
[131]
논문
Profiling DNA break sites and transcriptional changes in response to contextual fear learning
2021
[132]
논문
Real-time visualization of mRNA synthesis during memory formation in live mice
2022-07
[133]
논문
Activation of immediate early genes and memory formation
1999-04
[134]
논문
Rescue of aging-associated decline in Dnmt3a2 expression restores cognitive abilities
2012-07
[135]
논문
EGR1 recruits TET1 to shape the brain methylome during development and upon neuronal activity
2019-08
[136]
논문
Isoform-specific localization of DNMT3A regulates DNA methylation fidelity at bivalent CpG islands
2017-12
[137]
논문
Fear memory formation can affect a different memory: fear conditioning affects the extinction, but not retrieval, of conditioned taste aversion (CTA) memory
2014
[138]
논문
DNA methylation and its basic function
2013-01
[139]
논문
DNA methylation changes in plasticity genes accompany the formation and maintenance of memory
2016-01
[140]
논문
The involvement of the anterior cingulate cortex in remote contextual fear memory
2004-05
[141]
논문
Aging in the Brain: New Roles of Epigenetics in Cognitive Decline
2018-10-01
[142]
논문
Epigenetic mechanisms related to cognitive decline during aging
2020-02-01
[143]
논문
Epigenetic changes during ageing and their underlying mechanisms
2020-08-01
[144]
논문
The ageing epigenome and its rejuvenation
2020-03-01
[145]
논문
Cellular reprogramming and epigenetic rejuvenation
2021-09-01
[146]
논문
The emerging field of epigenetics in neurodegeneration and neuroprotection
2017-05-01
[147]
논문
Epigenetic regulation of cognition: A circumscribed review of the field
2016-11-01
[148]
논문
Epigenetics of the developing and aging brain: Mechanisms that regulate onset and outcomes of brain reorganization
2021-06-01
[149]
서적
Endocrine-Disrupting Chemicals
2021-01-01
[150]
논문
Choline, the brain and neurodegeneration: insights from epigenetics
2018-01-01
[151]
논문
Brain foods - the role of diet in brain performance and health
2021-05-01
[152]
논문
Physical exercise as an epigenetic modulator of brain plasticity and cognition
2017-09-01
[153]
뉴스
New discovery: Synapse hiding in the mice brain may advance our understanding of neuronal communication
https://interestinge[...]
2022-10-19
[154]
논문
A serotonergic axon-cilium synapse drives nuclear signaling to alter chromatin accessibility
2022-09-01
[154]
뉴스
Scientists discover new kind of synapse in neurons' tiny hairs
https://phys.org/new[...]
2022-10-19
[155]
논문
Epigenetics and brain evolution
2011-04-01
[156]
논문
Critical Notice: Cycles of Contingency – Developmental Systems and Evolution
2005-03-01
[157]
문서
Chapter: "Nervous System Development" in "Epigenetics," by Benedikt Hallgrimsson and Brian Hall
[158]
논문
'Open minded' cells: how cells can change fate
http://cromatina.icb[...]
2007-03-01
[159]
논문
Maternal methyl supplements in mice affect epigenetic variation and DNA methylation of offspring
2002-08-01
[160]
논문
Transposable elements: targets for early nutritional effects on epigenetic gene regulation
2003-08-01
[161]
논문
The agouti mouse model: an epigenetic biosensor for nutritional and environmental alterations on the fetal epigenome
2008-08-01
[162]
논문
Aberrant DNA methylation as a diagnostic biomarker of diabetic embryopathy
2019-11-01
[163]
웹사이트
Fearful Memories Passed Down to Mouse Descendants: Genetic imprint from traumatic experiences carries through at least two generations
https://www.scientif[...]
2013-12-01
[164]
웹사이트
Mice can 'warn' sons, grandsons of dangers via sperm
http://medicalxpress[...]
2013-12-13
[165]
논문
Too much success for recent groundbreaking epigenetic experiments
2014-10-01
[166]
논문
Parental olfactory experience influences behavior and neural structure in subsequent generations
2014-01-01
[167]
웹사이트
Epigenetics Paper Raises Questions
http://www.the-scien[...]
[168]
서적
Evolution: an introduction
Oxford University Press
[169]
서적
Evolution in four dimensions: genetic, epigenetic, behavioral, and symbolic variation in the history of life
MIT Press
[170]
문서
See also [[Denis Noble]]: ''The Music of Life'', esp pp. 93–98 and p. 48, where he cites Jablonka & Lamb and [[Massimo Pigliucci]]'s review of Jablonka and Lamb in [[Nature (journal)|''Nature'']] '''435''', 565–566 (2 June 2005)
[171]
논문
Beyond DNA: integrating inclusive inheritance into an extended theory of evolution
2011-06-01
[172]
논문
Models of a dual inheritance system
1990-03-01
[173]
논문
The frailty of adaptive hypotheses for the origins of organismal complexity
2007-05-01
[174]
논문
The extended evolutionary synthesis and the role of soft inheritance in evolution
2012-08-01
[175]
논문
Timescales of genetic and epigenetic inheritance
2007-02-01
[176]
논문
The evolution of reversible switches in the presence of irreversible mimics
2009-09
[177]
논문
Rate, spectrum, and evolutionary dynamics of spontaneous epimutations
2015-05
[178]
논문
Complex adaptations can drive the evolution of the capacitor [PSI], even with realistic rates of yeast sex
2009-06
[179]
논문
Transgenerational epigenetic inheritance: prevalence, mechanisms, and implications for the study of heredity and evolution
http://compgen.unc.e[...]
2017-11-01
[180]
서적
Do Butterflies Bite?: Fascinating Answers to Questions about Butterflies and Moths (Animals Q&A)
Rutgers University Press
[181]
논문
Relics of repeat-induced point mutation direct heterochromatin formation in Neurospora crassa
2009-03
[182]
서적
Epigenetics
Caister Academic Press
[183]
논문
Modeling kinetic rate variation in third generation DNA sequencing data to detect putative modifications to DNA bases
2013-01
[184]
논문
Entering the era of bacterial epigenomics with single molecule real time DNA sequencing
2013-04
[185]
논문
Comprehensive methylome characterization of Mycoplasma genitalium and Mycoplasma pneumoniae at single-base resolution
[186]
논문
The methylomes of six bacteria
2012-12
[187]
논문
Genome-wide mapping of methylated adenine residues in pathogenic Escherichia coli using single-molecule real-time sequencing
2012-12
[188]
논문
Bacterial Epigenomics: Coming of Age
2021-08
[189]
논문
Epigenetic gene regulation in the bacterial world
2006-09
[190]
논문
A random six-phase switch regulates pneumococcal virulence via global epigenetic changes
2014-09
[191]
논문
Epigenomic characterization of Clostridioides difficile finds a conserved DNA methyltransferase that mediates sporulation and pathogenesis
2020-01
[192]
논문
The multidimensional nature of epigenetic information and its role in disease
2011-03
[193]
논문
Epigenetic differences arise during the lifetime of monozygotic twins
2005-07
[194]
논문
DNA methylation profiles in monozygotic and dizygotic twins
2009-02
[195]
뉴스
The Claim: Identical Twins Have Identical DNA
https://www.nytimes.[...]
2008-03-11
[196]
논문
Epigenetics lessons from twins: prospects for autoimmune disease
2010-08
[197]
논문
Potential Diagnostic and Prognostic Biomarkers of Epigenetic Drift within the Cardiovascular Compartment
[198]
간행물
105830
OMIM
[199]
논문
Genomic imprinting in mammals: emerging themes and established theories
2006-11
[200]
논문
Angelman and Prader–Willi syndromes share a common chromosome 15 deletion but differ in parental origin of the deletion
1989-02
[201]
문서
A person's paternal grandson is the son of a son of that person; a maternal grandson is the son of a daughter.
[202]
웹사이트
Sex-specific, male-line transgenerational responses in humans
http://www.dundee.ac[...]
2006-02
[203]
웹사이트
NOVA | Transcripts | Ghost in Your Genes
https://www.pbs.org/[...]
PBS
2007-10-16
[204]
논문
Off-Target drug effects resulting in altered gene expression events with epigenetic and "Quasi-Epigenetic" origins
2016-05
[205]
논문
Understanding Epigenetic Effects of Endocrine Disrupting Chemicals: From Mechanisms to Novel Test Methods
2018-01
[206]
서적
Reference Module in Neuroscience and Biobehavioral Psychology
[207]
서적
Behavioral Genetics
https://books.google[...]
Worth Publishers
2017
[208]
논문
Transgenerational epigenetic inheritance: myths and mechanisms
2014-03
[209]
논문
Transcriptional and epigenetic mechanisms of addiction
2011-10
[210]
논문
Drug addiction: from bench to bedside
2021-08
[211]
논문
Epigenetic regulation in drug addiction
[212]
논문
Mechanisms of transgenerational inheritance of addictive-like behaviors
2014-04
[213]
논문
Transgenerational Inheritance of Paternal Neurobehavioral Phenotypes: Stress, Addiction, Ageing and Metabolism
2016-11
[214]
논문
Crosstalk between genetic and epigenetic information through cytosine deamination
2010-10
[215]
논문
Nonantibiotic Effects of Fluoroquinolones in Mammalian Cells
2015-09
[216]
논문
The histone methyltransferase inhibitor BIX01294 enhances the cardiac potential of bone marrow cells
2013-02
[217]
논문
Inhibition of G9a Histone Methyltransferase Converts Bone Marrow Mesenchymal Stem Cells to Cardiac Competent Progenitors
2015
[218]
논문
CD44 regulates epigenetic plasticity by mediating iron endocytosis
2020-10
[219]
논문
A druggable copper-signalling pathway that drives inflammation
2023-05
[220]
논문
RNA epigenetics
2015-01
[221]
논문
Epigenetics: Roles and therapeutic implications of non-coding RNA modifications in human cancers
2021-09
[222]
논문
Epigenome editing: targeted manipulation of epigenetic modifications in plants
2022-03
[223]
논문
Genetic variation influencing DNA methylation provides insights into molecular mechanisms regulating genomic function
https://push-zb.helm[...]
2023-01-20
[224]
논문
Protein tyrosine phosphatase UBASH3B is overexpressed in triple-negative breast cancer and promotes invasion and metastasis
2013-07
[225]
논문
Meta-analysis of genome-wide association studies for height and body mass index in ~700000 individuals of European ancestry
2018-10
[226]
논문
Meta-analysis of genome-wide association studies for body fat distribution in 694 649 individuals of European ancestry
2019-01
[227]
논문
Shared genetic and experimental links between obesity-related traits and asthma subtypes in UK Biobank
2020-02
[228]
논문
Evaluating the relationship between circulating lipoprotein lipids and apolipoproteins with risk of coronary heart disease: A multivariable Mendelian randomisation analysis
2020-03
[229]
논문
Blood cell transcriptomic-based early biomarkers of adverse programming effects of gestational calorie restriction and their reversibility by leptin supplementation
2015-03
[230]
논문
From the era of genome analysis to the era of genomic drug discovery: a pioneering example of rheumatoid arthritis
2014-11
[231]
논문
FADS1-FADS2 genetic polymorphisms are associated with fatty acid metabolism through changes in DNA methylation and gene expression
2018-08
[232]
논문
Genome-wide association study of plasma N6 polyunsaturated fatty acids within the cohorts for heart and aging research in genomic epidemiology consortium
2014-06
[233]
논문
An atlas of genetic influences on human blood metabolites
2014-06
[234]
논문
A GWAS of 170,000 Individuals Identifies Thousands of Alleles Perturbing Blood Cell Traits, Many of Which Are in Super Enhancers Setting Cell Identity
2016-12-02
[235]
논문
PhenoScanner V2: an expanded tool for searching human genotype-phenotype associations
2019-11
[236]
웹사이트
Epigenetics: It doesn't mean what quacks think it means
https://www.scienceb[...]
2013-02-04
[237]
서적
Epigenetic mechanisms of gene regulation
Cold Spring Harbor Laboratory Press
[238]
논문
Disputed definitions
http://www.nature.co[...]
[239]
논문
Brain function and chromatin plasticity
[240]
논문
Epigenetic mechanisms in cognition
[241]
문서
On Protein Synthesis.
http://profiles.nlm.[...]
[242]
논문
Central dogma of molecular biology
http://www.nature.co[...]
[243]
논문
Human epigenome project—Up and running
[244]
논문
Stability and flexibility of epigenetic gene regulation in mammalian development
[245]
논문
The epigenotype
[246]
논문
Paramutation: from maize to mice
http://www.sciencedi[...]
[247]
논문
Transgenerational epigenetic inheritance: prevalence, mechanisms, and implications for the study of heredity and evolution
[248]
간행물
Medical Subject Headings (2011 [[MeSH]])
http://www.nlm.nih.g[...]
NIH
2012-12-18
[249]
문서
オックスフォード英語辞典 인용문
[250]
문서
オズワルド・アベリー 인용문
[251]
논문
Epigenetic Factors Affecting Mating Type Expression in Certain Ciliates
[252]
논문
Mechanisms for the control of gene activity during development
[253]
논문
Perceptions of epigenetics
[254]
논문
An operational definition of epigenetics
http://genesdev.cshl[...]
[255]
서적
エピゲノム
http://lsd.pharm.kyo[...]
[256]
논문
Epigenomic plasticity within populations: its evolutionary significance and potential
http://www.nature.co[...]
[257]
논문
Maternal methyl supplements in mice affect epigenetic variation and DNA methylation of offspring
[258]
논문
Transposable elements: targets for early nutritional effects on epigenetic gene regulation
[259]
논문
Transgenerational plasticity is adaptive in the wild
[260]
논문
The genome strikes back: the evolutionary importance of defence against mobile elements
http://link.springer[...]
[261]
논문
Epigenetic gene regulation in the bacterial world
[262]
논문
'Open minded' cells: how cells can change fate
http://cromatina.icb[...]
[263]
문서
XX個体 인용문
[264]
논문
Birth of parthenogenetic mice that can develop to adulthood
[265]
논문
Epigenetic reprogramming in mammalian development
2012-10-31
[266]
논문
The multidimensional nature of epigenetic information and its role in disease
http://www.discovery[...]
[267]
논문
N6-Methyladenosine in nuclear RNA is a major substrate of the obesity-associated FTO
2011-10-16
[268]
논문
DNA methylation profiles in monozygotic and dizygotic twins
[269]
논문
Epigenetic differences arise during the lifetime of monozygotic twins
[270]
논문
Genetic or epigenetic difference causing discordance between monozygotic twins as a clue to molecular basis of mental disorders
http://www.nature.co[...]
[271]
논문
Genomic imprinting in mammals: emerging themes and established theories
[272]
서적
ヘミ接合性・半接合性
http://lsd.pharm.kyo[...]
[273]
OMIM
"105830"
[274]
논문
Angelman and Prader-Willi syndromes share a common chromosome 15 deletion but differ in parental origin of the deletion
[275]
논문
Genetic toxicities of human teratogens
[276]
논문
Association of valproate-induced teratogenesis with histone deacetylase inhibition in vivo
[277]
논문
Does thalidomide cause second generation birth defects?
[278]
서적
Epigenetics: A Reference Manual
Caister Academic Press
[279]
논문
Prostate cancer chemopreventive activity of phenethyl isothiocyanate through epigenetic regulation
[280]
논문
Potential role of HDAC inhibitors in cancer therapy: insights into oral squamous cell carcinoma
[281]
논문
Cancer treatment of the future: inhibitors of histone methyltransferases
[282]
웹사이트
FDA Approves New Drug for Skin Cancer, Zolinza
http://www.fda.gov/N[...]
FDA
2006-10-06
[283]
논문
Epigenetic gene regulation in the bacterial world
[284]
서적
Epigenetics
Caister Academic Press
[285]
논문
Cell plasticity in Caenorhabditis elegans: from induced to natural cell reprogramming
http://onlinelibrary[...]
[286]
논문
Nuclear organization and dosage compensation
[287]
논문
Evolution of dnmt-2 and mbd-2-like genes in the free-living nematodes Pristionchus pacificus, Caenorhabditis elegans and Caenorhabditis briggsae
[288]
논문
DNA methylation is widespread and associated with differential gene expression in castes of the honeybee, Apis mellifera
[289]
논문
Plant imprinted genes identified by genome-wide approaches and their regulatory mechanisms
http://pcp.oxfordjou[...]
[290]
문서
CpGの"p"の文字は、シトシンとグアニンの間のホスホジエステル結合を示す。5'-CpG-3' 配列の相補配列もまた5'-CpG-3'である。DNA複製でできる2本鎖DNAは、鋳型鎖のCpG部位がメチル化されていた場合、複製鎖の未メチル化CpGが塩基対を作るヘミメチル化状態となる。
[291]
논문
The human DNA methyltransferases (DNMTs) 1, 3a and 3b: coordinate mRNA expression in normal tissues and overexpression in tumors
[292]
논문
A targeting sequence directs DNA methyltransferase to sites of DNA replication in mammalian nuclei
[293]
논문
DNA methylation in health and disease
[294]
논문
Role for DNA methylation in genomic imprinting
[295]
논문
Alterations of DNA Methylation Caused by Cold Plasma Treatment Restore Delayed Germination of Heat-Stressed Rice ( Oryza sativa L.) Seeds
https://pubs.acs.org[...]
2021-02-15
[296]
문서
히ストンH3のアミノ酸配列(一次構造)のN末端から9番目、14番目のリシン|リジン(Kはリジン残基のアルファベット1文字表記)をH3K9, H3K14のように表記する。他のヒストンタンパク質とアミノ酸残基組み合せでも同様の表記を用いる。
[297]
논문
Histone H3K4 demethylases are essential in development and differentiation
[298]
논문
High-resolution profiling of histone methylations in the human genome
[299]
논문
DOT1L/KMT4 recruitment and H3K79 methylation are ubiquitously coupled with gene transcription in mammalian cells
[300]
논문
Determination of enriched histone modifications in non-genic portions of the human genome
[301]
논문
The landscape of histone modifications across 1% of the human genome in five human cell lines
[302]
논문
SET domain proteins modulate chromatin domains in eu- and heterochromatin
[303]
논문
Developmental roles of the histone lysine demethylases
[304]
논문
Translating the histone code
[305]
논문
ATP-dependent chromatin remodeling: genetics, genomics and mechanisms
[306]
논문
Potent and specific genetic interference by double-stranded RNA in Caenorhabditis elegans
http://www.nature.co[...]
[307]
웹사이트
Nobel Prize in Physiology or Medicine 2006
http://www.nobelpriz[...]
2006
[308]
논문
Prions are a common mechanism for phenotypic inheritance in wild yeasts
[309]
논문
"[PSI], a cytoplasmic suppressor of super-suppression in yeast"
[310]
논문
Non-Mendelian mutation allowing ureidosuccinic acid uptake in yeast
[311]
논문
Extrachromosomal psi+ determinant suppresses nonsense mutations in yeast
[312]
논문
A yeast prion provides a mechanism for genetic variation and phenotypic diversity
[313]
논문
Prions as adaptive conduits of memory and inheritance
[314]
논문
Cytoplasmic inheritance of the organization of the cell cortex in Paramecium aurelia
[315]
논문
Concepts of organization. The leverage of ciliate protozoa
[316]
서적
Genesis: the evolution of biology
Oxford University Press
[317]
서적
Cycles of Contingency: Developmental Systems and Evolution (Life and Mind: Philosophical Issues in Biology and Psychology)
The MIT Press
[318]
간행물
뇌신경 발달 및 기능의 후생유전적 조절 기전
http://www.ksmb.or.k[...]
분자세포 생물학 뉴스
2021-11-04
[319]
간행물
인체의 후성유전학 연구동향
http://m.bioin.or.kr[...]
바이오인
[320]
문서
'Oxford English Dictionary: "The word is used by W. Harvey, ''Exercitationes'' 1651, p. 148, and in the ''English Anatomical Exercitations'' 1653, p. 272. It is explained to mean ‘partium super-exorientium additamentum’, ‘the additament of parts budding one out of another’."'
[321]
저널
The epigenotype
[322]
문서
'See ''[[preformationism]]'' for historical background. [[Oxford English Dictionary]]: "the theory that the germ is brought into existence (by successive accretions), and not merely developed, in the process of reproduction. [...] The opposite theory was formerly known as the ‘theory of evolution’; to avoid the ambiguity of this name, it is now spoken of chiefly as the ‘theory of preformation’, sometimes as that of ‘encasement’ or ‘emboîtement’."'
[323]
서적
The Epigenetics of Birds
https://books.google[...]
Cambridge University Press
1953
[324]
저널
In search of evolutionary developmental mechanisms: the 30-year gap between 1944 and 1974
2004-01-15
[325]
저널
Floral Morphogenesis: Stochastic Explorations of a Gene Network Epigenetic Landscape.
http://www.plosone.o[...]
2008-11-03
[326]
저널
Branching and oscillations in the epigenetic landscape of cell-fate determination
http://www.sciencedi[...]
2015-01-30
[327]
저널
Epigenetic systems view of human development
[328]
저널
Floral Morphogenesis: Stochastic Explorations of a Gene Network Epigenetic Landscape
2008-11-03
[329]
문서
유인자는 유전정보 변형의 평형점, 한계점을 이룰 수 있으며, 특이 유인자(strange attractor)일 수도 있다.
[330]
간행물
암 후성유전체의 연구 동향
http://www.bioin.or.[...]
바이오인
[331]
저널
On the use of the word 'epigenetic'
2007-04
본 사이트는 AI가 위키백과와 뉴스 기사,정부 간행물,학술 논문등을 바탕으로 정보를 가공하여 제공하는 백과사전형 서비스입니다.
모든 문서는 AI에 의해 자동 생성되며, CC BY-SA 4.0 라이선스에 따라 이용할 수 있습니다.
하지만, 위키백과나 뉴스 기사 자체에 오류, 부정확한 정보, 또는 가짜 뉴스가 포함될 수 있으며, AI는 이러한 내용을 완벽하게 걸러내지 못할 수 있습니다.
따라서 제공되는 정보에 일부 오류나 편향이 있을 수 있으므로, 중요한 정보는 반드시 다른 출처를 통해 교차 검증하시기 바랍니다.
문의하기 : help@durumis.com