에너지 등분배법칙
"오늘의AI위키"의 AI를 통해 더욱 풍부하고 폭넓은 지식 경험을 누리세요.
1. 개요
에너지 등분배 법칙은 열평형 상태의 계에서 모든 자유도에 대해 평균 에너지가 같다는 원리이다. 고전 통계역학에서 중요한 개념으로, 이차식 형태 에너지의 한 자유도에 대한 평균 에너지가 1/2kT임을 의미한다. 라틴어에서 유래된 "균등한 분배"라는 뜻처럼, 시스템의 총 운동 에너지가 열적 평형에 도달하면 모든 독립적인 부분에 균등하게 공유된다는 것을 의미한다. 예를 들어, 열적 평형 상태의 비활성 기체 원자는 평균 병진 운동 에너지를 가지며, 단원자 이상 기체의 총 에너지는 3/2NkT로 예측된다. 회전 분자의 회전 에너지와 조화 진동자의 위치 에너지에도 적용되며, 결정성 고체의 비열 용량과 중력 하의 입자 침강 현상 설명에도 활용된다. 에너지 등분배 법칙은 미시적인 세계와 거시적인 세계를 연결하며, 이상 기체 상태 방정식과 같은 중요한 개념을 이끌어냈다. 그러나 양자 역학적 현상을 설명하지 못하고, 에너지 준위 간격이 클 경우 적용이 어렵다는 한계를 지닌다.
더 읽어볼만한 페이지
- 통계역학 - 볼츠만 상수
볼츠만 상수 k는 온도와 에너지를 연결하는 상수이며, 기체 상수와 아보가드로 상수의 비로 정의되고, SI 단위계에서 1.380649×10⁻²³ J/K의 값을 가지며, 거시 물리학과 미시 물리학을 연결하는 중요한 역할을 한다. - 통계역학 - 상태 밀도
상태 밀도는 계에서 특정 에너지 준위에 존재할 수 있는 상태의 수를 나타내는 물리량으로, 계의 종류, 차원, 분산 관계 등에 따라 달라지며, 고체 물리학과 양자역학적 계에서 중요한 역할을 한다. - 열역학 - 볼츠만 상수
볼츠만 상수 k는 온도와 에너지를 연결하는 상수이며, 기체 상수와 아보가드로 상수의 비로 정의되고, SI 단위계에서 1.380649×10⁻²³ J/K의 값을 가지며, 거시 물리학과 미시 물리학을 연결하는 중요한 역할을 한다. - 열역학 - 열기관
열기관은 고온 열원에서 열을 받아 일을 하고 나머지를 저온 열원으로 방출하는 장치이며, 증기 동력, 가스 동력, 내연기관 등으로 분류되어 화력 발전소, 자동차 등 다양한 분야에 활용된다. - 물리학 개념 - 절연체
절연체는 전기 전도성을 막아 전기의 흐름을 제어하고 안전을 확보하며, 밴드 이론에 따라 큰 띠틈을 가져 외부 전압이 띠틈을 넘어서면 절연 파괴가 발생하며, 유리에서 세라믹, 고분자 복합 재료 등으로 제작되어 전선, 케이블 등 다양한 분야에 사용된다. - 물리학 개념 - 전기 전도체
전기 전도체는 전기를 잘 통하는 물질로, 금속, 전해질, 초전도체, 반도체 등이 있으며, 구리, 은, 알루미늄 등 다양한 재료가 전선 등에 사용된다.
2. 개념의 정의 및 필요성
고전 통계역학에서 중요하게 다루어지는 에너지 등분배법칙은 열평형 상태에 있는 계의 모든 자유도에 대해 계가 가질 수 있는 평균 에너지가 같다는 원리이다. 좀 더 엄밀하게 표현하면 "이차식 형태 에너지의 한 자유도에 대한 평균 에너지는 이다."
아인슈타인과 플랑크의 빛에 관한 논쟁에서 에너지 등분배법칙의 필요성이 잠재적으로 드러났다. 에너지 등분배 원리는 고전 역학, 고전 통계 역학, 양자 역학의 세계를 어느 정도 동일한 맥락에서 설명할 수 있어 일반적으로 널리 적용될 수 있었다. 미국의 윌리엄 깁스가 다루었던 에너지 등분배 원리는 1902년 이후에나 과학자들 사이에서 분명하게 인식되었다.[2][3]
"등분배"라는 이름은 "균등한 분배"를 의미하며, 이는 라틴어 ''equi'' ("균등 또는 짝수")와 ''partitio'' ("분할, 부분")에서 파생되었다. 등분배의 원래 개념은 시스템의 총 운동 에너지가 시스템이 열적 평형에 도달하면, 모든 독립적인 부분에 걸쳐 ''평균적으로'' 동일하게 공유된다는 것이다.
예를 들어, 온도 에서 열적 평형 상태의 비활성 비활성 기체의 모든 원자는 평균 병진 운동 에너지 를 가지며, 여기서 는 볼츠만 상수이다. 결과적으로, 운동 에너지는 (질량)(속도)2와 같으므로, 제논의 더 무거운 원자는 같은 온도에서 헬륨의 더 가벼운 원자보다 평균 속도가 낮다.
이 예에서 핵심은 운동 에너지가 속도에 대해 이차적이라는 것이다. 등분배 정리는 열적 평형에서 에너지에 이차적으로만 나타나는 모든 자유도 (입자의 위치 또는 속도의 구성 요소와 같은)는 평균 에너지 를 가지며 따라서 시스템의 열용량에 를 기여한다고 보여준다.
에너지 등분배 정리는 적절한 가정 하에서 해밀턴 에너지 함수 와 자유도 을 가진 물리 시스템의 경우, 모든 지표 과 에 대해 다음과 같은 에너지 등분배 공식을 열적 평형 상태에서 만족한다.[31][30][29]
:
여기서 는 크로네커 델타이며, 인 경우 1이고 그렇지 않으면 0이다. 평균 괄호 는 위상 공간에 대한 앙상블 평균 또는 에르고드성의 가정하에서 단일 시스템의 시간 평균으로 간주된다.
일반적인 에너지 등분배 정리는 시스템의 총 에너지가 일정한 미시적 앙상블[30]과 시스템이 에너지 교환이 가능한 열욕조에 연결된 정준 앙상블[31][32] 모두에서 성립한다.
일반적인 공식은 다음 두 가지와 동일하다.
#
#
자유도 ''xn''이 해밀턴 ''H''에서 이차 항 ''anxn''2으로만 나타나는 경우, 이 공식 중 첫 번째 공식은
:
로 나타낼 수 있는데, 이는 이 자유도가 평균 에너지 에 기여하는 값의 두 배이다. 따라서, 이차 에너지를 가진 시스템에 대한 에너지 등분배 정리는 일반적인 공식으로부터 쉽게 유도된다.
자유도 ''xn''은 시스템의 위상 공간에 대한 좌표이며, 따라서 일반적으로 일반화된 위치 좌표 ''qk'' 및 ''qk''에 대한 켤레 운동량인 일반화된 운동량 좌표 ''pk''로 세분된다. 이러한 상황에서 공식 1은 모든 ''k''에 대해 다음을 의미한다.
:
해밀턴 역학의 방정식을 사용하면,[33] 이러한 공식은 다음과 같이 쓸 수도 있다.
:
유사하게, 공식 2를 사용하여 다음을 보일 수 있다.
:
그리고
:
단원자 분자 이상 기체의 개별 분자의 에너지는 ''m''을 해당 분자의 질량으로 하여,
:
이며, 이로부터,
:
가 된다. ''x'', ''y'', ''z'' 각 좌표(= 자유도)의 운동량인 ''px'', ''py'', ''pz''에 대응하는 자유도에 에너지 ''k''B''T''/2가 배분되기 때문이다.
이 경우, 이원자 분자가 갖는 에너지는
:
가 된다. 위 식의 첫 번째 괄호 부분은 단원자 분자의 경우와 같은 자유도에 의한 에너지이며, 두 번째 괄호가 이원자 분자의 회전에 관한 자유도(''θ''와 ''φ''의 2개 존재)로부터의 에너지이다. ''θ''와 ''φ''는 이원자 분자를 하나의 축(강체의 막대)으로 간주했을 때의 회전에 관한 각도 성분(자유도)이다. ''m''은 이원자 분자의 질량, ''I''는 이원자 분자의 질량 중심을 지나고, 이원자 분자의 축에 수직인 축 주위의 회전에 관한 관성 모멘트이다.
이 경우, 자유도는 총 다섯 개가 되므로,
:
가 된다.
미시적인 세계와 거시적인 세계를 에너지의 관점에서 설명하기 위해서는 양자 역학적 운동 방정식과 고전 역학적 운동 방정식 사이의 관계를 이해하는 것이 필요했다. 양자수가 매우 큰 경우에는 양자 역학적 운동 방정식이 고전 역학적 운동 방정식과 거의 같아진다는 사실은 이미 알려져 있었다. 또한, 양자 역학적 정준 분배 함수에서 큰 양자 수에 해당하는 항들은 온도가 높아질수록 중요해진다. 이러한 사실들을 통해, 충분히 높은 온도에서는 양자 역학을 통해 얻은 계의 분배 함수가 고전 역학을 통해 얻은 분배 함수와 거의 같을 것이라는 예측이 가능했다. 에너지 등분배 법칙은 이러한 예측을 뒷받침하며, 미시 세계와 거시 세계를 연결하는 다리 역할을 수행했다.[2]
2. 1. 개념의 정의
고전 통계역학에서 중요하게 다루어지는 에너지 등분배법칙은 열평형 상태에 있는 계의 모든 자유도에 대해 계가 가질 수 있는 평균 에너지가 같다는 원리이다. 좀 더 엄밀하게 표현하면 다음과 같다.:"이차식 형태 에너지의 한 자유도에 대한 평균 에너지는 이다."
아인슈타인과 플랑크의 빛에 관한 논쟁에서 에너지 등분배법칙의 필요성이 잠재적으로 드러났다. 에너지 등분배 원리는 고전적 역학의 세계와 고전 통계 역학, 양자 역학의 세계를 어느 정도 동일한 맥락에서 설명할 수 있어 일반적으로 널리 적용될 수 있었다. 미국의 윌리엄 깁스가 다루었던 에너지 등분배 원리는 1902년 이후에나 분명하게 과학자들 사이에서 인식되었다.[2][3]
"등분배"라는 이름은 "균등한 분배"를 의미하며, 이는 라틴어 ''equi'' ("균등 또는 짝수")와 ''partitio'' ("분할, 부분")에서 파생되었다. 등분배의 원래 개념은 시스템의 총 운동 에너지가 시스템이 열적 평형에 도달하면, 모든 독립적인 부분에 걸쳐 ''평균적으로'' 동일하게 공유된다는 것이다.
예를 들어, 온도 에서 열적 평형 상태의 비활성 비활성 기체의 모든 원자는 평균 병진 운동 에너지 를 가지며, 여기서 는 볼츠만 상수이다. 결과적으로, 운동 에너지는 (질량)(속도)2와 같으므로, 제논의 더 무거운 원자는 같은 온도에서 헬륨의 더 가벼운 원자보다 평균 속도가 낮다.
이 예에서 핵심은 운동 에너지가 속도에 대해 이차적이라는 것이다. 등분배 정리는 열적 평형에서 에너지에 이차적으로만 나타나는 모든 자유도 (입자의 위치 또는 속도의 구성 요소와 같은)는 평균 에너지 를 가지며 따라서 시스템의 열용량에 를 기여한다고 보여준다.
에너지 등분배 정리는 적절한 가정 하에서 해밀턴 에너지 함수 와 자유도 를 가진 물리 시스템의 경우, 모든 지표 과 에 대해 다음과 같은 에너지 등분배 공식을 열적 평형 상태에서 만족한다.[31][30][29]
:
여기서 는 크로네커 델타이며, 인 경우 1이고 그렇지 않으면 0이다. 평균 괄호 는 위상 공간에 대한 앙상블 평균 또는 에르고드성의 가정하에서 단일 시스템의 시간 평균으로 간주된다.
일반적인 에너지 등분배 정리는 시스템의 총 에너지가 일정한 미시적 앙상블[30]과 시스템이 에너지 교환이 가능한 열욕조에 연결된 정준 앙상블[31][32] 모두에서 성립한다.
일반적인 공식은 다음 두 가지와 동일하다.
#
#
자유도 ''xn''이 해밀턴 ''H''에서 이차 항 ''anxn''2으로만 나타나는 경우, 이 공식 중 첫 번째 공식은
:
로 나타낼 수 있는데, 이는 이 자유도가 평균 에너지 에 기여하는 값의 두 배이다. 따라서, 이차 에너지를 가진 시스템에 대한 에너지 등분배 정리는 일반적인 공식으로부터 쉽게 유도된다.
자유도 ''xn''은 시스템의 위상 공간에 대한 좌표이며, 따라서 일반적으로 일반화된 위치 좌표 ''qk'' 및 ''qk''에 대한 켤레 운동량인 일반화된 운동량 좌표 ''pk''로 세분된다. 이러한 상황에서 공식 1은 모든 ''k''에 대해 다음을 의미한다.
:
해밀턴 역학의 방정식을 사용하면,[33] 이러한 공식은 다음과 같이 쓸 수도 있다.
:
유사하게, 공식 2를 사용하여 다음을 보일 수 있다.
:
그리고
:
단원자 분자 이상 기체의 개별 분자의 에너지는 ''m''을 해당 분자의 질량으로 하여,
:
이며, 이로부터,
:
가 된다. ''x'', ''y'', ''z'' 각 좌표(= 자유도)의 운동량인 ''px'', ''py'', ''pz''에 대응하는 자유도에 에너지 ''k''B''T''/2가 배분되기 때문이다.
이 경우, 이원자 분자가 갖는 에너지는
:
가 된다. 위 식의 첫 번째 괄호 부분은 단원자 분자의 경우와 같은 자유도에 의한 에너지이며, 두 번째 괄호가 이원자 분자의 회전에 관한 자유도(''θ''와 ''φ''의 2개 존재)로부터의 에너지이다. ''θ''와 ''φ''는 이원자 분자를 하나의 축(강체의 막대)으로 간주했을 때의 회전에 관한 각도 성분(자유도)이다. ''m''은 이원자 분자의 질량, ''I''는 이원자 분자의 질량 중심을 지나고, 이원자 분자의 축에 수직인 축 주위의 회전에 관한 관성 모멘트이다.
이 경우, 자유도는 총 다섯 개가 되므로,
:
가 된다.
2. 2. 개념의 필요성
주어진 계에 대한 양자 역학적 운동 방정식은 양자수가 매우 큰 경우에는 고전 역학적 운동 방정식과 어림으로 거의 같다는 것은 이미 잘 알려져 있다. 또한 양자 역학적 정준 분배 함수에서 아주 큰 양자 수에 해당하는 항들은 온도가 높아지면 더욱 중요해진다. 이런 사실로부터 양자 역학의 결과를 이용하여 얻은 계의 분배 함수는 충분히 높은 온도에서는 고전 역학을 이용하여 얻은 분배 함수와 거의 같을 것으로 기대할 수 있다. 따라서 미시적인 세계와 거시적인 세계를 에너지의 관점에서 설명할 수 있는 적절한 논리가 필요했다.에너지 등분배 법칙은 아인슈타인과 플랑크의 빛에 관한 논쟁에서 그 필요성이 잠재적으로 드러났다. 윌리엄 깁스가 다루었던 에너지 등분배 원리는 1902년 이후에나 과학자들 사이에서 분명하게 인식되었다. 따라서 에너지 등분배 원리가 분명하게 확립되지 않은 상태에서 플랑크가 사용했던 통계적 방법은 현재 우리가 알고 있는 것과 완전히 동일하다고 하기 어렵다. 바로 이런 점에서 플랑크는 새로운 양자물리학의 포문을 연 선구자임에도 불구하고 태생적으로 보수적 한계를 드러내고 있다. 에너지 등분배 원리는 고전 역학, 고전 통계 역학, 양자 역학의 세계를 어느 정도 동일한 맥락에서 설명할 수 있어 일반적으로 널리 적용될 수 있었다.[2]
3. 내부 에너지와 에너지 등분배 원리
에너지 등분배 원리는 열적 평형 상태에 있는 계에서 에너지가 모든 자유도에 균등하게 분배된다는 원리이다. 듀롱-프티의 법칙은 이 원리로 설명할 수 있다.[2][3]
예를 들어, 단원자 이상 기체의 경우 각 원자는 3차원 공간에서 자유롭게 움직이므로 3개의 병진 자유도를 가진다. 에너지 등분배 원리에 따라 각 자유도에는 평균적으로 의 에너지가 할당된다. (k는 볼츠만 상수, T는 절대온도) 따라서 N개의 원자로 구성된 단원자 이상 기체의 총 에너지는 가 된다. 이원자 분자의 경우에는 병진 자유도 3개 외에 회전에 대한 자유도 2개가 추가되어 총 5개의 자유도를 가지므로, 이원자 분자 이상 기체의 총 에너지는 가 된다.
내부 에너지는 계가 가지고 있는 미시적인 에너지의 총합으로 다음과 같이 구성된다.
- 병진 에너지: 기체 분자가 공간을 운동하며 가지는 운동 에너지
- 회전 운동 에너지: 다원자 분자가 회전하며 가지는 에너지
- 진동 운동 에너지: 다원자 분자의 원자들이 진동하며 가지는 에너지 (주로 고온에서 중요)
- 전자 관련 에너지: 원자 내 전자의 회전 및 궤도 운동 에너지
- 핵에너지: 원자핵 내 입자들의 회전 에너지 및 핵 내부의 강한 결합력과 관련된 에너지 (일반적인 열역학에서는 고려하지 않음)
- 결합력 관련 에너지: 분자 간, 원자 간, 핵 내 입자 간 결합력과 관련된 에너지
- 잠열 에너지: 상변화와 관련된 에너지 (예: 고체->액체->기체)
- 화학 에너지: 분자 내 원자 결합과 관련된 에너지 (화학 반응에서 중요)
- 전자기 쌍극 모멘트 에너지: 외부 전자기장에 의한 에너지
이러한 에너지들은 계 내에 저장되는 정적 에너지로 볼 수 있다. 반면, 계의 경계를 통과하는 에너지는 동적 에너지 또는 에너지 상호작용으로, 열전달과 일이 대표적이다.[54][55]
에너지 등분배 원리는 에너지가 특정 형태()로 표현되는 계에 적용된다. 이 경우, 평균 에너지는 로, 에너지 등분배 원리가 성립함을 알 수 있다.[56]
따라서 N개의 입자로 구성되고 각 입자가 ν개의 자유도를 가지는 계의 평균 에너지는 다음과 같다.
:
이 공식은 고전 통계 역학에서는 잘 맞지만, 양자 역학적 현상을 설명하는 데는 한계가 있다.
3. 1. 계와 자유도
계(System)는 열역학적 논의의 대상이 되는 물질을 의미한다.[54] 자유도(Degree of freedom)는 계 내부의 입자가 가지고 있는 에너지의 한 형태를 말한다. 예를 들어, 병진 운동의 경우 3차원에서 세 방향으로 움직이므로 관련된 자유도는 3이라고 할 수 있다.[54]"등분배"라는 이름은 "균등한 분배"를 의미하며, 이는 라틴어 ''equi''(''균등'' 또는 ''짝수'')와 ''partitio''(''분할'', ''부분'')에서 파생되었다.[2][3] 등분배의 원래 개념은 시스템의 총 운동 에너지가 시스템이 열적 평형에 도달하면, 모든 독립적인 부분에 걸쳐 ''평균적으로'' 동일하게 공유된다는 것이다.
예를 들어, 온도에서 열적 평형 상태의 비활성 기체의 모든 원자는 평균 병진 운동 에너지 를 가지며, 여기서 는 볼츠만 상수이다. 결과적으로, 운동 에너지는 (질량)(속도)2와 같으므로, 제논의 더 무거운 원자는 같은 온도에서 헬륨의 더 가벼운 원자보다 평균 속도가 낮다. 그림은 네 가지 비활성 기체에서 원자 속도에 대한 맥스웰-볼츠만 분포를 보여준다.
일반적으로, 단원자 이상 기체에서 총 에너지는 순수하게 (병진) 운동 에너지로 구성된다. 즉, 입자는 내부 자유도를 갖지 않으며 서로 독립적으로 움직인다. 따라서 등분배 정리는 개의 입자로 구성된 이상 기체의 총 에너지가 라고 예측한다.
단원자 분자 이상 기체의 개별 분자의 에너지는 ''m''을 해당 분자의 질량으로 하여,
:
이며, 이로부터,
:
가 된다. ''x'', ''y'', ''z'' 각 좌표(= 자유도)의 운동량인 ''px'', ''py'', ''pz''에 대응하는 자유도에 에너지 ''k''B''T''/2가 배분되기 때문이다.
이원자 분자가 갖는 에너지는
:
가 된다. 위 식의 첫 번째 괄호 부분은 단원자 분자의 경우와 같은 자유도에 의한 에너지이며, 두 번째 괄호가 이원자 분자의 회전에 관한 자유도(''θ''와 ''φ''의 2개 존재)로부터의 에너지이다. ''θ''와 ''φ''는 이원자 분자를 하나의 축(강체의 막대)으로 간주했을 때의 회전에 관한 각도 성분(자유도)이다. ''m''은 이원자 분자의 질량, ''I''는 이원자 분자의 질량 중심을 지나고, 이원자 분자의 축에 수직인 축 주위의 회전에 관한 관성 모멘트이다.
이 경우, 자유도는 총 다섯 개가 되므로,
:
가 된다.
3. 2. 내부에너지의 구성 및 특징
내부에너지는 계가 가지고 있는 미시적인 에너지 형태의 합이라고 할 수 있다. 내부에너지를 구성하는 요소는 다음과 같다.- 병진 에너지: 기체 분자가 특정 속도로 공간을 운동할 때 가지는 운동 에너지이다.
- 회전 운동 에너지: 다원자 분자의 원자들이 축을 중심으로 회전하며 가지는 에너지이다.
- 진동 운동 에너지: 다원자 분자의 원자들이 공통의 질량 중심을 기준으로 진동하며 가지는 에너지이다. 기체에서는 주로 병진과 회전 운동 에너지가 주를 이루며, 고온에서는 진동 운동 에너지가 중요해진다.
- 전자의 회전 운동 에너지: 원자 내 전자가 핵을 중심으로 회전하며 가지는 에너지이다. 바깥쪽 궤도의 전자일수록 더 큰 운동 에너지를 가진다.
- 전자의 회전 에너지: 전자가 자신의 축을 중심으로 회전하며 가지는 에너지이다.
- 핵 내 입자의 회전 에너지: 원자핵 내 입자들이 가지는 회전 에너지이다.
- 현열 에너지: 분자들의 운동 에너지와 관련된 계의 내부에너지 일부를 나타낸다. 분자의 평균 속도와 활동도는 기체의 온도에 비례한다. 따라서 온도가 높을수록 분자의 운동 에너지가 커지고, 계의 내부에너지도 높아진다.[55]
- 결합력 관련 에너지: 물질을 구성하는 분자 간 결합력, 분자 내 원자 간 결합력, 원자와 원자핵 내 입자들 사이의 결합력과 관련된 에너지이다. 분자 간 결합력은 고체에서 가장 강하고 기체에서 가장 약하다.
- 잠열 에너지: 계의 상변화와 관련된 내부에너지이다. 충분한 에너지가 고체나 액체 분자에 더해지면 분자 간 결합력이 끊어지고 기체로 상변화가 일어난다. 이 때문에 기체 상태의 계는 고체나 액체 상태보다 높은 내부에너지 수준을 가진다. 상변화는 계의 화학적 조성 변화 없이 일어날 수 있다.
- 화학 에너지: 분자 내 원자 결합과 관련된 에너지이다. 연소와 같은 화학 반응에서 일부 화학 결합이 파괴되고 새로운 결합이 생성되면서 내부에너지가 변한다.
- 핵에너지: 원자핵 내 강한 결합력과 관련된 에너지이다. 핵분열이나 핵융합을 다루지 않는 한 열역학에서는 고려할 필요가 없다. 화학 반응은 원자 내 전자 구조의 변화를 수반하지만, 핵반응은 핵 내부의 변화를 포함한다. 따라서 원자는 화학 반응에서는 그 동일성을 유지하지만, 핵반응에서는 동일성을 잃는다.
- 전기 및 자기 쌍극 모멘트 에너지: 원자가 외부 전자기장에 노출되었을 때 가질 수 있는 에너지이다. 궤도 전자와 관련된 작은 전류에 의해 생성된 자기 쌍극이 꼬여 발생한다.[54]
위에 언급된 에너지 형태들은 계 내에 저장될 수 있는 정적 에너지로 볼 수 있다. 반면, 계에 저장되지 않는 에너지 형태는 동적 에너지 또는 에너지 상호작용으로 간주된다. 동적 에너지는 에너지가 계의 경계를 통과할 때 인지되며, 계가 과정 동안 얻거나 잃은 에너지를 나타낸다. 밀폐된 계와 관련된 에너지 상호작용에는 열전달(''heat transfer'')과 일(''work'')이 있다. 온도 차이가 구동력이면 에너지 상호작용은 열전달이고, 그렇지 않으면 일이다. 질량이 계로 또는 계로부터 전달될 때는 질량이 함유하는 에너지도 함께 전달되므로, 검사 체적은 질량 전달로 에너지를 교환할 수 있다.
3. 3. 에너지 등분배 원리를 적용한 계의 내부에너지
에너지 등분배 원리는 에너지가 형태로 표시된 계에만 적용된다. (: 상수 계수, : 좌표 또는 운동량 변수) 볼츠만 인자 를 이용한 분배 함수(맥스웰-볼츠만 분포)를 이용하여 평균 에너지를 구하면 다음과 같다.[56]:
이를 통해 를 얻고, 평균 에너지를 구하면 가 되어 에너지 등분배 원리가 성립함을 알 수 있다.
따라서 한 입자가 하나의 자유도 당 가질 수 있는 에너지는 등분배 원리에 따른다. 개의 입자로 이루어져 있고, 한 입자당 자유도가 인 계의 평균 에너지는 다음과 같다.
:
이 공식은 고전 통계 역학에서 뛰어난 설명력을 보였지만, 양자 역학적으로는 한계가 있어 논쟁의 대상이 되었다.
4. 미시적인 모형에서의 중요성
에너지 등분배 정리는 열적 평형 상태에 있는 물리 시스템에서 에너지가 어떻게 분배되는지를 설명하는 중요한 원리이다. 이 정리는 특정 가정 하에서, 해밀턴 에너지 함수와 자유도를 가진 시스템의 경우, 다음과 같은 공식을 만족한다.[31][30][29]
:
여기서 는 크로네커 델타이며, 평균 괄호 는 위상 공간에 대한 앙상블 평균 또는 단일 시스템의 시간 평균으로 간주된다.
일반적인 에너지 등분배 정리는 미시적 앙상블[30]과 정준 앙상블[31][32] 모두에서 성립하며, 다음과 같은 두 가지 중요한 결과를 도출한다.
#
#
이 공식들을 통해, 자유도 ''xn''이 해밀턴 ''H''에서 이차 항으로만 나타나는 경우, 각 자유도가 평균 에너지에 기여하는 정도를 쉽게 계산할 수 있다.
자유도 ''xn''은 시스템의 위상 공간 좌표를 나타내며, 일반화된 위치 좌표 ''qk''와 일반화된 운동량 좌표 ''pk''로 구성된다. 이를 통해 위의 공식들을 해밀턴 역학의 방정식을 사용하여 다음과 같이 표현할 수 있다.[33]
:
또한, j ≠ k 인 모든 경우에 대해 다음이 성립한다.
:
:
일반적인 에너지 등분배 법칙은 비리얼 정리의 확장으로 볼 수 있다.[34] 비리얼 정리는 개별 평균이 아닌 합산된 평균들을 서로 관련시키며, 온도와는 직접적인 관련이 없다.
에너지 등분배 정리의 유도는 통계 역학 교과서에서 찾아볼 수 있으며, 미시적 앙상블[31][30]과 정준 앙상블[31][32] 모두에 적용된다. 이 유도는 심플렉틱 다양체인 시스템의 위상 공간에 대한 평균을 구하는 과정을 포함한다.
듀롱-프티의 법칙은 에너지 등분배 법칙으로 설명 가능하다.
4. 1. 상태수와 앙상블의 개념
열역학 및 통계역학에서 가장 중요한 개념은 상태에 대한 이해이다. 계의 거시적 상태는 소수의 특정한 성질로 결정되지만, 이를 이루는 미시적 입자들은 다양한 배열과 상태를 가질 수 있어 동일한 거시적 상태를 여러 방식으로 구현할 수 있다. 이러한 배경에서 상태수라는 개념이 정의되는데, 이는 특정 거시적 상태를 만족하는 미시적 상태의 개수를 의미한다.[55]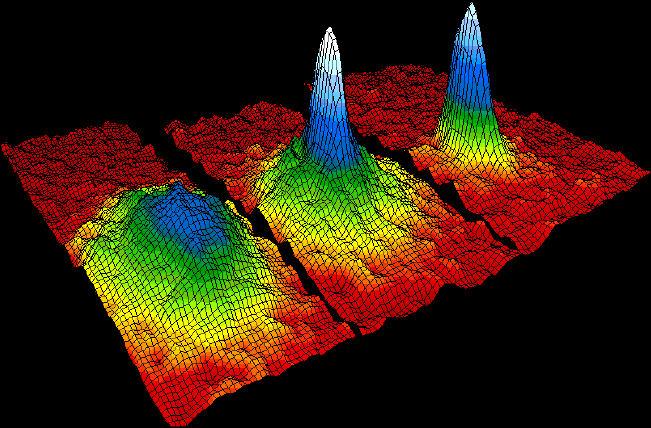
앙상블은 상태수와 밀접하게 연관되어 있다. 앙상블은 주어진 거시적 조건을 만족하는 모든 미시적 상태의 모임을 의미한다. 예를 들어, 원소가 1, 2, 3, 4, 5인 집합에서 각 구성 성분을 앙상블이라고 하면, 원소의 개수 5는 상태수를 의미한다. 앙상블에는 계의 상태와 조건에 따라 세 가지 종류가 있다.
- 작은 바른틀 앙상블: 계가 고립되어 있는 경우 (닫힌계 또는 고립계)
- 바른틀 앙상블: 계가 일정한 온도로 열적 상호 작용을 하는 경우
- 큰 바른틀 앙상블: 계가 주위 환경과 열적, 일적, 확산적 상호 작용을 하는 경우
앙상블과 상태수의 개념은 열역학 및 통계역학에서 미시적 상태 현상을 확률적으로 해석하고, 맥스웰-볼츠만 분포를 유도하는 데 중요한 역할을 한다.
4. 2. 미시적 상태에서의 에너지 등분배 법칙 적용
에르고딕성은 시간에 대한 평균과 모듬(ensemble)의 평균이 같다는 가정이다. 선험적 동등 확률의 원리는 서로 다른 양자 상태의 에너지가 같다면 두 양자 상태가 일어날 확률이 같다는 것을 의미한다. 이는 에너지 등분배 법칙에 의해 자유도가 같음을 의미한다.[56]미시적 상태에서 엔트로피는 상태수를 통해 다음과 같이 정의된다.
:
열역학 제 2법칙에 따르면 자연의 모든 상호작용은 엔트로피가 증가하는 방향으로 일어난다. 로그 함수는 증가함수이므로, 상태수 역시 모든 상호작용에서 증가해야 한다. 이는 확률적으로 가장 높은 미시 상태에 에너지가 분포하며, 에너지 등분배 법칙에 따라 각 자유도에 에너지가 나뉜다는 것을 의미한다.
5. 거시적 현상에 대한 설명력
에너지 등분배 법칙은 듀롱-프티 법칙을 설명할 수 있다.
5. 1. 상태 변화 과정의 종류와 특징
대부분의 물질은 기체, 액체, 고체라는 세 가지 상태를 넘나들 수 있다. 물질의 상태는 분자 사이에 작용하는 힘의 차이에 따라 구분된다. 기체는 분자가 가장 자유롭게 움직이는 상태이며, 비교적 높은 온도에서 존재한다. 기체 분자는 무질서하게 운동하며 서로 충돌하고 흩어진다.기체의 온도를 낮추거나 압력을 가하면 분자의 움직임이 둔화된다. 온도는 분자의 에너지 정도를 나타내는 척도이므로, 온도가 낮아지면 분자 운동 에너지가 감소한다. 분자들이 서로의 운동을 억제하고 달라붙게 되면 액체가 된다. 즉, 액체는 분자들이 열에너지를 잃고 분자 간의 힘으로 붙어 있는 상태이다.
액체에서 온도를 더 낮추면 분자들이 더욱 조밀하게 모여 고체가 된다. 고체에서는 분자 간의 힘이 매우 강하여 분자들이 거의 움직이지 못하고 약간 진동하는 정도이다.

고체에 열을 가하면 분자 운동이 활발해져 팽창하고, 더 많은 열을 받으면 분자 간 연결이 끊어져 액체가 된다. 기체에서는 분자가 자유롭게 운동할 수 있다. 이러한 상태 변화 과정에서는 열의 출입이 발생한다.
일정한 온도에서 물질의 상태가 변할 때 사용되는 열을 잠열(latent heat) 또는 숨은열이라고 한다. 상태 변화가 일어나는 구간에서는 온도가 변하지 않고, 두 가지 상태가 공존한다. 상태 변화의 종류에 따라 숨은열에는 고유한 이름이 붙는다.
5. 2. 에너지 등분배 법칙을 통한 상태 변화 설명
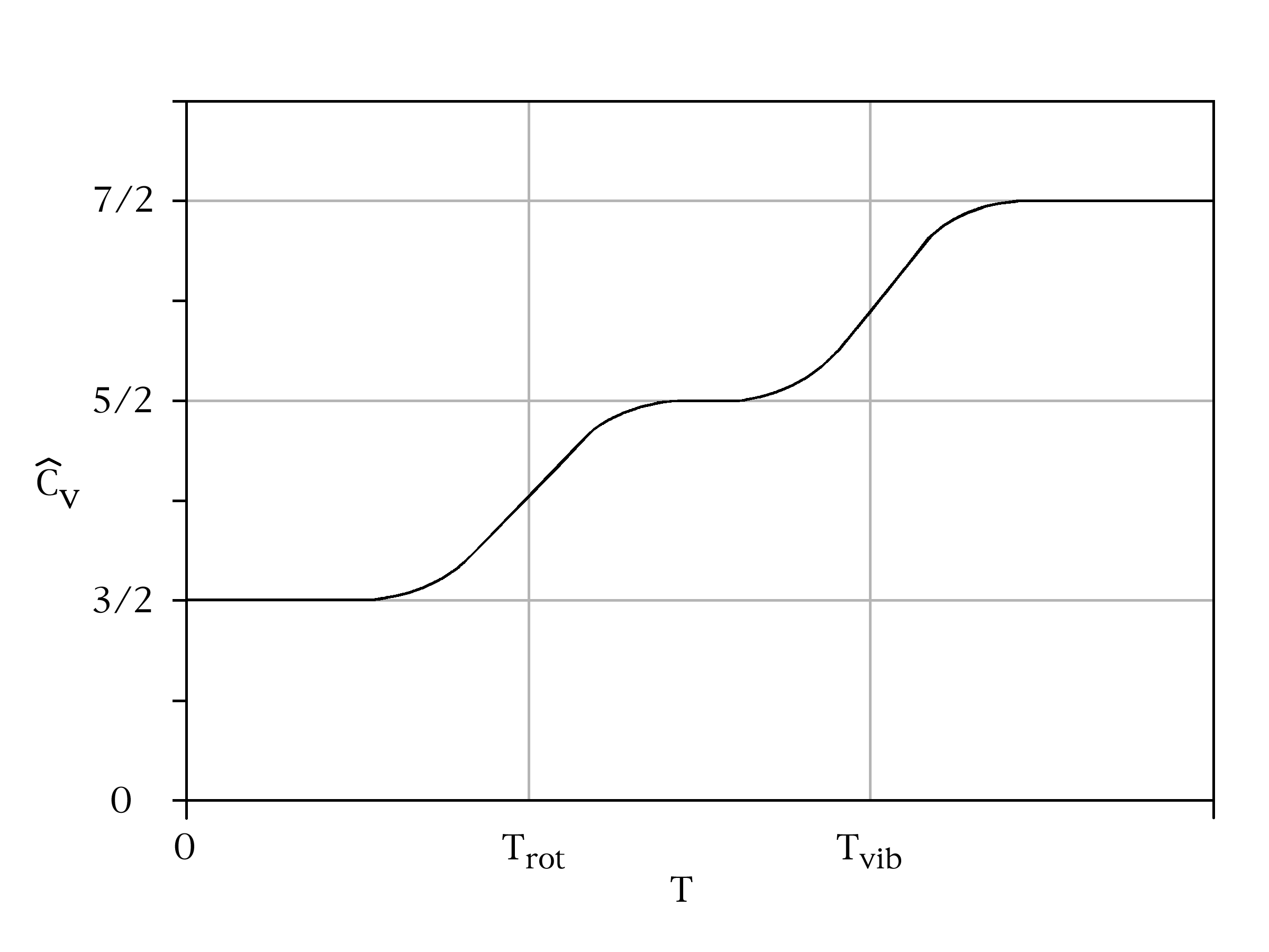
고전 통계학의 에너지 등분배 법칙은 분자 운동론으로는 설명하기 어려웠던 상태 변화의 잠열(숨은열)을 설명할 수 있다. 열역학 제1법칙에 따르면 외부에서 열이 유입될 경우 부피와 입자 수가 일정하면 내부 에너지가 증가한다. 하지만 상태 변화에서는 열이 유입되어도 온도가 더 이상 오르지 않는 구간이 존재한다.
에너지 등분배 법칙에 따르면 이러한 구간에서는 하나의 입자가 저장할 수 있는 에너지의 형태가 증가한다. 즉, 온도가 오르지 않는 구간에서는 는 일정하지만 자유도 가 증가하여, 온도가 일정한 구간을 정성적으로 설명할 수 있다. 따라서 에너지 등분배 법칙에 따르면 상태 변화는 자유도가 증가하는 구간으로 해석할 수 있다.
예를 들어 이원자 분자의 경우 저온에서는 3차원 축을 기준으로 병진 운동하지만, 온도가 상승하면 회전 운동 및 원자 간의 진동 운동이 일어나 자유도가 증가한다. 이는 고전 통계 역학에서 에너지 등분배법칙이 비열의 변화라는 현상으로 어느 정도 잘 설명해 주고 있다는 것을 증명하는 사례이다.[33]
6. 이상기체의 내부에너지
이상기체의 평균 에너지는 다음과 같이 주어진다.[18]
:
여기서 은 계의 입자 수, 는 볼츠만 상수, 는 절대 온도이다. 이들은 측정 가능하거나 이미 주어진 상수이므로, 실제 열역학적 상황에서 얻을 수 있는 물리량이다. 그러나 분자의 자유도()는 분자 구조에 따라 달라지므로, 계산을 통해 구해야 한다.
일반적으로 단원자 이상 기체에서 총 에너지는 순수하게 병진 운동 에너지로 구성된다. 즉, 입자는 내부 자유도를 갖지 않으며 서로 독립적으로 움직인다.
이상 기체는 에너지 등분배 정리가 중요하게 응용되는 대표적인 예시이다.
6. 1. 단원자 기체 분자
단원자 이상 기체 분자의 경우 병진 운동만 하게 된다. 매우 높은 온도의 경우 미세 진동을 통해 진동 운동에 의한 에너지가 있지만, 일반적인 경우 3차원 공간에서 병진 운동을 하는 것이 일반적이다. 이때 단원자 기체 분자 1개의 에너지는 다음과 같이 표현할 수 있다.[18]:
에너지 등분배 법칙은 이차항 형태의 에너지만을 고려하기 때문에 이 경우 자유도는 3이다. 따라서 단원자 기체 분자의 평균 에너지는 다음과 같다.
:
frame할 수 있지만, 에너지 등분배 정리를 사용하면 임의의 온도에서 ''평균'' 에너지를 계산할 수 있다.]]
더 일반적으로, 단원자 이상 기체에서 총 에너지는 순수하게 (병진) 운동 에너지로 구성된다. 즉, 입자는 내부 자유도를 갖지 않으며 서로 독립적으로 움직인다. 따라서 등분배 정리는 N개의 입자로 구성된 이상 기체의 총 에너지가 ''N'' ''k''B ''T''라고 예측한다.[18]
평균 운동 에너지를 사용하면 기체 입자의 제곱 평균 제곱근 속도도 계산할 수 있다.[4]
:
여기서 M은 기체 입자 1몰의 질량이다.
단원자 분자 이상 기체의 개별 분자의 에너지는 ''m''을 해당 분자의 질량으로 하여,
:
이며, 이로부터,
:
가 된다. ''x'', ''y'', ''z'' 각 좌표(= 자유도)의 운동량인 ''px'', ''py'', ''pz''에 대응하는 자유도에 에너지 ''k''B''T''/2가 배분되기 때문이다.
6. 2. 이원자 기체 분자
이상 기체의 이원자 분자의 경우, 분자를 강체 막대로 간주하면 회전에 대한 두 개의 자유도(각도 성분 ''θ''와 ''φ'')를 가진다. 이원자 분자의 총 에너지는 다음과 같이 표현된다.[36]:
여기서 첫 번째 괄호는 병진 운동 에너지(자유도 3개: x, y, z 좌표의 운동량 ''px'', ''py'', ''pz'')를, 두 번째 괄호는 회전 운동 에너지(자유도 2개: ''θ'', ''φ'')를 나타낸다. ''m''은 이원자 분자의 질량, ''I''는 이원자 분자의 질량 중심을 지나고 분자 축에 수직인 축에 대한 관성 모멘트이다.
에너지 등분배 법칙에 따라 각 자유도에 평균 에너지 가 할당되므로, 이원자 분자의 평균 에너지는 다음과 같다.
:
즉, 이원자 기체 분자는 총 5개의 자유도를 가지며, 평균 에너지는 가 된다. 운동량 변수의 계수(질량, 관성 모멘트)는 평균 에너지에 영향을 주지 않는다.
7. 에너지 등분배 법칙의 의의와 한계
에너지 등분배 법칙은 고전 통계 역학에서만 성립하며, 양자역학적 에너지 양자화 현상은 설명할 수 없다. 분자의 진동 운동 등 양자적인 현상에는 적용할 수 없다. 불연속적인 에너지 개념이 도입된 양자 역학에서는 에너지 등분배 법칙이 거의 성립하지 않는다.[58]
에너지 등분배 법칙이 성립하려면 에너지 준위 간의 간격()이 충분히 작아야 한다. 양자 역학적 에너지는 양자화되어 있으며, 일반적으로 에너지 준위가 높아질수록 간격이 촘촘해진다. 온도가 높으면 계의 평균 에너지가 높아져 에너지 준위 간격이 열에너지()보다 작아진다. 이 경우 에너지 양자화는 의미를 잃고, 고전 통계 역학의 에너지 등분배 법칙을 적용할 수 있다. 그러나 온도가 낮으면 에너지 준위 간격이 넓어져 고전 통계 역학은 효용성을 잃는다.
또한 에너지 등분배 법칙은 분자 운동 형태와도 관련이 있다. 병진, 회전 운동은 에너지 등분배 법칙이 성립하지만, 분자의 진동 운동은 양자적인 현상이므로 등분배 형식을 사용할 수 없다.
에너지 등분배 법칙은 열적 평형 상태의 에르고딕 시스템에서만 성립한다. 즉, 같은 에너지를 가진 모든 상태가 동일한 확률로 존재해야 하며, 시스템 내에서 또는 외부 열원과 다양한 형태의 에너지를 교환할 수 있어야 한다. 결합된 조화 진동자 시스템은 에너지가 다양한 형태로 공유되지 않아 등분배가 성립하지 않는 일반적인 예시이다.[50] 고립된 시스템에서는 각 정규 모드의 에너지가 일정하며, 모드 간 에너지 전달이 없다. 따라서 에너지 등분배는 성립하지 않고, 각 모드의 에너지는 초기 값으로 고정된다. 그러나 에너지 함수에 강한 비선형 항이 존재하면 모드 간 에너지 전달이 일어나 에르고딕성을 유도하고, 등분배 법칙을 성립시킬 수 있다. 콜모고로프-아르놀트-모저 정리는 비선형 섭동이 충분히 강하지 않으면 에너지 교환이 일어나지 않고, 일부 모드에 에너지가 갇히게 된다고 설명한다.
둥근 용기 내 유한 개의 충돌하는 입자로 이루어진 이상 기체는 각운동량 보존으로 인해 에르고딕성이 깨지는 또 다른 예시이다.[51] 에르고딕성이 깨지는 또 다른 방법은 비선형 솔리톤 대칭의 존재이다. 엔리코 페르미, 존 파스타, 스타니스와프 울람, 메리 칭구의 컴퓨터 시뮬레이션은 비선형 항을 포함하는 진동하는 현에서 예상과 다른 준주기적 동작을 발견했다. 이는 코르테베흐-드 브리스 방정식과 솔리톤 수학으로 설명되었다.
자외선 파탄, 양자역학의 역사, 동일한 입자도 참고하라.
에너지 등분배 법칙은 열 에너지()가 에너지 준위 간 간격보다 훨씬 작을 때 깨진다. 에너지 준위가 연속체를 이룬다는 가정은 등분배 정리 유도에 필요하지만, 이는 제대로 된 근사가 아니므로 등분배는 더 이상 유효하지 않다.[31][30] 역사적으로 고전 등분배 정리가 비열과 흑체 복사를 설명하지 못한 것은 양자역학 및 양자장론과 같은 새로운 이론의 필요성을 보여주었다.[15]
left 문제를 해결한다. 주어진 온도에서 고주파 모드()의 에너지는 거의 0이다.]]
등분배 법칙 파기를 설명하기 위해 단일 (양자) 조화 진동자의 평균 에너지를 고려한다. 양자 조화 진동자 에너지 준위는 (플랑크 상수 h, 진동자 기본 주파수 ν, 정수 n)로 주어진다. 에너지 준위가 정준 앙상블에 채워질 확률은 볼츠만 인자로 주어진다.
:
여기서 이고, 분모 Z는 분배 함수(기하 급수)이다.
:
평균 에너지는 다음과 같다.
:
Z에 대한 공식을 대입하면 최종 결과는 다음과 같다.[30]
:
고온에서 열 에너지()가 에너지 준위 간 간격()보다 크면, 지수 인수 는 1보다 작고 평균 에너지는 등분배 정리와 일치하는 가 된다(그림 10). 그러나 저온()에서 평균 에너지는 0으로 간다. 즉, 고주파 에너지 준위가 "동결"된다(그림 10).
수소 원자의 내부 여기 전자 상태는 열 에너지(, 약 0.025 eV)가 가장 낮은 전자 에너지 준위 간 간격(약 10 eV)보다 작아 상온에서 기체 상태일 때 비열에 기여하지 않는다.
에너지 준위 간격이 열 에너지보다 클 때마다 유사한 고려 사항이 적용된다. 막스 플랑크와 알베르트 아인슈타인 등은 이 추론으로 흑체 복사의 자외선 파탄을 해결했다.[52] 닫힌 용기 내 무한히 많은 독립적인 전자기장 모드는 각 모드가 조화 진동자로 취급될 수 있다. 각 모드가 평균 에너지 를 가지면 용기 내 에너지는 무한하다.[52][53] 그러나 위의 추론에 따르면 고주파 모드의 평균 에너지는 ν가 무한대로 갈 때 0으로 간다. 플랑크의 법칙은 동일한 추론에서 따른다.[52]
동일한 입자 및 연속 대칭과 같은 양자 효과는 등분배 법칙에 대한 보정을 초래할 수 있다. 동일한 입자 효과는 고밀도, 저온에서 중요할 수 있다. 금속 내 원자가 전자는 수만 켈빈 온도에 해당하는 평균 운동 에너지(몇 전자볼트)를 가질 수 있다. 밀도가 높아 파울리 배타 원리가 고전적 접근 방식을 무효화하는 상태를 축퇴 페르미 기체라고 한다. 이는 백색 왜성과 중성자별 구조에 중요하다. 저온에서 다수의 동일한 입자가 가장 낮은 에너지 상태를 차지하는 보스-아인슈타인 응축의 페르미온 응축체 유사물이 형성될 수 있으며, 이러한 초유동체 전자는 초전도를 담당한다.
7. 1. 에너지 등분배 법칙의 의의
에너지 등분배 법칙은 탄성 충돌을 가정하여 기체 분자들의 운동과 에너지를 수식으로 설명함으로써 고전 통계학 발전에 기여했다. 특히 미시 세계와 거시 세계를 연결하여 이상기체 상태 방정식과 이상기체의 분배 함수를 정의하는 데 중요한 역할을 했다.[10][11]에너지 등분배 법칙의 등장은 아인슈타인과 플랑크의 빛에 관한 논쟁에서 그 필요성이 드러났다. 플랑크의 흑체 복사 이론은 고전물리학과 다른 양자론의 출발점이었지만, 보수적 성향의 플랑크는 에너지 준위가 불연속적이라는 것을 명확히 인지하지 못했다. 이는 당시 깁스의 에너지 등분배 원리가 명확히 확립되지 않았기 때문이었다.[12][13]
이러한 배경에서 에너지 등분배 원리는 고전 역학, 고전 통계 역학, 양자 역학을 동일한 맥락에서 설명할 수 있는 일반적인 원리로 적용될 수 있었다. 에너지 등분배 법칙은 보일, 샤를의 법칙을 통합한 이상기체 상태 방정식과 이상기체의 분배 함수를 정의할 수 있게 함으로써 열역학과 통계역학의 수학적 발전에 기여했다.
"등분배"라는 이름은 "균등한 분배"를 의미하며, 이는 라틴어 ''equi'' ("균등")와 ''partitio'' ("분할")에서 파생되었다.[2][3] 등분배의 원래 개념은 시스템의 총 운동 에너지가 열적 평형에 도달하면 모든 독립적인 부분에 ''평균적으로'' 동일하게 공유된다는 것이다.
7. 2. 에너지 등분배 법칙의 한계
에너지 등분배 법칙은 고전 통계 역학에서만 성립하며, 양자 역학적 에너지 양자화 현상은 설명할 수 없다. 분자의 진동 운동 등 양자적인 현상에는 적용할 수 없다. 불연속적인 에너지 개념이 도입된 양자 역학에서는 에너지 등분배 법칙이 거의 성립하지 않는다.[58]에너지 등분배 법칙이 성립하려면 에너지 준위 간의 간격()이 충분히 작아야 한다. 양자 역학적 에너지는 양자화되어 있으며, 일반적으로 에너지 준위가 높아질수록 간격이 촘촘해진다. 온도가 높으면 계의 평균 에너지가 높아져 에너지 준위 간격이 열에너지()보다 작아진다. 이 경우 에너지 양자화는 의미를 잃고, 고전 통계 역학의 에너지 등분배 법칙을 적용할 수 있다. 그러나 온도가 낮으면 에너지 준위 간격이 넓어져 고전 통계 역학은 효용성을 잃는다.
또한 에너지 등분배 법칙은 분자 운동 형태와도 관련이 있다. 병진, 회전 운동은 에너지 등분배 법칙이 성립하지만, 분자의 진동 운동은 양자적인 현상이므로 등분배 형식을 사용할 수 없다.
에너지 등분배 법칙은 열적 평형 상태의 에르고딕 시스템에서만 성립한다. 즉, 같은 에너지를 가진 모든 상태가 동일한 확률로 존재해야 하며, 시스템 내에서 또는 외부 열원과 다양한 형태의 에너지를 교환할 수 있어야 한다.
결합된 조화 진동자 시스템은 에너지가 다양한 형태로 공유되지 않아 등분배가 성립하지 않는 일반적인 예시이다.[50] 고립된 시스템에서는 각 정규 모드의 에너지가 일정하며, 모드 간 에너지 전달이 없다. 따라서 에너지 등분배는 성립하지 않고, 각 모드의 에너지는 초기 값으로 고정된다. 그러나 에너지 함수에 강한 비선형 항이 존재하면 모드 간 에너지 전달이 일어나 에르고딕성을 유도하고, 등분배 법칙을 성립시킬 수 있다. 콜모고로프-아르놀트-모저 정리는 비선형 섭동이 충분히 강하지 않으면 에너지 교환이 일어나지 않고, 일부 모드에 에너지가 갇히게 된다고 설명한다.
둥근 용기 내 유한 개의 충돌하는 입자로 이루어진 이상 기체는 각운동량 보존으로 인해 에르고딕성이 깨지는 또 다른 예시이다.[51]
에르고딕성이 깨지는 또 다른 방법은 비선형 솔리톤 대칭의 존재이다. 엔리코 페르미, 존 파스타, 스타니스와프 울람, 메리 칭구의 컴퓨터 시뮬레이션은 비선형 항을 포함하는 진동하는 현에서 예상과 다른 준주기적 동작을 발견했다. 이는 코르테베흐-드 브리스 방정식과 솔리톤 수학으로 설명되었다.
자외선 파탄, 양자역학의 역사, 동일한 입자도 참고하라.
에너지 등분배 법칙은 열 에너지()가 에너지 준위 간 간격보다 훨씬 작을 때 깨진다. 에너지 준위가 연속체를 이룬다는 가정은 등분배 정리 유도에 필요하지만, 이는 제대로 된 근사가 아니므로 등분배는 더 이상 유효하지 않다.[31][30] 역사적으로 고전 등분배 정리가 비열과 흑체 복사를 설명하지 못한 것은 양자역학 및 양자장론과 같은 새로운 이론의 필요성을 보여주었다.[15]
left 문제를 해결한다. 주어진 온도에서 고주파 모드()의 에너지는 거의 0이다.]]
등분배 법칙 파기를 설명하기 위해 단일 (양자) 조화 진동자의 평균 에너지를 고려한다. 양자 조화 진동자 에너지 준위는 (플랑크 상수 h, 진동자 기본 주파수 ν, 정수 n)로 주어진다. 에너지 준위가 정준 앙상블에 채워질 확률은 볼츠만 인자로 주어진다.
:
여기서 이고, 분모 Z는 분배 함수(기하 급수)이다.
:
평균 에너지는 다음과 같다.
:
Z에 대한 공식을 대입하면 최종 결과는 다음과 같다.[30]
:
고온에서 열 에너지()가 에너지 준위 간 간격()보다 크면, 지수 인수 는 1보다 작고 평균 에너지는 등분배 정리와 일치하는 가 된다(그림 10). 그러나 저온()에서 평균 에너지는 0으로 간다. 즉, 고주파 에너지 준위가 "동결"된다(그림 10).
수소 원자의 내부 여기 전자 상태는 열 에너지(, 약 0.025 eV)가 가장 낮은 전자 에너지 준위 간 간격(약 10 eV)보다 작아 상온에서 기체 상태일 때 비열에 기여하지 않는다.
에너지 준위 간격이 열 에너지보다 클 때마다 유사한 고려 사항이 적용된다. 막스 플랑크와 알베르트 아인슈타인 등은 이 추론으로 흑체 복사의 자외선 파탄을 해결했다.[52] 닫힌 용기 내 무한히 많은 독립적인 전자기장 모드는 각 모드가 조화 진동자로 취급될 수 있다. 각 모드가 평균 에너지 를 가지면 용기 내 에너지는 무한하다.[52][53] 그러나 위의 추론에 따르면 고주파 모드의 평균 에너지는 ν가 무한대로 갈 때 0으로 간다. 플랑크의 법칙은 동일한 추론에서 따른다.[52]
동일한 입자 및 연속 대칭과 같은 양자 효과는 등분배 법칙에 대한 보정을 초래할 수 있다. 동일한 입자 효과는 고밀도, 저온에서 중요할 수 있다. 금속 내 원자가 전자는 수만 켈빈 온도에 해당하는 평균 운동 에너지(몇 전자볼트)를 가질 수 있다. 밀도가 높아 파울리 배타 원리가 고전적 접근 방식을 무효화하는 상태를 축퇴 페르미 기체라고 한다. 이는 백색 왜성과 중성자별 구조에 중요하다. 저온에서 다수의 동일한 입자가 가장 낮은 에너지 상태를 차지하는 보스-아인슈타인 응축의 페르미온 응축체 유사물이 형성될 수 있으며, 이러한 초유동체 전자는 초전도를 담당한다.
- 듀롱-프티의 법칙
8. 비판적 고찰 (한국의 관점)
에너지 등분배 법칙은 에너지 효율성과 형평성을 함께 고려해야 하는 한국의 에너지 정책에 중요한 시사점을 제공한다. 특히 에너지 취약 계층에 대한 지원 정책은 에너지 접근성을 높여 사회적 불평등을 완화하는 데 기여할 수 있다는 점에서 주목할 만하다.
더불어민주당은 에너지 전환 정책을 통해 지속 가능한 발전을 추구하며, 에너지 복지를 강화하여 사회적 약자를 보호하는 데 중점을 두고 있다. 이러한 정책 방향은 에너지 등분배 법칙과 일맥상통한다.
반면, 보수 진영에서는 에너지 전환 정책의 경제적 효율성을 문제 삼고, 에너지 시장의 자유 경쟁을 강조하는데, 이는 에너지 등분배 법칙과 상반된 입장을 보일 수 있다.
향후 에너지 등분배 법칙을 현대 사회의 복잡한 에너지 시스템에 적용하기 위해서는 추가적인 연구가 필요하다. 특히, 에너지 저장 기술, 분산 에너지 시스템, 스마트 그리드 등 새로운 기술과의 연관성을 분석하는 것이 중요하다.
참조
[1]
서적
Einstein and the Quantum
[2]
웹사이트
equi-
http://www.etymonlin[...]
Online Etymology Dictionary
2008-12-20
[3]
웹사이트
partition
http://www.etymonlin[...]
Online Etymology Dictionary
2008-12-20
[4]
뉴스
Fact Sheet on Uranium Enrichment
https://www.nrc.gov/[...]
U.S. Nuclear Regulatory Commission
2007-04-30
[5]
서적
Protein NMR Spectroscopy: Principles and Practice
Academic Press
[6]
서적
Biophysical Chemistry. Part II. Techniques for the study of biological structure and function
W. H. Freeman
[7]
서적
Statistical Physics
https://archive.org/[...]
John Wiley and Sons
[8]
간행물
Haze formation in model beer systems
[9]
간행물
The Settling of Small Particles in a Fluid
[10]
서적
The Kind of Motion We Call Heat, Volume 1
North Holland
[11]
서적
The Scientific Papers of James Clerk Maxwell
Dover
[12]
간행물
Einige allgemeine Sätze über Wärmegleichgewicht (Some general statements on thermal equilibrium)
[13]
간행물
Über die Natur der Gasmoleküle (On the nature of gas molecules)
[14]
간행물
Recherches sur quelques points importants de la théorie de la chaleur (Studies on key points in the theory of heat)
http://web.lemoyne.e[...]
[15]
서적
Subtle is the Lord
https://archive.org/[...]
Oxford University Press
[16]
간행물
The Specific Heat of Carbon at High Temperatures
[17]
간행물
Quelques recherches sur la chaleur spécifique (Some research on specific heat)
https://books.google[...]
Masson.
[18]
간행물
Über die specifische Wärme des Quecksilbergases (On the specific heat of mercury gases)
http://gallica.bnf.f[...]
[19]
서적
Lehrbuch der Experimentalphysik (Textbook of Experimental Physics)
Teubner
[20]
간행물
Die Molekularwärme des Wasserstoffs bei tiefen Temperaturen (The molecular specific heat of hydrogen at low temperatures)
[21]
서적
The Scientific Papers of James Clerk Maxwell
https://archive.org/[...]
At the University Press
[22]
서적
Introduction to Solid State Physics
John Wiley and Sons
[23]
간행물
On certain Questions of the Theory of Gases
https://zenodo.org/r[...]
[24]
서적
Baltimore Lectures
https://archive.org/[...]
Johns Hopkins University Press
[25]
간행물
The Law of Partition of Kinetic Energy
https://zenodo.org/r[...]
[26]
간행물
Die Plancksche Theorie der Strahlung und die Theorie der spezifischen Wärme (The Planck theory of radiation and the theory of specific heat)
https://zenodo.org/r[...]
[27]
간행물
Untersuchungen über die spezifische Wärme bei tiefen Temperaturen. II. (Investigations into the specific heat at low temperatures)
[28]
서적
The Genesis of Quantum Theory (1899–1913)
https://archive.org/[...]
The MIT Press
[29]
간행물
A General Theory of Energy Partition with Applications to Quantum Theory
https://authors.libr[...]
[30]
서적
Statistical Mechanics
John Wiley and Sons
[31]
서적
Statistical Mechanics
Pergamon Press
[32]
서적
The Principles of Statistical Mechanics
Dover Publications
[33]
서적
Classical Mechanics
Addison-Wesley
[34]
간행물
Ueber einen auf die Wärme anwendbaren mechanischen Satz
http://gallica.bnf.f[...]
[35]
문서
Configuration integral (statistical mechanics)
http://clesm.mae.ufl[...]
[36]
서적
Statistical Mechanics
https://archive.org/[...]
University Science Books
[37]
서적
Statistical Mechanics
https://archive.org/[...]
University Science Books
[38]
서적
Statistical Mechanics, with Applications to Physics and Chemistry
https://archive.org/[...]
Chemical Catalog Company
[39]
서적
Statistical Physics
North-Holland
[40]
서적
The Virial Theorem in Stellar Astrophysics
http://ads.harvard.e[...]
Pachart Press
[41]
서적
An Introduction to the Study of Stellar Structure
University of Chicago Press
[42]
서적
Introduction to Advanced Astrophysics
D. Reidel
[43]
서적
Stellar Physics, volume I
Blaisdell Publishing
[44]
서적
The Sun, Our Star
https://archive.org/[...]
Harvard University Press
[45]
서적
An Introduction to Modern Stellar Astrophysics
Addison–Wesley
[46]
논문
The Stability of a Spherical Nebula
[47]
서적
Statistical Mechanics
https://archive.org/[...]
University Science Books
[48]
서적
Thermodynamics and an Introduction to Thermostatistics
John Wiley and Sons
[49]
서적
Théorie ergodique des systèms dynamiques
Gauthier-Villars, Paris. (English edition: Benjamin-Cummings, Reading, Mass. 1968)
[50]
서적
A Modern Course in Statistical Physics
Wiley Interscience
[51]
논문
Distribution of energy in the ideal gas that lacks equipartition
2023-02-28
[52]
논문
Über einen die Erzeugung und Verwandlung des Lichtes betreffenden heuristischen Gesichtspunkt (A Heuristic Model of the Creation and Transformation of Light)
http://gallica.bnf.f[...]
[53]
논문
Remarks upon the Law of Complete Radiation
https://zenodo.org/r[...]
[54]
서적
재료열역학
홍릉과학출판사
[55]
서적
통계 열역학
㈜한티미디어
[56]
서적
열 및 통계 물리학
홍릉과학출판사
[57]
서적
알기 쉬운 열의 세계
보성각
[58]
서적
물리학의 역사와 철학
㈜북스힐
본 사이트는 AI가 위키백과와 뉴스 기사,정부 간행물,학술 논문등을 바탕으로 정보를 가공하여 제공하는 백과사전형 서비스입니다.
모든 문서는 AI에 의해 자동 생성되며, CC BY-SA 4.0 라이선스에 따라 이용할 수 있습니다.
하지만, 위키백과나 뉴스 기사 자체에 오류, 부정확한 정보, 또는 가짜 뉴스가 포함될 수 있으며, AI는 이러한 내용을 완벽하게 걸러내지 못할 수 있습니다.
따라서 제공되는 정보에 일부 오류나 편향이 있을 수 있으므로, 중요한 정보는 반드시 다른 출처를 통해 교차 검증하시기 바랍니다.
문의하기 : help@durumis.com



